分液和萃取 知识点题库
-
(1) 除去豆浆中的颗粒物杂质
-
(2) 用海水晒盐
-
(3) 除去豆油中的水
-
(4) 从碘水中提取碘
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液,0.1000mol/L盐酸 |
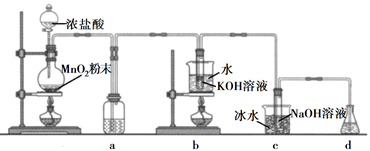
回答下列问题:
-
(1) 盛放MnO2粉末的仪器名称是,a中的试剂为。
-
(2) b中采用的加热方式是,c中化学反应的离子方程式是,采用冰水浴冷却的目的是。
-
(3) d的作用是,可选用试剂(填标号)。
A.Na2S B.NaCl C.Ca(OH)2 D.H2SO4
-
(4) 反应结束后,取出b中试管,经冷却结晶,,,干燥,得到KClO3晶体。
-
(5) 取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显色。可知该条件下KClO3的氧化能力NaClO(填“大于”或“小于")。
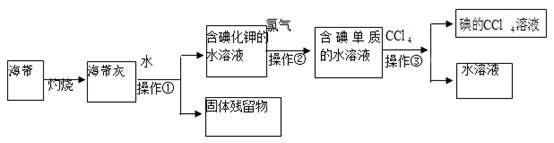
请回答下列问题:
-
(1) 操作①的名称为、;
-
(2) 向含碘单质的水溶液中加入CCl4振荡、静置后,观察到的现象是;
-
(3) 操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是。
-
(4) 从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶、牛角管外,还需要,实验中温度计水银球所处位置为。

-
(1) 滤渣I的主要成分是(填化学式),写出一种能提高酸浸速率的措施。
-
(2) 操作①用到的玻璃仪器有。
-
(3) 加入氧化钴的目的是调节溶液的pH。若要将浸出液中Fe3+和Al3+完全沉淀,则浸出液的pH范围应控制在(已知:溶液中离子浓度小于1×10-5mol/L,则认为离子完全沉淀; Ni(OH)2、Fe(OH)3 、Al(OH)3 的Ksp 分别为1×10-15 , 1×10-38 , 1×10-32;Kw=1×10‑14)。
-
(4) 加入有机萃取剂的目的是。
-
(5) “反萃取”原理是用反萃取剂使被萃取物从有机相返回水相的过程。向操作①后溶有NiR2 的有机层中加入硫酸溶液,可重新得到RH,写出该步骤反应的离子方程式。
-
(6) 300℃时,在空气中煅烧CoC2O4• 2H2O晶体可制得Co3O4 , 该反应的化学方程式为。
 B .
B . 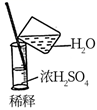 C .
C . 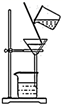 D .
D . 
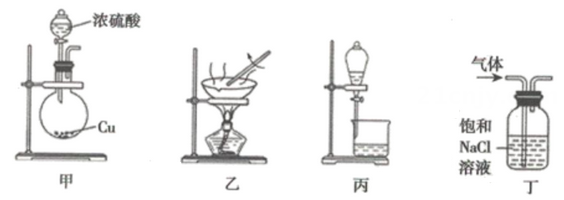
| 选项 | 操作或做法 | 目的 |
| A | 将铜丝插入浓硝酸中 | 制备 |
| B | 将密闭烧瓶中的 | 探究温度对平衡移动的影响 |
| C | 将溴水滴入 | 萃取溶液中生成的碘 |
| D | 实验结束,将剩余 | 节约试剂 |
| 选项 | 实验操作和现象 | 结论 |
| A | 向FeCl2和KSCN的混合溶液中滴入硝酸酸化的AgNO3溶液,溶液变红 | 氧化性:Fe3+<Ag+ |
| B | 将蘸有浓氨水的玻璃棒靠近溶液X,有白烟产生 | 溶液X一定是浓盐酸 |
| C | 将电石与水反应产生的气体通入溴水,溴水褪色 | 生成的乙炔气体中含有H2S |
| D | 向碘水中加入等体积CCl4 , 振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
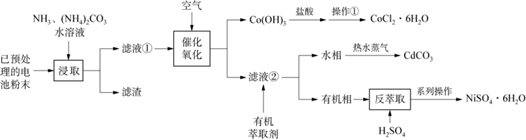
已知:Ⅰ.滤液①中含有Ni(NH3)62+、Cd(NH3)42+、Co(NH3) 62+等物质。
Ⅱ.萃取和反萃取的反应原理分别为:
Ni(NH3)62++ 2HR  NiR2+2NH4++4NH3 ;NiR2+2H+
NiR2+2NH4++4NH3 ;NiR2+2H+  Ni2+ +2HR
Ni2+ +2HR
-
(1) 为了加快浸取速率,可采取的措施为(任写一条)。
-
(2) 已知浸取过程中NH3和NH4+的物质的量之和与Ni、Cd、Co浸取率的关系如表2所示。
表2浸取过程中氨总量与各离子浸取率的关系
编号
n(NH3)+
n(NH4+)/mol
Ni浸取率/%
Cd浸取率/%
Co浸取率/%
①
2.6
97.2
88.6
98.1
②
3.5
86.0
98.8
86.7
③
4.8
98.4
98.8
94.9
④
5.6
97.7
85.1
96.8
⑤
9.8
95.6
84.1
96.1
则可采用的最佳实验条件编号为。
-
(3) Co(OH)3与盐酸反应产生气体单质,该反应的化学方程式。
-
(4) 操作①的名称为、过滤、洗涤。
-
(5) 向有机相中加入H2SO4能进行反萃取的原因为(结合平衡移动原理解释)。
-
(6) 将水相加热并通入热水蒸气会生成CdCO3沉淀,并产生使红色石蕊试纸变蓝的气体,该反应的离子方程式为。
-
(7) 上述工艺流程中可能循环使用的物质为。
-
(8) 已知Ksp(CdCO3)=1.0×10-12 , Ksp(NiCO3)=1.4×10-7。若向物质的量浓度均为0.2mol/L的Cd2+和Ni2+溶液中滴加Na2CO3溶液(设溶液体积增加1倍),使Cd2+恰好沉淀完全,即溶液中c(Cd2+)=1.0×10-5mol/L时,是否有NiCO3沉淀生成(填“是”或者“否”)。
 B .
B .  C .
C .  D .
D . 
 ),下列有关说法正确的是( )
),下列有关说法正确的是( ) 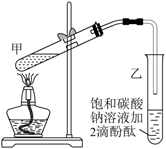
 、2mL浓硫酸和2mL
、2mL浓硫酸和2mL  B . 乙试管中的饱和碳酸钠溶液可以换成氢氧化钠溶液
C . 从乙试管中分离得到纯净干燥的乙酸乙酯的操作是:振荡、静置、分液
D . 生成的乙酸乙酯的结构简式为
B . 乙试管中的饱和碳酸钠溶液可以换成氢氧化钠溶液
C . 从乙试管中分离得到纯净干燥的乙酸乙酯的操作是:振荡、静置、分液
D . 生成的乙酸乙酯的结构简式为 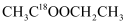

-
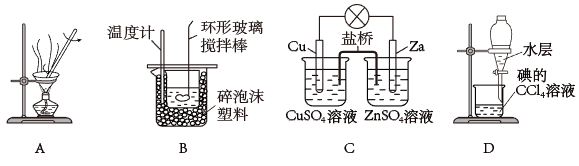
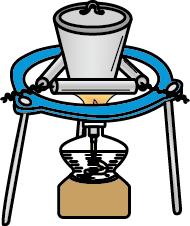
(1) 实验室焙烧海带,需要下列仪器中的(填字母)。
a.试管b.烧杯c.坩埚d.泥三角e.铁三脚架f.酒精灯
-
(2) 指出提取碘的过程中有关的实验操作名称:①,③。
-
(3) 提取碘的过程中,可选择的有机试剂是____。A . 甲苯、酒精 B . 四氧化碳、苯 C . 汽油、乙酸 D . 汽油、甘油
-
(4) 为使海藻灰中破离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有、。
-
(5) 某学习小组用
 萃取碘水中的碘,在如图的分液漏斗中,下层液体呈色;他们打开分液漏斗活塞,却未见液体流下,原因可能是。
萃取碘水中的碘,在如图的分液漏斗中,下层液体呈色;他们打开分液漏斗活塞,却未见液体流下,原因可能是。
-
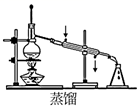
(6) 从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏。进行上述蒸馏操作时,使用了水浴加热。使用水浴加热的原因是。
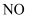
 降温
降温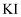 溶液中,加入乙醇并振荡
溶液中,加入乙醇并振荡 固体放回原试剂瓶
固体放回原试剂瓶


