分液和萃取 知识点题库
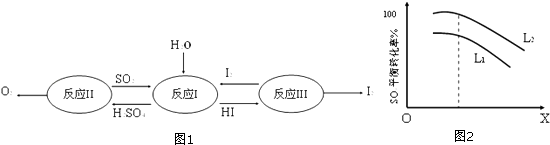
完成下列填空
-
(1) 反应Ⅰ的化学方程式是.
反应Ⅰ得到的产物用I2进行分离.该产物的溶液在过量I2的存在下会分成两层﹣﹣含低浓度I2的H2SO4层和高浓度的I2的HI层.
-
(2) 根据上述事实,下列说法正确的是(选填序号).
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
-
(3) 辨别两层溶液的方法: ,
-
(4) 经检测,H2SO4层中c(H+):c(SO
 )=2.06:1.其比值大于2的原因是.
)=2.06:1.其比值大于2的原因是. 反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g)﹣1100kJ 它由两步反应组成:
i.H2SO4(l)→SO3(g)+H2O(g)﹣177kJ ii.SO3(g)分解.
L(L1、L2),X可分别代表压强或温度.图2表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系.
-
(5) X代表的物理量是,推断的依据是.
-
(6) 判断L1和L2的大小,并简述理由.
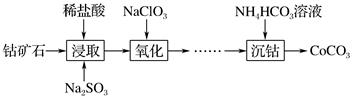
下表列出了几种离子生成氢氧化物沉淀的pH(“沉淀完全”是指溶液中离子浓度低于1.0×10-5 mol·L-1)
| Al3+ | Fe3+ | Fe2+ | Mn2+ | Co2+ | |
| 开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.7 | 7.6 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.8 | 9.2 |
-
(1) 写出“浸取”步骤Co2O3·CoO发生反应的离子方程式 。
-
(2) “浸取”步骤除Co2O3·CoO外,钴矿石中还能被Na2SO3还原的物质有 (填化学式)。
-
(3) 加NaClO3的目的是氧化Fe2+ , NaClO3的用量过多会造成的不良后果是 。
-
(4) “沉钴”步骤向CoCl2溶液加入NH4HCO3溶液需要55~57 ℃条件下进行,温度控制在55~57℃的原因为 。
-
(5) 已知金属萃取剂对金属离子的萃取率与pH的关系如图所示。
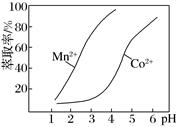
请补充完整由“氧化”后的溶液制备CoCO3的实验方案:向“氧化”后的溶液中加入,得较纯CoCl2溶液,加入NH4HCO3溶液沉钴得CoCO3。(实验中须使用试剂:Na2CO3溶液、金属萃取剂、盐酸)。
A.干馏 B.萃取 C.分液
-
(1) 四氯化碳和水的混合物的分离;
-
(2) 把煤转化为焦炉气、煤焦油和焦炭等;
-
(3) 海水提溴获得的溴水中,用苯提取溴单质 。
①用NaCl固体配制一定物质的量浓度的溶液
②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④从含NaCl的溶液中获得蒸馏水 ⑤用CCl4萃取碘水中的碘

-
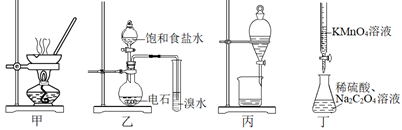
(1) Ⅰ.某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。请回答下列问题:
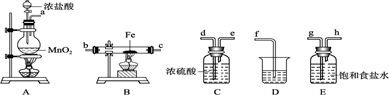
A 中发生反应的化学方程式为。在该反应中当 0.4molHCl发生反应时,生成标准状况下的Cl2 的体积为。浓盐酸在反应中显示出来的性质是(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
-
(2) 各装置的正确连接顺序为(填写装置代号)A→→→→D。
-
(3) 装置 E 的作用是。写出装置 D(D中所盛溶液为 NaOH)中反应的化学方程式
-
(4) 工业上用电解法制备氯气的化学方程式为:。
-
(5) Ⅱ.某小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈色;他们打开分液漏斗活塞,却未见液体流下,原因可能是
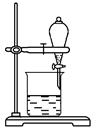
 B .
B . 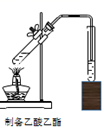 C .
C . 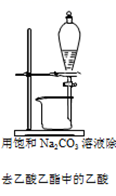 D .
D . 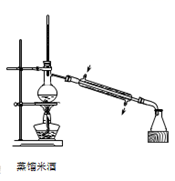
|
十八醇 |
丙烯酸 |
甲苯 |
丙烯酸十八酯 |
| |
| 相对分子质量 | 270 | 72 | 92 | 324 | |
| 密度/g•cm-3 | 0.81 | 1.05 | 0.90 | 0.80 | |
| 沸点/℃ | 210 | 141 | 110.6 | 402 | |
| 说中溶解度 | 难溶 | 可溶 | 难溶 | 难溶 | |
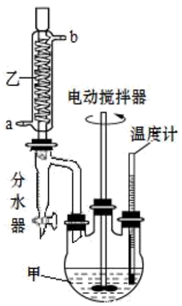
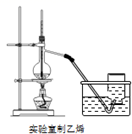
| 实验步骤: Ⅰ.向仪器甲中依次加入十八醇(C18H37OH)、阻凝剂、携水分 剂,安装好其他仪器。 Ⅱ.搅拌、加热,瓶内试剂完全溶解后加入丙烯酸、催化剂,加热至回流温度115~120℃,待分水器水量达到理论量时停止甲加热。 Ⅲ.取甲中产物倒入分液漏斗中,先后用5%Na2CO3溶液和蒸馏水多次洗涤,分液后有机层加入无水MgSO4 , 静置、过滤,得粗产品,进一步提纯,得纯净产品。 | |||||
回答下列问题:
-
(1) 仪器甲名称,仪器乙的作用为。
-
(2) 步骤Ⅱ生成丙烯酸十八酯的反应方程式为,保持回流温度恒定可采用的加热方式为(填标号)
a.沸水浴 b.盐浴 c.电加热套 d.油浴
-
(3) 为将反应生成的水及时移出,需加入携水剂。实验选用甲苯做携水剂的原因。
-
(4) 用5%Na2CO3溶液水洗的目的,加入无水MgSO4的目的。
-
(5) 步骤Ⅲ进一步提纯,在该提纯步骤中会用到的仪器有(填标号)。
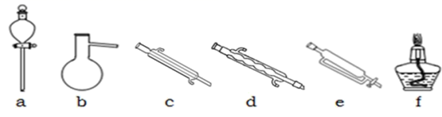
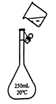 B . 制蒸馏水
B . 制蒸馏水 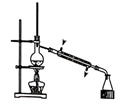 C . 收集HCl气体
C . 收集HCl气体 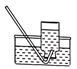 D . 分离苯与水
D . 分离苯与水 

有关 X 的说法正确的是( )
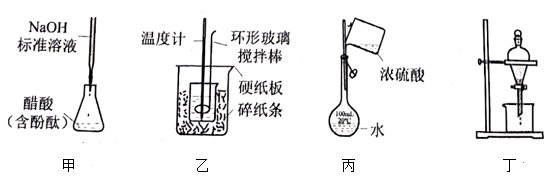
 标准溶液
B . 从食盐水中得到
标准溶液
B . 从食盐水中得到 晶体,当坩埚中出现大量固体时,停止加热,利用余热蒸干
C . 用苯萃取溴水中的
晶体,当坩埚中出现大量固体时,停止加热,利用余热蒸干
C . 用苯萃取溴水中的 , 分离时溴和苯的混合溶液从分液漏斗下口放出
D . 配制一定物质的量浓度溶液时,将量取好的物质放入容量瓶中,加水溶解至刻度线
, 分离时溴和苯的混合溶液从分液漏斗下口放出
D . 配制一定物质的量浓度溶液时,将量取好的物质放入容量瓶中,加水溶解至刻度线