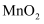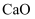常见气体制备原理及装置选择 知识点题库
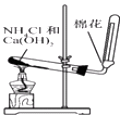 制取NH3
B .
制取NH3
B . 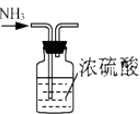 干燥NH3
C .
干燥NH3
C . 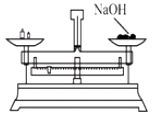 称量NaOH固体
D .
称量NaOH固体
D .  石油的分馏
石油的分馏
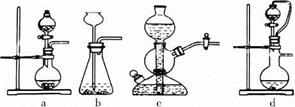
下图装置可用于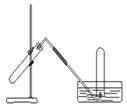
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒.
实验步骤:
(1)实验开始时,必须进行的第一步操作是检验装置的 ;
(2)向试管中加入一定量的固体药品 ,然后倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞,其目的是
(3)反应一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
(4)将铜丝向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是 ;
(5)将注射器插入试管口的橡皮塞中,向试管内推入空气,现象是
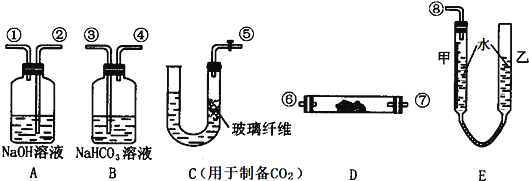
某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积.图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水.甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低.
实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水.
请回答:
(1)图中各装置接口连接顺序是:(填各接口的编号,其中连接胶管及夹持装置均省略)
→ → →⑥→⑦→ → →
(2)装置C中放入的反应物是 和 (填化学式).
(3)装置B的作用是 .
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意 (填字母编号).
a.视线与凹液面最低处相平
b.等待气体恢复常温才读数
c.读数时应上下移动乙管,使甲乙两管液面相平
d.读数时不一定使甲乙两管液面相平
(5)实验测收集的氧气在标准状况下体积为V L,则参与反应的Na2O2 的物质的量为 mol.
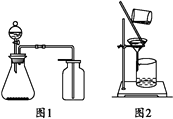
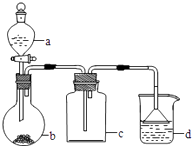
选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | 浓盐酸 | HCl | NaOH溶液 |
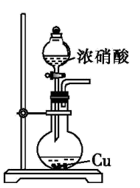
C | 稀硝酸 | Cu | NO2 | H2O |
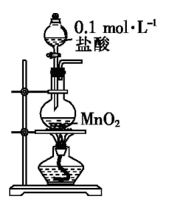
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
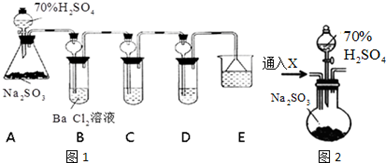
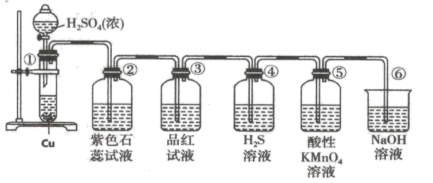
根据要求回答下列问题:
-
(1) 装置A中反应的化学方程式为。
-
(2) 利用装置C可以证明SO2具有漂白性,C中盛放的溶液是。
-
(3) 通过观察D中现象,即可证明SO2具有氧化性,D中盛放的溶液可以是________。A . NaCl溶液 B . 酸性KMnO4 C . FeCl3 D . Na2S溶液
-
(4) 研究小组发现B中有白色沉淀BaSO4生成,为进一步验证B中产生沉淀的原因,研究小组进行如下两次实验:
实验i:另取BaCl2溶液,加热煮沸,冷却后加入少量苯(起液封作用),然后再按照上述装置进行实验,结果发现B中沉淀量减少,但仍有轻微浑浊.
实验ii:用如上图2的F装置代替上述实验中的A装置(其他装置不变),连接后往装置F中通入气体X一段时间,再加入70%H2SO4溶液,结果B中没有出现浑浊.
①“实验i”中煮沸BaCl2溶液的目的是;
②气体X可以是(填序号)。
A.CO2
B.Cl2
C.N2
D.NO2
③B中形成沉淀的原因是(用化学方程式表示):。
 B .
B . 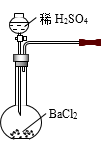 C .
C . 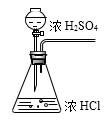 D .
D . 
-
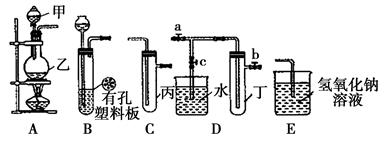
(1) 利用B装置可制备的气体有(写出一种即可)。
-
(2) 若装置A,C,E相连后用于制取Cl2 , 写出A中发生的离子方程式。 若要收集到纯净干燥的氯气,需要在装置A、C之间增加两个装有和的洗气瓶(填写试剂的名称)。
-
(3) 若装置A、C、E相连后用于制取SO2 , 尾气吸收时容易发生倒吸现象,改进措施为。
-
(4) 若装置B、D、E相连后可制得NO2并进行有关实验。欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹,再打开止水夹,微热试管丁使烧杯中的水进入丁中,充分反应后,若向试管中通入一定量的氧气至试管内完全充满液体,则所得溶液中溶质的物质的量浓度是 mol/L(气体按标准状况计算)。
-
(1) I.
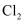 是一种重要的化工原料,下图是一些含氯产品:
是一种重要的化工原料,下图是一些含氯产品: ①
 ②
②  ③
③  ④
④  ⑤
⑤ 
①中钢瓶上应贴的标签为___________。
A . 腐蚀品 B . 爆炸品 C . 有毒品 D . 易燃品 -
(2) 化学工业中通过“氯碱工业”制取氯气等产品,其化学方程式为。
-
(3) 制备“84消毒液”(有效成分为
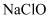 )的化学方程式为。
)的化学方程式为。
-
(4) 工业上将氯气通入石灰乳中制取漂白粉,其有效成分是(填化学式)。
-
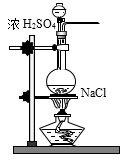
(5) II.实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以利用反应:
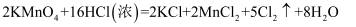 制取并收集纯净、干燥的氯气,部分装置如图所示:
制取并收集纯净、干燥的氯气,部分装置如图所示: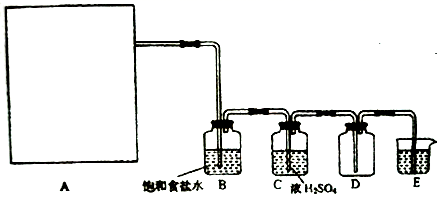
若以
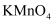 和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置(填代号)。
和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置(填代号)。a.
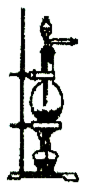 b.
b. 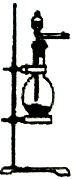 c.
c. 
-
(6) 装置B的作用。
-
(7) E中的试剂可选___________。A .
 溶液
B .
溶液
B .  溶液
C .
溶液
C .  溶液
D . 水
溶液
D . 水
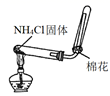 B . 分离乙酸乙酯和乙醇
B . 分离乙酸乙酯和乙醇 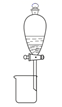 C . 制备无水氯化镁
C . 制备无水氯化镁 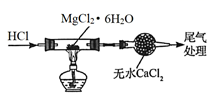 D . 实验室制备SO2
D . 实验室制备SO2 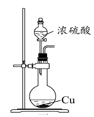
-
(1) Na2S2O4用于保鲜剂时能去除O2 , 先生成Na2SO3并缓慢释放SO2 , 该反应的化学方程式为。
-
(2) 锌粉法制备Na2S2O4的工艺流程如图所示:
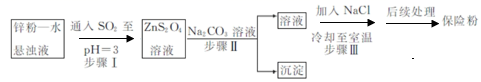
①实验室可用浓硫酸和亚硫酸钠反应制取SO2 , 并希望能控制反应速度,图中可选用的发生装置是(填字母)。
②工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是。步骤Ⅱ中发生反应的化学方程式为。
③在步骤.中得到的Na2S2O4固体要用乙醇洗涤,其优点是。
-
(3) 目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将HCOONa和烧碱加入乙 醇水溶液液中,然后通入SO2发生反应,有CO2气体放出,总反应的化学方程式是。
-
(4) 连二亚硫酸钠的分析检测。铁氰化钾法:铁氰化钾K3[Fe(CN)6]是一种比较弱的氧化剂,其具有强氧化剂所没有的选择性氧化性,能将S2O42-氧化为SO32- , [Fe(CN)6]3-还原为[Fe(CN)6]4-。取50.00mLNa2S2O4样品溶液,用0.02mol•L-1的K3[Fe(CN)6]标准液滴定至终点,消耗10.00mL。该样品中Na2S2O4的含量为g•L-1。(以SO2计)
-
(1) 甲组的同学拟制备原料气NO和Cl2 , 制备装置如下图所示:

①制备NO发生装置可以选用(填写字母代号),请写出发生反应的离子方程式:。
②欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→ (按气流方向,用小写字母表示)。
-
(2) 乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①实验室也可用X装置制备NO,X装置的优点为。
②检验装置气密性并装入药品,打开K2 , 然后再打开 ,通入一段时间气体,其目的为,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中NOCl可能发生反应的化学方程式为。
④若尾气处理装置连接上图烧杯中导管d,则烧杯中可加入 溶液。
-
(1) 在①中发生的化学反应方程式为;
-
(2) ②中实验现象是,证明
 有性质;
有性质;
-
(3) ③中的品溶液,证明
 有性质;
有性质;
-
(4) ④中实验现象是,证明
 有性质;
有性质;
-
(5) ⑥中反应的离子方程式为。
| A | B | C | D |
| | | | |
| 制备 | 制备 | 收集 | 制备 |
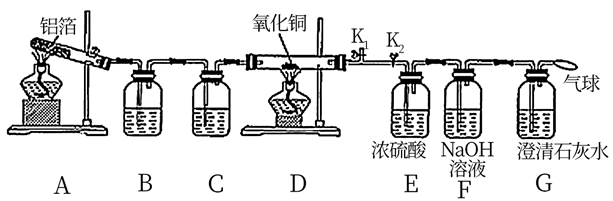
查阅资料得:实验室制取甲烷常用的方法为无水醋酸钠(CH3COONa)与氢氧化钠在二氧化锰作催化剂的条件下共热,产物中有少量的副产物丙酮(CH3COCH3),丙酮可与水混溶。
-
(1) 组装好仪器后,首先进行的操作是,实验中先点燃(填“A”或“D”)处酒精灯,目的是,此时K1、K2的状态为(填标号)。
A. K1关闭、K2关闭
B. K1关闭、K2打开
C.K1打开、K2打开
D.K1打开、K2关闭
-
(2) 装置A中主要发生反应的化学方程式为,试管内壁加一层铝箔不仅能使药品受热均匀,还能。
-
(3) 装置B中盛装的试剂为。
-
(4) 实验过程中记录的实验数据如下:
装置
D
E
F
G
实验前装置总质量/g
180.0
277.8
311.5
301.0 。
实验后装置总质量/g
177.2
279.6
312.6
301.0
若装置D中的氧化铜全部被还原成铜,则气球中收集到的由D中反应产生的气体在标准状况下的体积为L,此条件下,装置D中发生反应的化学方程式为。
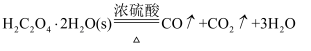 制取并得到纯净干燥的CO气体,合适的组合装置是( )
制取并得到纯净干燥的CO气体,合适的组合装置是( ) 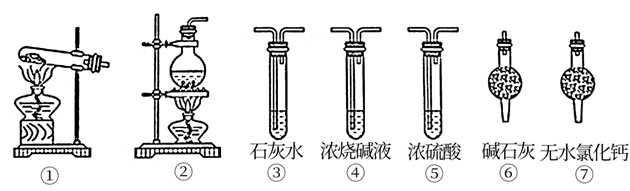
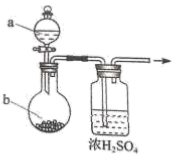
| 选项 | 气体 | a | b |
| A | | 稀 | |
| B | | | |
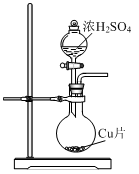
| C | | 浓 | 铁片 |
| D | | 浓氨水 | |
 还原
还原 的实验(部分夹持装置略)。
的实验(部分夹持装置略)。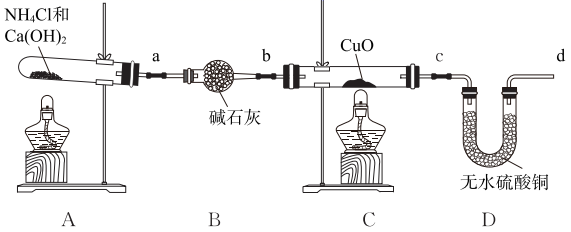
回答下列问题:
-
(1) 连接装置后,填装药品前应进行的操作为。
-
(2) 实验过程中应先点燃(填“A”或“C”)处酒精灯。
-
(3) A中制氨气的化学方程式是。
-
(4) 装置B的名称为。
-
(5) 指导老师认为实验装置存在缺陷,需要增加一个装置进行改进,请指出需要改进的位置(选填“a”“b”“c”或“d”),并在方框中画出改进装置及所用试剂。

-
(6) 证明氨气能还原氧化铜的现象为。


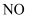

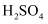
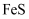

 溶液
溶液