常见金属的活动性顺序及其应用 知识点题库
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知(1)a、c均能与稀硫酸反应产生氢气;(2)b和d的硝酸盐反应,置换出d单质;(3)c与强碱溶液反应放出气体;(4)c、e在冷浓硝酸中发生钝化。由此可判断a、b、c、d、e依次是( )
A . Fe、Cu、Al、Ag、Mg
B . Mg、Cu、Al、Ag、Fe
C . Al、Cu、Ag、Mg、Fe
D . Mg、Ag、Al、Cu、Fe
金属材料在人类社会的发展史上一直发挥着重要的作用。人类历史上使用最早的金属( )
A . 铜
B . 铁
C . 铝
D . 钛
有甲、乙、丙、丁四种金属.将甲、乙用导线相连放入稀H2SO4中可以看到乙慢慢地溶解,而甲的表面有气体逸出.把丁放到乙的硝酸盐溶液中后,丁的表面覆盖一层乙的单质.用石墨电极电解含相同物质的量浓度的甲和丙两种金属的盐溶液,丙的单质先析出.将甲放入稀盐酸中有H2析出.已知四种金属中有一种是铜.根据以上实验判断铜是( )
A . 甲
B . 乙
C . 丙
D . 丁
对四种金属G、L、M、R进行如下实验:
实验 金属 | G | L | M | R |
和冷水反应 | 无反应 | 慢慢反应 | 未做 | 未做 |
和2mol/L HCl 反应 | 溶解并放出气体 | 溶解并放出气体 | 无反应 | 无反应 |
和Rn+的水溶液反应 | 溶解并形成沉淀 | 未做 | 溶解并形成沉淀 | 未做 |
根据表中所给实验结果,判断这四种金属活动性由强到弱的次序正确的是( )
A . L、G、R、M
B . G、L、M、R
C . L、G、M、R
D . L、R、G、M
A、B、C都是金属,B中混有C时,只有C能被盐酸溶解;A与B组成原电池时,A为正极.则A、B、C三种金属的活动性顺序为( )
A . A>B>C
B . A>C>B
C . C>B>A
D . B>C>A
在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是( )
A . 滤液中一定有Fe(NO3)3
B . 滤渣只含Ag和Cu,一定无Zn
C . 滤渣中一定有Ag、Cu和Fe,一定无Zn
D . 滤渣中可能有Ag、Cu、Fe和Zn
硬铝的组成金属有铝、镁、铜、锰.已知:锰丝放入稀硫酸中,有气泡产生;锰丝放入硫酸铝溶液中,表面没有金属析出.下列有关金属的活动性强弱判断错误的是( )
A . Mn>Cu
B . Al>Mn
C . Mg>Al
D . Mn>Mg
地壳中含量最多的金属元素和非金属元素组成的化合物的化学式是( )
A . CuO
B . Al2O3
C . Fe2O3
D . SiO2
有下列原料:①海水 ②石灰石 ③赤铁矿 ④铝土矿 ⑤焦炭 ⑥氧化汞
工业冶炼用 方法制Al,其原料主要是(填序号)。
工业冶炼用方法制Fe,其原料主要是(填序号)。
工业冶炼用方法制Hg,其原料主要是(填序号)。
工业冶炼用 方法制Al,其原料主要是(填序号)。
工业冶炼用方法制Fe,其原料主要是(填序号)。
工业冶炼用方法制Hg,其原料主要是(填序号)。
某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
-
(1) 称取样品a g(精确到0.1 g),称量时通常使用的主要仪器的名称是。
-
(2) 将样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为,溶解、过滤用到的玻璃仪器是。
-
(3) 向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是、。
-
(4) 将步骤(3)中所得的溶液通入过量的CO2,过滤后所得滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。写出灼烧滤渣的化学方程式是,原样品中铝的质量分数是。
下表中给出了四个实验装置和对应的部分实验现象,其中a、b、c、d为金属电极,由此可判断四种金属的活动性顺序是( )
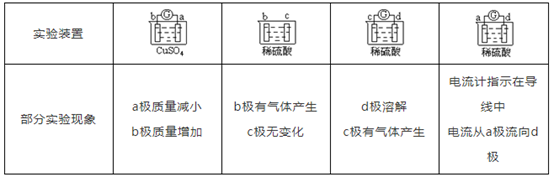
A . d>a>b>c
B . b>c>d>a
C . a>b>c>d
D . a>b>d>c
下列“实验方案”不宜用于完成“实验目的”的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 确认Fe(OH)3胶体是否制备成功 | 用可见光束照射 |
| B | 确认金属活泼性:Na>Cu | 将金属钠投入CuSO4溶液中 |
| C | 确认钠与水反应生成NaOH | 向反应后的混合液中滴加酚酞 |
| D | 确认Cl2无漂白作用 | 将有色纸条放入干燥Cl2中 |
A . A
B . B
C . C
D . D
下列关于钠的用途的叙述中,错误的是( )
A . 钠可用于制造高压钠灯
B . 钠可用于制造过氧化钠等化合物
C . 钠和钾组成的合金可作为原子反应堆的导热剂
D . 钠可将钛、锆、铌、钽等金属从它们的盐溶液中置换出来
有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B为正极;将A、D分别投入等浓度盐酸中,D比A反应剧烈;将铜浸入B的盐溶液里,无明显变化;如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是( )
A . D>A>B>C
B . D>C>A>B
C . B>A>D>C
D . A>B>C>D
下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
A . A原子最外层电子数比B原子的最外层电子数少
B . A原子电子层数比B原子的电子层数多
C . 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多
D . 常温时,A能从酸中置换出氢,而B不能
国产航母山东舰已经列装服役,它是采用模块制造然后焊接组装而成的,对焊接有着极高的要求。实验室模拟在海水环境和河水环境下对焊接金属材料使用的影响(如图)。下列相关描述中正确的是( )
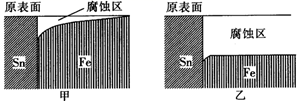
A . 由图示的金属腐蚀情况说明了Sn元素的金属性强于Fe元素
B . 由图示可以看出甲是海水环境下的腐蚀情况,乙是河水环境下的腐蚀情况
C . 两种环境下铁被腐蚀时的电极反应式均为Fe-3e-=Fe3+
D . 为了防止舰艇在海水中被腐蚀,可在焊点附近用锌块打“补丁”
a、b、c三种金属浸入稀硫酸中,a、c相连时,a质量减少;b、c相连,c上有气泡;a、b相连,b为负极。则三种金属的活动性顺序由大到小排列为( )
A . 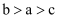 B .
B . 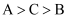 C .
C . 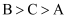 D .
D . 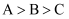
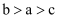 B .
B . 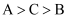 C .
C . 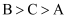 D .
D . 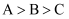
有A、B、C、D四种金属。将A与B用导线连接起来,浸入稀硫酸中,B为正极。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活泼性由强到弱的顺序是( )
A . D>A>B>C
B . B>A>D>C
C . D>B>A>C
D . D>A>C>B
下列实验操作、现象及结论都正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 用铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 该溶液中可能含有 |
| B | 取少量溶液 | 该溶液中含有 |
| C | 取少量金属 | 该白色固体为 |
| D | 将金属 | 说明 |
A . A
B . B
C . C
D . D
下列“实验结论”与“实验操作及现象”不相符的一组是( )
实验操作及现象 | 实验结论 | |
A | 向紫色石蕊溶液中滴加氯水,溶液先变红后褪色 | 氯水具有酸性和漂白性 |
B | 向某溶液中滴加AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
C | 向Al(OH)3沉淀中滴加NaOH溶液,沉淀溶解 | 铝元素表现出一定的非金属性 |
D | 把绿豆大的Na和K分别投入水中,K与水反应更剧烈 | 金属性:Na<K |
A . A
B . B
C . C
D . D
最近更新
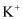
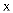 加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的无色无味气体
加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的无色无味气体
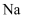 放在坩埚中灼烧,产生白色固体
放在坩埚中灼烧,产生白色固体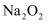
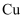 活泼
活泼


