常见金属的活动性顺序及其应用 知识点题库
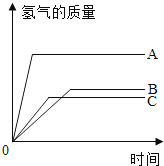
相同质量的三种金属A、B、C和相同质量分数的足量稀硫酸反应,都生成+2价金属硫酸盐,其反应情况如图所示,则三种金属的活动性顺序是 ,它们的相对原子质量大小的顺序是 .
①Y与M用导线连接放入稀硫酸中,M上冒气泡;
②M,N为电极,与N的盐溶液组成原电池,电子从M极流出,经过外电路,流入N极;
③Z+2H2O(冷水)═Z(OH)2+H2↑;
④水溶液中,X+Y2+═X2++Y.
则这五种金属的活动性由强到弱的顺序为( )
①水溶液中X+Y2+═X2++Y;
②Z+2H2O(冷水)═Z(OH)2+H2↑;
③M,N为电极,与N盐溶液组成原电池,M电极反应为M﹣2e﹣═M2+;
④Y可以溶于稀硫酸中,M不被稀硫酸氧化.
则这五种金属的活动性由弱到强的顺序是( )
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小 b极质量增加 | b极有气体产生 c极无变化 | d极溶解 c极有气体产生 | 电流计指示在导线中 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
金属 | 电子流动方向 | 电压/V |
A | A→Fe | +0.76 |
B | Fe→b | ﹣0.18 |
C | C→Fe | +1.32 |
D | D→Fe | +0.28 |
已知构成原电池两电极的金属活动性相差越大,电压表读数越大.则A、B、C、D四种金属中活泼性最强的是( )
①水溶液中:X+Y2+═X2++Y
②Z+2H2O(冷)═Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M﹣2e﹣═M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化.
则这五种金属的活泼性由弱到强的顺序是( )
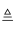 MgO+H2O
D . Ba(OH)2+SO2═BaSO4↓+H2O
MgO+H2O
D . Ba(OH)2+SO2═BaSO4↓+H2O
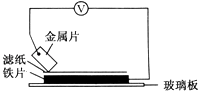
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;
⑤用惰性电极电解含B离子和E离子的溶液,E先析出.
据此,判断五种金属的活动性顺序是( )
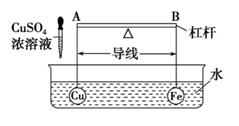

| 选项 | 操作 | 现象 | 结论 |
| A | 将铜粉加入 | 溶液变蓝 | 金属铜比铁活泼 |
| B | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状的炭 | 浓硫酸具有脱水性和强氧化性 |
| C | 向含酚酞的NaOH溶液中通入 | 溶液红色褪去 | |
| D | 某溶液中滴加足量盐酸酸化的 | 生成白色沉淀 | 原溶液中一定有 |
| A | B | C | D | |
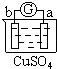
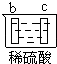
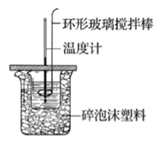
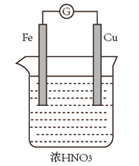
| 装置 | | | | |
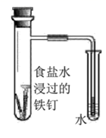
| 实验 | 测定中和热 | 验证铁的活泼性强于铜 | 结合秒表测量 | 验证铁的吸氧腐蚀 |
A.
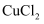 和
和  的混合溶液中加入少量的
的混合溶液中加入少量的 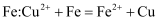 B . 碱性锌锰干电池的正极反应式:
B . 碱性锌锰干电池的正极反应式: 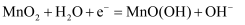 C . 向
C . 向  溶液中加少量
溶液中加少量 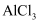 溶液:
溶液: 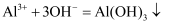 D . 磁性氧化铁溶于浓硝酸:
D . 磁性氧化铁溶于浓硝酸: 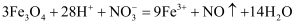


 溶液中
溶液中
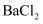 溶液
溶液
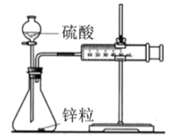
 和硫酸反应的速率
和硫酸反应的速率


