氯气的化学性质 知识点题库
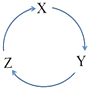
下列各物质中,不能按如图(“→”表示一步完成)关系相互转化的是( )
选项 | X | Y | Z |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A . A
B . B
C . C
D . D
下列化合物中,不能通过单质之间的反应直接制取的是( )
A . Fe3O4
B . FeCl3
C . FeCl2
D . CuCl2
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图1所示的实验装置.

-
(1) 气体发生装置A产生的气体是.
-
(2) 为验证通入D装置中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液;②氯化亚铁溶液;③硫氰化钾溶液;
④苯酚溶液;⑤品红溶液;⑥酸性高锰酸钾溶液.
Ⅰ.若Cl2过量:取适量D中溶液滴加至盛有(填序号)试剂的试管内,再加入(填序号)试剂,实验现象是.
-
(3) Ⅱ.若SO2过量:取适量D中溶液滴加至盛有(填序号)试剂的试管内,实验现象是.
另一小组设计如图2所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.
①若从左端分别通入SO2和Cl2 , 装置A中观察到的现象是否相同?(填“相同”或“不相同”).若装置D装的是铁粉,通入Cl2与铁粉充分反应时现象为.
②若装置B中装有5.0mL 1.0mol/L的碘水,当通入足量Cl2完全反应后,共转移了5.0×10﹣2mol电子,该反应的化学方程式为:.
-
(4) 若由元素S和O组成﹣2价的酸根离子X,X中S和O的质量比为4:3,当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式:.
关于新制的氯水和久置的氯水,下列说法不正确的是( )
A . 新制的氯水呈浅黄绿色,久置的氯水无色
B . 新制的氯水漂白作用强,久置的氯水漂白作用很弱或消失
C . 新制的氯水中没有氯离子,久置的氯水中才含有氯离子
D . 新制的氯水中含氯气多,久置的氯水中含有极少量的氯气或不含氯气
在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列实验现象和结论不一致的是( )
A . 加入有色布条,一会儿有色布条褪色,说明溶液中有HClO存在
B . 溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在
C . 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl﹣存在
D . 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A . Fe
B . Mg
C . Cu
D . Ag
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病暴发的有效方法之一.漂白粉是常用的消毒剂.
-
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式
-
(2) 漂白粉的有效成分是(填化学式).
下列物质中能明显增强漂白粉溶液的漂白能力的是( )
A . 食盐
B . 白醋
C . 小苏打
D . 烧碱
Cl2与NaOH溶液反应,当反应温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法错误的是( )
A . 若产物为NaClO、NaCl,则反应后的溶液中n(ClO-) = n(Cl-)
B . 若产物为NaClO、NaClO3、NaCl,则参加反应NaOH与Cl2物质的量之比一定为2∶1
C . 若产物为NaClO、NaClO3、NaCl,则由反应后溶液中n(Cl-)和n(ClO3-)可计算反应的n(Cl2)
D . 若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
一定量的氢气在氯气中燃烧,所得混合物用100mL质量分数为20%,密度为1.2g/cm3的NaOH溶液吸收,恰好完全吸收,测得溶液中含有NaClO的物质的量为0.1mol。
-
(1) 原NaOH溶液的物质的量浓度为mol/L;
-
(2) 所得溶液中Cl-的物质的量为mol;
-
(3) 原混合气体中氯气和氢气的物质的量之比为。
下列化工生产与该生产过程中使用的一些生产工艺不相符的是( )
A . 氢气和氯气制盐酸——催化和气循环
B . 氢气和氮气合成氨——压缩和水冷却
C . 联合制碱法制纯碱——过滤和热灼烧
D . 二氧化硫接触氧化——催化和热交换
2019年12月以来,我国部分地区突发的新冠病毒肺炎威胁着人们的身体健康。下列有关说法正确的是( )
A . 新型冠状病毒由C,H,O三种元素组成
B . 口罩中间的熔喷布具有核心作用,其主要原料为聚丙烯,属于有机高分子材料
C . 过氧化氢、乙醇、过氧乙酸等消毒液均可以将病毒氧化而达到消毒的目的
D . “84”消毒液(有效成分为NaClO)可以与洁厕灵(主要成分为盐酸)混合使用
下列关于工业生产的说法正确的是( )
A . 工业上利用H2和Cl2的混合气体在光照下反应来制取盐酸
B . 工业上以氯气和澄清石灰水为原料制造漂白粉
C . 工业上将氯气溶于NaOH溶液制备漂白粉
D . 漂白粉要干燥和密封保存
NaClO溶液有杀菌、消毒、漂白作用。某兴趣小组查资料得到Cl2和烧碱在70℃以上主要发生副反应:3Cl2+6NaOH  NaClO3+5NaCl+3H2O,并设计如图制备NaClO溶液的装置:
NaClO3+5NaCl+3H2O,并设计如图制备NaClO溶液的装置:
 NaClO3+5NaCl+3H2O,并设计如图制备NaClO溶液的装置:
NaClO3+5NaCl+3H2O,并设计如图制备NaClO溶液的装置: 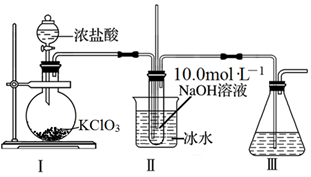
-
(1) 装置Ⅰ中烧瓶内发生反应的化学方程式为。
-
(2) 装置Ⅱ中用冰水浴控制温度的目的是;装置Ⅲ的作用是。
-
(3) 上述装置存在一处缺陷,会导致NaClO产率降低,改进的方法是。
-
(4) 用NaOH固体配制480mL10.0mol·L-1的NaOH溶液时,所需玻璃仪器除量筒、烧杯、胶头滴管外还需要。
-
(5) 配制上述NaOH溶液时,将称量好的NaOH固体g放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容会导致结果(填“偏大”、“不变”或“偏小”)。配制溶液的过程中定容时的操作是。
氯水中存在许多微粒,它们在不同的反应中表现各自的性质,下列实验和结论一致且正确的是( )
A . 加入有色布条,一会儿有色布条褪色,说明氯水中含有Cl2
B . 氯水呈浅黄绿色,且有刺激性气味,说明氯水中含有Cl2
C . 先加入盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明氯水中含有Cl-
D . 加入NaOH溶液,氯水浅黄绿色消失,说明氯水中含有HClO
某兴趣小组设计如图所示的装置进行氯气与金属钠的反应,先将钠预热,在钠熔化成小球时撤去热源,并通入氯气即发生反应(氯气可与KI溶液反应置换出碘单质),下列叙述错误的是( )

A . 钠在氯气中燃烧产生黄色火焰
B . 反应产生的大量白烟是氯化钠固体
C . 棉球①的作用是吸收过量氯气防止产生污染
D . 棉球②变蓝色则证明氯气已被碱完全吸收
已知X中仅含有三种元素,为探究其组成,特进行如下实验。其中,X的水溶液常用来消毒,固体A为厨房中常见物质。A、B均为纯净物。请回答:

-
(1) 物质X的化学式。
-
(2) 请写出物质X受热分解化学方程式。
-
(3) 请写出固体A、固体B在稀硫酸中反应的离子化学方程。
-
(4) 设计实验,验证固体B中的非金属元素。
下列“类比”合理的是( )
A . 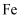 与S反应生成
与S反应生成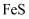 , 则
, 则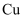 与S反应生成
与S反应生成 B .
B . 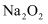 与
与 反应生成
反应生成 和
和 , 则
, 则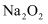 与
与 反应生成
反应生成 和
和 C .
C .  能与
能与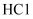 反应生成
反应生成 , 则
, 则 也可以与
也可以与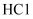 反应生成
反应生成 D .
D . 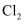 与水反应生成
与水反应生成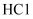 和
和 , 则
, 则 与水反应生成
与水反应生成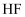 和
和
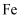 与S反应生成
与S反应生成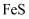 , 则
, 则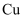 与S反应生成
与S反应生成 B .
B . 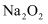 与
与 反应生成
反应生成 和
和 , 则
, 则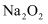 与
与 反应生成
反应生成 和
和 C .
C .  能与
能与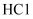 反应生成
反应生成 , 则
, 则 也可以与
也可以与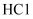 反应生成
反应生成 D .
D . 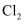 与水反应生成
与水反应生成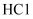 和
和 , 则
, 则 与水反应生成
与水反应生成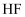 和
和
下列有关常见元素及其化合物的说法正确的是( )
A . 工业上用氯气与澄清石灰水反应制备漂白粉
B . 金属钠具有强还原性,可用金属钠和TiCl4溶液反应制备金属Ti
C . 镁是国防金属,工业上采用电解熔融氧化镁的方法获得镁单质
D . 食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化作用
下列说法错误的是( )
A . 利用丁达尔现象可以鉴别胶体和溶液
B . 利用酚酞鉴别等物质的量浓度的碳酸钠和碳酸氢钠溶液
C . 利用氢气与氯气混合光照制氯化氢气体
D . PM2.5在空气中形成的分散系中可能含有气溶胶
最近更新



