物质检验实验方案的设计 知识点题库
①品红溶液②氯化钙③酸性高锰酸钾④溴水⑤氢硫酸⑥澄清石灰水.
A.稀H2SO4 B.CuCl2 溶液 C.BaCl2 溶液 D.NaOH溶液
-
(1) 若向未知溶液中加入一种试剂后,有沉淀生成,同时溶液由无色变成黄色;则加入的试剂可以是或(选填上述给定试剂的序号A、B、C、D);产生的沉淀可能是或(填化学式).
-
(2) 根据以上实验现象,可以判断溶液中(以下填化学式)一定含有离子,不能确定是否含有离子;而在不能确定的离子中,离子可以通过选用上述给定的试剂和原未知溶液进行试验便能够确定.
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向淀粉的酸性水解液中滴入少量新制Cu(OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B | NaAlO2溶液与NaHCO3溶液混合 | 白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 的△H<0 |
D | 向盛有1mL0.1 mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)sp(AgCl) |

编号 | A | B | C | D |
实 验 方 案 |
|
|
|
|
目 的 | 验证乙炔可与溴发生加成反应 | 验证淀粉水解产物具有还原性 | 验证溴乙烷在氢氧 化钠乙醇溶液中发生消去反应产生乙烯 | 验证碳酸的酸性强于苯酚 |

已知:Ag粉呈黑色,Ag2O呈黑褐色;Ag2O难溶于水,易溶于氨水。
请回答下列问题:
-
(1) 实验(一)探究硝酸银热稳定性。
甲同学设计如图1装置进行实验:
实验步骤及现象:①装置A中AgNO3完全分解后残留有黑色粉末。②用带火星的木条检验集气瓶收集的气体,木条复燃;集气瓶中气体遇空气不变色。③取少量反应后装置C中的溶液于试管,加入铜粉,铜粉不断溶解,产生无色气体,遇空气逐渐变红棕色,溶液变为蓝色。
集气瓶收集的气体是(填化学式,不考虑水蒸气);从水槽中取出集气瓶的操作方法是。
-
(2) 装置C中发生反应的化学方程式为。
-
(3) 实验(二)探究硝酸银分解的固体产物成分。
乙同学对实验(一)残留固体成分提出假设:
假设1:黑色固体是Ag;假设2:黑色固体是Ag2O;假设3:黑色固体是。
-
(4) 丙同学设计实验验证乙同学提出的假设:
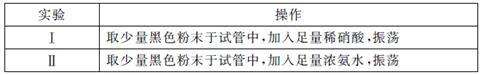
上述方案(填“I”或“II”)能达到实验目的,另一方案不能达到目的,理由是。
-
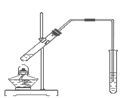
(5) 丁同学设计实验定量探究上述黑色固体组成。
取3.40g黑色粉末按图2装置进行实验,当硬质玻璃管中黑色粉末完全反应后,测得装置E增重0.18g。

①当硬质玻璃管中黑色粉末完全反应后,继续通入一段时间H2的目的是;装置F的作用为。
②根据数据计算,黑色粉末成分为(若为两种物质,计算其物质的量之比;若为一种物质,计算其物质的量)。
 装置:制乙酸乙酯
B .
装置:制乙酸乙酯
B .  装置:验证乙烯气体中混有SO2
C .
装置:验证乙烯气体中混有SO2
C . 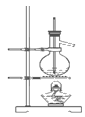 装置:石油的蒸馏
D .
装置:石油的蒸馏
D .  装置:证明石蜡油分解的过程中产生的气体含有烯烃
装置:证明石蜡油分解的过程中产生的气体含有烯烃

| 选项 | 实验操作和现象 | 结论 |
| A | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
| B | 室温下,向 | 镁与盐酸反应放热 |
| C | 室温下,向浓度均为 | 白色沉淀是BaCO3 |
| D | 向 | H2O2具有氧化性 |
| 选项 | 实验事实 | 结论 |
| A | NH3 的水溶液可以导电 | NH3是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | 浓硝酸久置发黄 | 硝酸不稳定 |
| D | 浓硫酸能使蓝色胆矾晶体变成白色 | 浓硫酸具有脱水性 |
| 选项 | 实验操作和实验现象 | 结论 |
| A | 向 | 氧化性: |
| B | 向盛某盐溶液的试管中滴入浓氢氧化钠溶液并加热,试管口处湿润的红色石蕊试纸变蓝 | 该盐中含有 |
| C | 将稀盐酸滴入 | 非金属性: |
| D | 将红热的炭放入浓硫酸中,产生的气体通入澄清石灰水,石灰水变浑浊 | 碳被氧化成 |
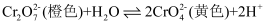 。用K2Cr2O7溶液进行下列实验。下列说法错误的是( )
。用K2Cr2O7溶液进行下列实验。下列说法错误的是( ) 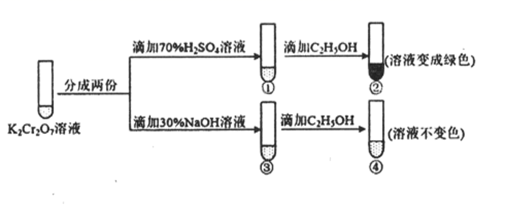
 和
和  浓度相等说明反应达平衡
B . ①中溶液橙色加深,③中溶液变黄
C . ②中
浓度相等说明反应达平衡
B . ①中溶液橙色加深,③中溶液变黄
C . ②中  被C2H5OH还原为Cr3+
D . 若向④中加入70%H2SO4溶液至过量,溶液变为绿色
被C2H5OH还原为Cr3+
D . 若向④中加入70%H2SO4溶液至过量,溶液变为绿色
①尿素热裂解脱氨合成氰尿酸:3CO(NH2)2 3NH3↑+H3(CNO)3(氰尿酸微溶于冷水)
3NH3↑+H3(CNO)3(氰尿酸微溶于冷水)
②碱溶氰尿酸:H3(CNO)3(s)+3NaOH(ag)=Na3(CNO)3(aq)+3H2O(l) ΔH<0

-
(1) 仪器X的支管的作用是。
-
(2) D装置中反应的化学方程式为。
-
(3) 在A装置中“碱溶氰尿酸”后通入Cl2进行“氯化”制得粗产品,该反应的化学方程式为。
-
(4) 使用上述装置制备三氯异氰尿酸,按气体流向从左至右,导管连接顺序为(填字母)。
-
(5) 为了确保产品纯度,A装置中“碱溶氰尿酸”过程中时(填实验现象),停止滴加NaOH溶液。
-
(6) A装置在“氯化”阶段需控制反应温度在10℃-15℃,控制反应温度的实验操作为。
-
(7) 粗产品中Cl3(CNO)3含量测定。将mg粗产品溶于蒸馏水中配制成100mL溶液。取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min后,加入淀粉溶液,用cmol/LNa2S2O3标准溶液进行滴定,滴定至终点消耗vmLNa2S2O3标准溶液。(已知:杂质与KI不反应,涉及的反应为Cl3(CNO)3+6I-+3H+=H3(CNO)3+3I2+3Cl- , I2+2S2O
 =2I-+S4O
=2I-+S4O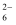 )
)①粗产品中Cl3(CNO)3的百分含量为%(用含m,c,V的代数式表示)。
②下列操作将导致测定结果偏低的是。
A.滴定前滴定管中未排气泡,滴定后气泡消失
B.盛装Na2S2O3标准溶液的滴定管未润洗
C.读数时,滴定前平视,滴定后俯视
D.加入KI溶液的量不足
选项 | 实验操作或实验方案 | 目的 |
A | 用蘸有浓盐酸的玻璃棒靠近输送氨气的管道 | 检验氨气是否泄漏 |
B | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 | 检验 |
C | 用 | 探究浓度对反应速率的影响 |
D | 向盛有某无色溶液的试管中,滴加浓NaOH溶液,在管口放一片湿润的红色石蕊试纸 | 检验 |
选项 | 实验操作和现象 | 结论 |
A | 向溶有SO2的BaCl2溶液中通入X气体,出现白色沉淀 | X气体一定具有强氧化性 |
B | 将石蜡油高温分解产物通入酸性KMnO4溶液,溶液褪色 | 分解产物中一定有乙烯 |
C | AgNO3标准液滴定未知浓度NaCl溶液时,用K2CrO4作指示剂 | Ksp(AgCl)<Ksp(Ag2CrO4) |
D | 常温下,分别测定浓度均为0.1 mol·L-1NaF和NaClO溶液的pH,后者大 | 酸性:HF>HClO |
选项 | 实验操作和现象 | 结论 |
A | 将湿润的蓝色石蕊试纸置于集气瓶口,试纸变红 | 集气瓶内的气体为 NH3 |
B | 常温时向盛有浓硝酸的两支试管中分别投入铜片与铁片后,铜片逐渐溶解而铁片不溶解 | 金属性:Cu > Fe |
C | 向鸡蛋清溶液中加入少量CuSO4 溶液,出现浑浊,分离沉淀后加足量水,沉淀不溶解 | 蛋白质发生了变性 |
D | 向某乙醇试样中加入一小块金属钠,有气泡生成 | 该乙醇中含有一定量的水 |
 和焦亚硫酸钠
和焦亚硫酸钠 可用作食品添加剂。回答下列问题:
可用作食品添加剂。回答下列问题:
-
(1) 实验室用
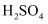 和
和 制取
制取 的化学方程式为。欲净化与收集
的化学方程式为。欲净化与收集 , 选择必要装置,按气流方向连接顺序为(填仪器接口的字母编号)。
, 选择必要装置,按气流方向连接顺序为(填仪器接口的字母编号)。
-
(2) ①焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。已知:
 。
。试剂:稀盐酸、稀
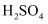 、稀
、稀 、
、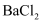 溶液、酸性
溶液、酸性 溶液、
溶液、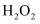 溶液
溶液实验编号
实验步骤
现象
结论
Ⅰ
取少量样品,加入除氧蒸馏水
固体完全溶解得到无色溶液
/
Ⅱ
取实验Ⅰ的溶液,
样品已氧化变质
Ⅲ
另取实验Ⅰ的溶液,加入酸性KMnO4溶液
溶液褪色
样品未完全氧化变质
②
 是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有
是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有 能否用酸性
能否用酸性 溶液检验?作出判断并说明理由。
溶液检验?作出判断并说明理由。 -
(3) 某小组利用下列装置测定空气中
 的含量。
的含量。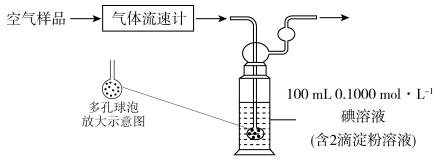
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是;该装置中发生的离子方程式为:。若空气流速为
 , 当观察到时,结束计时,测定耗时t min。假定样品中的
, 当观察到时,结束计时,测定耗时t min。假定样品中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是 。
。
A | B | C | D |
用此装置制备无水MgCl2 | 检验溴乙烷消去产物中的乙烯 | 观察气泡鉴别乙醇与甲醚(CH3OCH3) | 用此装置制备溴苯并验证有HBr产生 |
|
|
|
|
 N2O4
N2O4



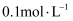 HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升
HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 和
和 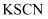 的混合溶液中滴入酸化的
的混合溶液中滴入酸化的  溶液,混合溶液变红
溶液,混合溶液变红

 溶液中,溶液中出现凝胶
溶液中,溶液中出现凝胶

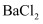 溶液
溶液 固体是否变质
固体是否变质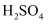 反应,记录出现浑浊的时间
反应,记录出现浑浊的时间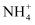 的存在
的存在






