二价铁离子和三价铁离子的检验 知识点题库
I.取5ml 0.1mol/L的KI溶液,滴加5﹣6滴FeCl3稀溶液;
Ⅱ.继续加入2mlCCl4振荡
Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为 .
探究活动Ⅱ的实验现象为
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4﹣反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高.
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
实验操作 | 现象和结论 |
步骤一: | 若产生蓝色沉淀,则 . |
步骤二: | 若乙醚层呈血红色,则 . |
②写出实验操作“步骤一”中的反应离子方程式: .
Ⅳ.为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作:
①移取25.00mLFeCl3稀溶液至锥形瓶中,加入 用作指示剂,再用c mol/LKI标准溶液滴定,达到滴定终点时的现象是 .
②重复滴定三次,平均耗用c mol/LKI标准溶液VmL,则FeCl3稀溶液物质的量浓度为 mol/L.
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 (填“偏高”或“偏低”或“不变”).
绿矾是一种重要的化工原料.
【问题1】绿矾晶体(FeSO4•7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案.可供选择的试剂:KSCN溶液、酸性KMnO4溶液、Cl2水、NaOH溶液、BaCl2溶液请参与完成方案设计.
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
方案1:取少量溶液,加入几滴 试剂,如果观察到的现象是 ;实验结论:证明绿矾样品没有被氧化.
方案2:取少量溶液,加入几滴 试剂,如果观察到的现象是 .
实验结论:证明绿矾样品完全被氧化.
使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 .
【问题2】以绿矾为原料可以制取聚合硫酸铁(SPFS).聚合硫酸铁是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用.其组成可表示成Fex(OH)y(SO4)z•nH2O(其中Fe为+3价).工业上常用的一种制备流程为:

取7.507g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485g,向上述滤液中加入NH3•H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.800g.通过计算确定该固体聚合硫酸铁样品的化学式为 .(写出计算过程)

请回答下列问题:
-
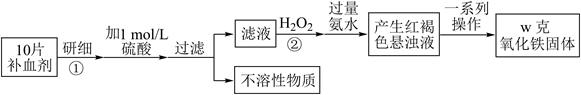
(1) 向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有(填离子符号),检验滤液中还存在Fe2+的方法为(说明试剂、现象)。
-
(2) 步骤②加入过量H2O2的目的是。
-
(3) 步骤③中反应的离子方程式为。
-
(4) 步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量。
-
(5) 假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为g。
-
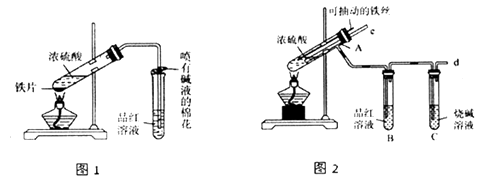
(1) 比较两实验装置,图2装置的优点是:
①能更好地吸收有毒气体SO2 , 防止其污染环境;②。
-
(2) 导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻值SO2 气体逸出而防止污染环境;二是。
-
(3) 能说明有SO2气体产生的实验现象是。
-
(4) 反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有 以下三种可能:
I:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A 稀HCl溶液 B 稀硫酸 C KSCN溶液 D KMnO4溶液
E NaOH溶液 F 淀粉KI溶液 G H2O2溶液
验证Ⅱ:取试样,先滴加少量的(填试剂序号,下同),振荡,再滴加少量的,根据溶液颜色的变化可确定假设Ⅱ是否正确。
验证Ⅲ:步骤1.取试样,滴加少量的(填试剂序号,溶液的颜色变色,则试样中含有Fe3+ , 发生反应的离子方程式为;
步骤2.再取适量的试样,滴加少量的(填试剂序号),溶液颜色的变化为,则试样中含有Fe2+。
| 选项 | 实验 | 现象 | 结论 |
| A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
| B | 将SO2气体通入到Ba(NO3)2溶液中 | 生成白色沉淀 | 此沉淀是BaSO3 |
| C | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| D | 燃烧的钠粒放入CO2中 | 燃烧且有白色和黑色颗粒产生 | 黑色颗粒是炭,白色颗粒可能是Na2CO3 |


-
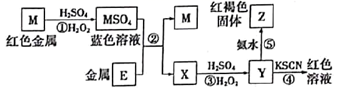
(1) 滤液A中铁元素的存在形式为(填离子符号),生成该离子的离子方程式为,检验滤液A中存在该离子的试剂为(填试剂名称)。
-
(2) 金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为,在实验室中完成此实验还需要的试剂是。
a.KClO3 b.KCl c.Mg d.MnO2
-
(3) 为使固体混合物D在空气中灼烧完全分解,应,直至连续两次测定的实验结果相同(或质量相差小于0.1 g)时为止;灼烧时必须用到的实验仪器是。
-
(4) 溶液G与固体混合物B反应的离子方程式为。
-
(5) 将Na2CO3溶液滴入到一定量的CuCl2溶液中,得到氯化钠、二氧化碳和一种绿色的不溶于水的盐(不含结晶水),该盐受热分解产生三种氧化物,则该盐的化学式是。
-
(1) 厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈(填字母代号)。
a.浅蓝色 b.浅红色 c.浅绿色
-
(2) 检验某补铁剂中的Fe2+是否被氧化成Fe3+ , 可用溶液(填字母代号)。
a.NaOH b.H2O2 c.KSCN
-
(3) 电解氧化铝时加入冰晶石的作用为。
-
(4) 完成乙醇发生催化氧化的化学方程式:2CH3CH2OH+O2
 。
。
-
(5) 常见的酸性锌锰电池的负极材料为Zn,请写出负极的电极反应式:。
-
(6) 铝热反应是工业上常用的反应之一,请写出Al与Fe3O4发生铝热反应的化学方程式:。
选项 | 实验操作 | 现象 | 结论 |
A | 分别加热Na2CO3和 NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
B | 向稀的苯酚水溶液中滴加饱和溴水 | 生成白色沉淀 | 产物三溴苯酚不溶于水 |
C | 向含I-的无色溶液中滴加少量新氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 还原性性:Cl->I- |
D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+即有氧化性又有还原性 |
(初步探究)室温下进行下表所列实验。
|
序号 |
操作 |
现象 |
|
实验Ⅰ |
取5mL 0.1mol/L KI溶液,滴加0.1mol/L FeCl3溶液5∼6滴(混合溶液pH=5) |
溶液变为棕黄色 |
|
实验Ⅱ |
取2mL实验Ⅰ反应后的溶液,滴加2滴0.1mol⋅L−1 KSCN溶液 |
溶液呈红色 |
-
(1) 证明实验Ⅰ中有Fe2+ 生成,加入的试剂为。
-
(2) 写出实验Ⅰ反应的离子方程式:。
-
(3) 上述实验现象可以证明Fe3+与I−发生可逆反应,实验Ⅰ在用量上的用意是
-
(4) 在实验I的溶液中加入CCl4 , 实验现象是,取其上层清液中滴加KSCN溶液,并未看到明显的红色,其原因为(从平衡移动的角度解释)。
(深入探究)20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
-
(5) 已知在酸性较强的条件下,I−可被空气氧化为I2 , 故甲同学提出假设:该反应条件下空气将I−氧化为I2 , 使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:,20min内溶液不变蓝,证明该假设不成立,导致溶液不变蓝的因素可能是。
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向NaCl、NaI的混合稀溶液中滴入少量稀 AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| B | 室温下,向溶液X中滴加少量双氧水,再加入KSCN溶液,变红 | 溶液X中一定含Fe2+ |
| C | 用洁净铂丝蘸取溶液Y在火焰上灼烧,火焰呈黄色溶液 | Y中含 Na+不含K+ |
| D | 室温测定浓度均为0.1mol·L-1的CH3COONa溶液和NaNO2溶液的pH, CH3COONa 溶液的pH大 | HNO2 电离出H+的能力比CH3COOH强 |
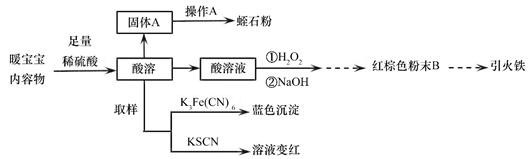
(实验方案)
(实验装置)(制引火铁)
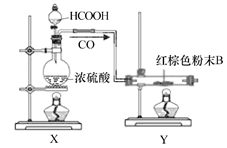
回答下列问题:
-
(1) 在“暖宝宝”的使用过程中,蛭石粉的作用是。影响“暖宝宝”发热的持续时间和温度的主要因素是。
-
(2) “实验方案”中“操作A”的具体内容为。
-
(3) 有关使用后的“暖宝宝”中铁元素的存在形式,下列说法正确的是_______。A . 一定含有Fe、Fe2+、Fe3+ B . 一定含Fe3+ C . 一定含有Fe2+、Fe3+ D . 可能含Fe
-
(4) 制引火铁的“实验装置”中有两处明显的缺陷,分别是和。
-
(5) 制取CO时,浓硫酸的作用是。实验开始时,应先点燃(填“X”或“Y”)处酒精灯。
-
(6) “引火铁”在空气中能自燃的原因是。
下列说法错误的是( )
-
(1) 工业上常用FeCl3作印刷电路板的蚀刻剂。某实验小组欲从印刷电路板的废液中回收铜,并获得FeCl3溶液,设计了如下方案:

①试剂D为(填名称)。
②滤液B的溶质为(填化学式)。
③通入气体F时发生反应的离子方程式为。
④工业上制作印刷电路板的原理为(用离子方程式表示)。
-
(2) 水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O
 +O2+xOH-=Fe3O4↓+S4O
+O2+xOH-=Fe3O4↓+S4O 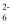 +2H2O。请回答下列问题:
+2H2O。请回答下列问题: ①水热法制备Fe3O4纳米颗粒的反应中,被氧化的元素为(填元素符号)。
②该反应的化学方程式中x=。
③每生成1 mol Fe3O4 , 反应转移的电子为mol。
 晶体。具体的流程如下:
晶体。具体的流程如下: 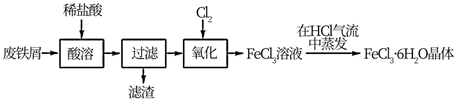
试回答下列问题:
-
(1) 请写出“酸溶”时发生反应的离子方程式:
 、 。
、 。
-
(2) 过滤时,需要用到的玻璃仪器有。
-
(3) “氧化”过程中发生反应的化学方程式为,该反应中氧化剂是。
-
(4) 蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是。
-
(5) “氧化”过程结束后,如何证明溶液中有Fe3+存在?请写出实验方案:。
 (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 , 含少量
, 含少量 、
、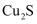 、
、 等杂质)为原料制备铋酸钠的流程如下:
等杂质)为原料制备铋酸钠的流程如下: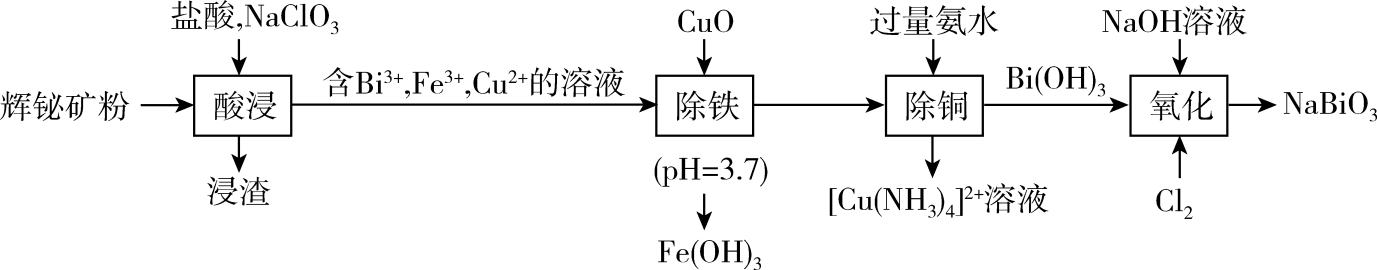
请回答下列问题:
-
(1) “浸渣”的主要成分是(填化学式)。用硝酸替代“盐酸,
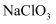 ”也可以实现“酸浸”,从环保角度考虑,存在的缺点是。
”也可以实现“酸浸”,从环保角度考虑,存在的缺点是。
-
(2) 检验“酸浸”液中是否含
 , 可选择的试剂是____(填标号)。
A . KSCN溶液 B .
, 可选择的试剂是____(填标号)。
A . KSCN溶液 B .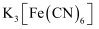 溶液
C . KSCN溶液和双氧水
溶液
C . KSCN溶液和双氧水
-
(3) “除铁”的离子方程式为。
-
(4) 已知
 ,
, 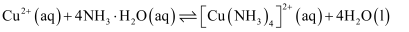 的平衡常数
的平衡常数 。
。 的平衡常数
的平衡常数 。
。
-
(5) 探究
 的性质:
的性质:实验
操作
现象
Ⅰ
取少量
 粉末于试管中,加入浓盐酸,振荡;用镊子夹一块湿润的淀粉KI试纸放置在试管口上方
粉末于试管中,加入浓盐酸,振荡;用镊子夹一块湿润的淀粉KI试纸放置在试管口上方浅黄色固体溶解,产生黄绿色气体,试纸变蓝
Ⅱ
在稀硫酸酸化的
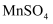 溶液中加入
溶液中加入 粉末,振荡
粉末,振荡无色溶液变紫红色溶液
①实验Ⅱ中发生反应的离子方程式为。
②结合上述实验及所学知识,在酸性条件下,
 、
、 、
、 的氧化性由强到弱的顺序是。(填化学式)。
的氧化性由强到弱的顺序是。(填化学式)。③结合上述流程中“氧化”步骤中发生的反应,说明
 和
和 的氧化性相对强弱不一致的主要原因是。
的氧化性相对强弱不一致的主要原因是。
 表示
表示



