溶液pH的定义 知识点
溶液PH的定义:是用溶液中的氢离子的浓度大小表示溶液的酸碱性,PH=-lgC(H+),PH越小表示溶液酸性越强,氢离子的浓度越大。
溶液pH的定义 知识点题库
正常情况下,人体血液的pH的范围是( )
A . 8.67~9.26
B . 7.35~7.45
C . 7.00
D . 大于5.70
25℃的下列溶液中,碱性最强的是( )
A . pH=11的溶液
B . c(OH﹣)=0.12 mol/L的溶液
C . 1L中含有4g NaOH的溶液
D . c(H+)=1×10﹣10mol/L的溶液
在下列的各种叙述中,正确的是( )
A . 在任何条件下,纯水的pH=7
B . 在任何条件下,纯水都呈中性
C . 在100℃时,纯水的pH>7
D . 在100℃时,纯水中c(H+)<10﹣7mol/L
下列溶液肯定是酸性的是( )
A . 含H+的溶液
B . 能使酚酞显无色的溶液
C . pH<7的溶液
D . c(OH﹣)<c(H+)的溶液
物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
A . Ba(OH)2、Na2SO3、FeCl3、KCl
B . Na2SiO3、Na2CO3、KNO3、NH4Cl
C . NH3•H2O,H3PO4、Na2SO4、H2SO4
D . NaHCO3、H2SO4、C2H5OH,HCl
为了研究土壤的酸碱性,某学生做了如下实验:将一定体积的蒸馏水加入一定质量的土壤中,充分搅拌后,过滤并留取滤液,测滤液的pH后向滤液中滴加氨水,每加入2mL氨水就搅拌均匀并测量溶液的pH,所得实验记录如下:
加氨水体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液的pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
利用上述记录的数据,以加入的氨水体积为横坐标、pH为纵坐标绘制曲线图,并根据曲线图回答下列问题:
-
(1) 所测土壤的酸碱性如何?
-
(2) 所用氨水的pH和c(OH﹣)分别为多少?
-
(3) 为使该滤液呈中性,所加入氨水的恰当体积是多少?
已知在100℃,水的离子积Kw=1×10﹣12 , 本题涉及的溶液温度均为100℃.下列说法中正确的是( )
A . 0.005 mol/L的H2SO4溶液,pH=2
B . 0.001 mol/L的NaOH溶液,pH=11
C . 0.005 mol/L的H2SO4溶液与0.01 mol/L的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性
D . 完全中和pH=3的H2SO4溶液50 mL,需要pH=9的NaOH溶液100 mL
pH相同的盐酸和醋酸两种溶液,它们的( )
A . H+的物质的量相同
B . 物质的量浓度相同
C . H+的物质的量浓度不同
D . H+的物质的量浓度相同
物质的量浓度相同的下列溶液中.符合按pH由小到大顺序排列的是( )
A . HCl、 NH4Cl 、CH3COOH、 NaNO3 、Na2CO3 、NaHCO3 、NaOH
B . HCl 、NH4Cl 、CH3COOH、NaHCO3 、NaNO3 、Na2CO3 、 NaOH
C . HCl 、CH3COOH 、 NH4Cl 、 NaNO3 、NaHCO3 、Na2CO3、 NaOH
D . HCl 、CH3COOH 、 NH4Cl 、 NaNO3 、Na2CO3 、NaHCO3 、NaOH
下列酸溶液的pH相同时,其物质的量浓度最小的是( )
A . H2SO4
B . H2SO3
C . CH3COOH
D . HNO3
物质的量浓度相同的下列物质的水溶液,酸性最强的是( )
A . HCl
B . H2SO4
C . CH3COOH
D . NaCl
将浓度均为0.1mol∙L-1的下列溶液稀释10倍,其中pH增大的是( )
A . HNO3
B . NaOH
C . KI
D . NaHCO3
室温下,pH=4的盐酸和pH=10的氨水等体积混合后,所得溶液的pH值( )
A . 一定小于7
B . 一定等于7
C . 一定大于7
D . 无法判断
已知常温时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误的是( )
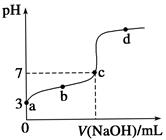
A . a点表示的溶液中c(CH3COO-)略小于10-3 mol·L-1
B . b点表示的溶液中c(CH3COO-)>c(Na+)
C . c点表示CH3COOH和NaOH恰好反应完全
D . b、d点表示的溶液中  均等于K
均等于K
 均等于K
均等于K
pH值相等的盐酸(甲)和醋酸(乙),盐酸与醋酸浓度的大小关系是( )
A . 甲=乙
B . 甲>乙
C . 甲<乙
D . 不确定
常温下,向20 mL 0.1mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述错误的是( )
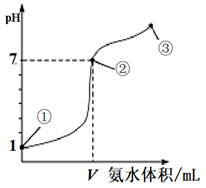
A . V>20 mL
B . ①、②、③点水的电离程度大小为:②>③>①
C . 在点②所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH 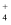 )
D . 在点②、③之间可能存在:c(NH
)
D . 在点②、③之间可能存在:c(NH 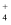 )>c(Cl-)=c(OH-)>c(H+)
)>c(Cl-)=c(OH-)>c(H+)
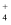 )
D . 在点②、③之间可能存在:c(NH
)
D . 在点②、③之间可能存在:c(NH 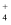 )>c(Cl-)=c(OH-)>c(H+)
)>c(Cl-)=c(OH-)>c(H+)
为更合理地表示溶液的酸碱性,科学家提出“酸度”(用AG表示)概念,AG=lg[c(H+)/c(OH-)].下列叙述中正确的是( )
①任何温度下,纯水的AG等于0; ②溶液的AG越小,酸性越强;
③常温下,0.1mol/L盐酸的AG=12; ④25℃时,某溶液的AG=-10,其pH=10.
A . ①③
B . ②④
C . ①②
D . ③④
为验证氯水中次氯酸光照分解产物,采用数字化实验,得到的数据图像如图。该图像所代表的意义是( )
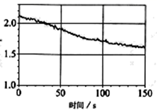
A . 氯离子浓度随时间的变化
B . 氧气体积分数随时间的变化
C . 氯水的pH随时间的变化
D . 氯水导电能力随时间的变化
现有室温下三种溶液:①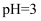 的稀盐酸 ②
的稀盐酸 ②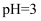 的
的 溶液 ③
溶液 ③ 的氨水。相同条件下,下列说法正确的是( )
的氨水。相同条件下,下列说法正确的是( )
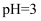 的稀盐酸 ②
的稀盐酸 ②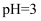 的
的 溶液 ③
溶液 ③ 的氨水。相同条件下,下列说法正确的是( )
的氨水。相同条件下,下列说法正确的是( )A | ①、②分别加入同样的锌粒 | 开始时,反应速率:①>② |
B | ①、②分别加水稀释10倍后 | pH:①<② |
C | ①、③中水的电离程度 | ①<③ |
D | ①、③溶液等体积混合后 |
|
A . A
B . B
C . C
D . D
相同温度下,等物质的量浓度的下列溶液中,pH最小的是( )
A .  B .
B .  C .
C .  D .
D . 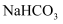
 B .
B .  C .
C .  D .
D . 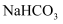
最近更新