中和滴定 知识点题库
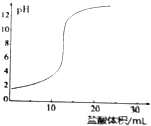 用盐酸滴定NaOH溶液的滴定曲线如图所示
用盐酸滴定NaOH溶液的滴定曲线如图所示
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
指示剂 | 变色范围 | 酸色 | 碱色 |
石蕊 | 5.0﹣8.0 | 红色 | 蓝色 |
酚酞 | 8.0﹣10.0 | 无色 | 红色 |
甲基橙 | 3.1﹣4.4 | 红色 | 黄色 |
请完成下列问题:
-
(1) 选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是.(填序号)除以上仪器外还缺的玻璃仪器有、.
-
(2) 正确的操作步骤是(填写字母)→→→→.
-
(3) 滴定管读数应注意.
-
(4) 操作中锥形瓶下垫一张白纸的作用是.
-
(5) 操作D中液面应调整到;
-
(6) 滴定到终点时锥形瓶内溶液的pH约为;终点时的颜色变化是.
-
(7) 若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响(填“偏高”、“偏低”或“无影响”,其他操作均正确).
I.称取xg某油脂,加入含ymol I2的韦氏溶液( 韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用c mol/LNa2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液VmL(滴定反应为:2 Na2S2O3+ I2=Na2S4O6+2NaI)。回答下列问题:
-
(1) 有关滴定的下列说法正确的是________(填标号)。A . 标准Na2S2O3溶液应盛装在碱式滴定管中 B . 滴定时眼睛只要注视滴定管中溶液体积的变化 C . 滴定到溶液由无色变蓝色时应该立即停止滴定 D . 同样的滴定应重复2-3次,取几次滴定所用溶液的平均值计算滴定结果
-
(2) 该油脂的碘值为g(列式表示)。
-
(3) 用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是。
-
(4) II.现要从上述测定碘值实验后的含碘废液中回收碘单质(废液中含有H2O、油脂、I2、I-)。设计如图一所示的实验过程:

为了将含碘废液中的I2完全转化为I-而进入水层,向含碘度液中加入了稍过量的A溶液,则A应该具有性。
-
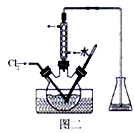
(5) 将操作①所得溶液放入图二所示的三颈烧瓶中,并用盐酸调至pH约为2,再缓慢通入适量Cl2 , 使其在30~40℃反应。反应要控制在30~40℃的原因是;Cl2不能过量,因为过量的Cl2将I2氧化为IO3- , 写出该反应的离子方程式。
-
(6) 操作②包含多步操作,将在三颈烧瓶中反应完全后的溶液经过操作②获得碘单质,在操作②中必须用列下列所示的部分仪器或装置,这些仪器和装置是(填标号)。


已知:H2O2可看作二元弱酸,它的一级电离常数Ka1=1.55×10-12

-
(1) Ⅰ.检测二氧化硫的含量
仪器A的名称是。
-
(2) B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中过量H2O2溶液充分反应,C中发生反应的化学方程式为。
-
(3) 用0.0900 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 (填编号)。向C中所得溶液中滴加几滴酚酞试剂,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为 g·L-1。
-
(4) 该测定结果比实际值偏高,分析原用可能是(任答一条即可),
-
(5) 本实验中所用的H2O2溶液的浓度,常用KMnO4标准溶液进行测定,H2O2可看作二元弱酸,但一般不利用酸碱中和滴定法过行测定的原因任答一条即可)。
-
(6) Ⅱ.分析H2O2的催化分解原理
碱性介质中H2O2分解远比酸性介质中快,NaOH可促使H2O2失去质子,请写出H2O2与NaOH溶液反应生成的酸式盐的电子式。
-
(7) I-催化H2O2分解的原理分为两步,总反应可表示为:
2H2O2(aq)=2H2O(l)+O2(g) △H<0
若第一步反应为 H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应
则第二步反应为△H <0 快反应
-
(8) 能正确的表示I-催化H2O2分解真理的示意图为。


a.取25.00mL未知浓度的HCl溶液放入锥形瓶中;b.此瓶需事先用蒸馏水洗净,并将该瓶用待测液润洗过;c.加入几滴酚酞作指示剂;d.取一支酸式滴定管 , 经蒸馏水洗净;e.直接往其中注入标准NaOH溶液 , 进行滴定;f.一旦发现溶液由无色变成粉红色 , 即停止滴定,记下数据。
-
(1) 制备FeSO4溶液的实验步骤如下:
步骤1.称取4.0g碎铁屑,放入烧杯中,加入10%Na2CO3溶液,煮沸、水洗至中性。
步骤2.向清洗后的碎铁屑中加入3mol/L H2SO4溶液20mL,盖上表面皿,放在水浴中加热。不时向烧杯中滴加少量蒸馏水,控制溶液的pH不大于1。
步骤3.待反应速度明显减慢后,趁热过滤得FeSO4溶液。
①步骤1的实验目的是。
②步骤2“不时向烧杯中滴加少量蒸馏水”的目的是;“控制溶液的pH不大于1”的目的是。
-
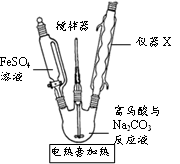
(2) 制取富马酸亚铁的实验步骤及步骤(Ⅱ)的实验装置如下:

①步骤(Ⅰ)所得产品(富马酸)为-丁烯二酸(填“顺”或“反”)。
②富马酸与足量Na2CO3溶液反应的方程式为。
③图中仪器X的名称是,使用该仪器的目的是。
-
(3) 测定(2)产品中铁的质量分数的步骤为:准确称取产品ag, 加入新煮沸过的3mol/LH2SO4溶液15mL,待样品完全溶解后,再加入新煮沸过的冷水50mL和4滴邻二氮菲-亚铁指示剂,立即用cmol/L (NH4)2Ce(SO4)3标准溶液滴定(Ce4++Fe2+=Ce3++Fe3+),滴定到终点时消耗标准液VmL。
①(NH4)2Ce(SO4)3标准溶液适宜盛放在(填“酸式”或“碱式”)滴定管中。
②该实验中能否用KMnO4标准溶液代替(NH4)2Ce(SO4)3标准溶液滴定Fe2+ , 说明理由。
③产品中铁的质量分数为(用含a、V的代数式表示)。
-
(1) 用amol·L-1的HCl滴定未知浓度的NaOH溶液,用酚酞做指示剂,达到滴定终点的现象是。若用甲基橙做指示剂,滴定终点现象是。
-
(2) 用标准碘溶液滴定溶有SO2的水溶液,以测定水中SO2的含量,应选用做指示剂,达到滴定终点的现象是。
-
(3) 用标准酸性KMnO4溶液滴定溶有SO2的水溶液,以测定水中SO2的含量,是否需要选用指示剂(填“是”或“否”),达到滴定终点的现象是。

完成下列填空:
-
(1) 稀释白醋时需要的仪器有烧杯、。
-
(2) 本实验选用酚酞作指示剂。达到滴定终点时,指示剂从色变为色。
-
(3) 某同学一共进行了三次实验,以下是他设计的实验数据记录表,表格中A是,B是。
实验
次数
稀释后白醋
体积(mL)
标准NaOH溶液
A
B
消耗体积(mL)
1
20.00
22.05
2
20.00
21.34
3
20.00
21.30
①数据处理:消耗标准NaOH溶液的体积=mL。
②若测得稀释后白醋的浓度0.0594mol·L-1 , 则该食醋 (选填“符合”或“不符合”)国家标准。
-
(4) 标准NaOH溶液通过以下步骤准备:
①配制500mL浓度约为0.1mol·L-1的NaOH溶液;
②用KHC8H4O4标准溶液准确测定该NaOH溶液的浓度。
称量所需的NaOH固体置于大烧杯中,加入500mL蒸馏水,搅拌溶解,该配制浓度约为0.1mol·L-1NaOH溶液的步骤 (填“可行”或“不可行”)。
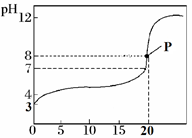

回答下列问题:
-
(1) 该酸为酸(填“强”或者“弱”),你的判断理由是。
-
(2) 点P时溶液中的 c(HA)=mol·L−1。
-
(3) ①该中和滴定应选择做指示剂,滴定终点时的现象是。
指示剂变色范围(pH)
甲基橙(3.1~4.4)
石蕊(5~8)
酚酞(8.2~10.0)
颜色
<3.1
3.1~4.4
>4.4
<5
5~8
>8
<8.2
8.2~10.0
>10.0
红
橙
黄
红
紫
蓝
无色
粉红
红
②滴定起始和终点的液面位置如图2所示,则消耗NaOH溶液的体积为mL。
③下列操作使滴定结果偏高的是。
a.滴定前,碱式滴定管未用NaOH溶液润洗
b.锥形瓶的待测液中加少量水稀释
c.碱式滴定管滴定前有气泡,滴定后无气泡
d.读数时,滴定前仰视,滴定后俯视
 溶液的浓度,甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
溶液的浓度,甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
 溶液的锥形瓶滴定前用
溶液的锥形瓶滴定前用  溶液润洗2~3次
溶液润洗2~3次

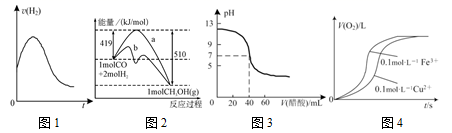
 CH3OH(g)的物质能量与反应过程的变化关系,b曲线可能使用了催化剂
C . 图3表示25 ℃时用0.100 0 mol·L−1醋酸滴定40.00 mL 0.100 0 mol·L−1NaOH溶液得到的滴定曲线
D . 图4表示向2 mL 5%的H2O2溶液中分别滴加0.1 mol·L−1 Fe3+和Cu2+(两溶液的阴离子相同)各1 mL,生成氧气的体积随时间的变化,表明Cu2+能使反应更快
CH3OH(g)的物质能量与反应过程的变化关系,b曲线可能使用了催化剂
C . 图3表示25 ℃时用0.100 0 mol·L−1醋酸滴定40.00 mL 0.100 0 mol·L−1NaOH溶液得到的滴定曲线
D . 图4表示向2 mL 5%的H2O2溶液中分别滴加0.1 mol·L−1 Fe3+和Cu2+(两溶液的阴离子相同)各1 mL,生成氧气的体积随时间的变化,表明Cu2+能使反应更快
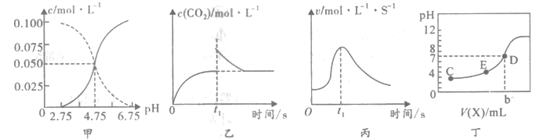
 的醋酸与醋酸钠混合溶液中
的醋酸与醋酸钠混合溶液中  、
、  与pH的关系曲线,
与pH的关系曲线, 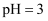 的溶液中:
的溶液中:  B . 图乙是恒温密闭容器中发生
B . 图乙是恒温密闭容器中发生 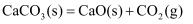 反应时,
反应时,  随反应时间变化的曲线,
随反应时间变化的曲线, 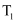 时刻改变的条件可能是缩小容器的体积
C . 图丙是铁条与盐酸反应的反应速率随反应时间变化的曲线,
时刻改变的条件可能是缩小容器的体积
C . 图丙是铁条与盐酸反应的反应速率随反应时间变化的曲线, 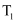 时刻溶液的温度最高
D . 图丁是常温下,用0.10mol/L NaOH溶液滴定
时刻溶液的温度最高
D . 图丁是常温下,用0.10mol/L NaOH溶液滴定 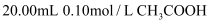 溶液。则酚酞可作本实验的指示剂,D点为滴定终点
溶液。则酚酞可作本实验的指示剂,D点为滴定终点
-
(1) I.醋酸是一种常见的弱酸,回答下列问题:
下列措施可以使醋酸溶液中CH3COOH电离程度增大的是_______(填字母序号)。A . 升温 B . 通入HCl气体 C . 加入NaOH固体 D . 加入NaHSO4固体I.醋酸是一种常见的弱酸,回答下列问题:下列措施可以使醋酸溶液中CH3COOH电离程度增大的是(填字母序号)。
-
(2) 用0.1 mol∙L−1NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol∙L−1的盐酸和醋酸溶液,滴定过程中溶液pH随加入NaOH溶液体积变化的曲线如图。请回答:

滴定盐酸的曲线是(填“I”或“II”);M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是。
-
(3) II.国家标准规定葡萄酒中SO2的最大含量为0.25g∙L−1。某兴趣小组用图1所示装置(夹持装置已略去)收集某葡萄酒中的SO2 , 然后对其含量进行测定。
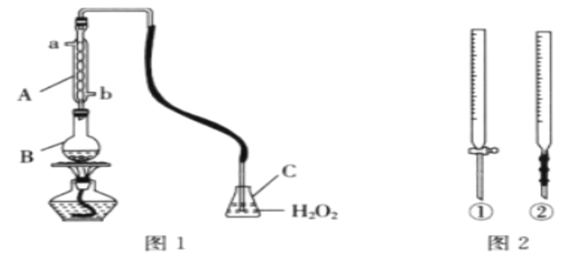
向B中加入300.00mL葡萄酒和适量稀硫酸,加热使SO2全部逸出,并与C中H2O2完全反应,C中反应的离子方程式为。
-
(4) 除去C中剩余的H2O2 , 然后用0.0900 mol∙L−1的NaOH标准溶液进行滴定,NaOH标准溶液应盛装在图2中的(填“①”或“②”)中;如用酚酞作指示剂,则滴定终点的现象B为。
-
(5) 滴定测得,消耗NaOH标准溶液25.00mL,则该葡萄酒中SO2的含量为g·L-1。
 的盐酸分别滴定20.00ml,浓度均为
的盐酸分别滴定20.00ml,浓度均为 三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
 B . 该NaX溶液中:
B . 该NaX溶液中: C . 分别滴加20.00mL盐酸后,再将三种溶液混合:
C . 分别滴加20.00mL盐酸后,再将三种溶液混合: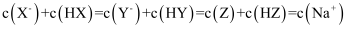 D . 当
D . 当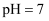 时,三种溶液中:
时,三种溶液中: 、
、 和
和 都小于
都小于
-
(1) 工业上通过电解饱和食盐水制备氯气,阳极反应历程如下:Cl--e-=Cl•,
 →Cl2。阳极反应历程可描述为:,阳极电极反应式是。
→Cl2。阳极反应历程可描述为:,阳极电极反应式是。
-
(2) 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示,此过程中腐蚀电池的负极是,正极反应式是。

-
(3) 工业膜电解法制得的焦亚硫酸钠(Na2S2O5)会含有杂质(杂质不与高锰酸钾反应),取某Na2S2O5产品10.0g配成100mL溶液,取10.00mL加入过量20.00mL0.3000mol•L-1酸性高锰酸钾溶液,充分反应后,用0.2500mol•L-1的Na2SO3标准液滴定至终点,消耗Na2SO3溶液20.00mL。
已知:5S2O
 +4MnO
+4MnO +2H+=4Mn2++10SO
+2H+=4Mn2++10SO +H2O
+H2O5SO
 +2MnO
+2MnO +6H+=2Mn2++5SO
+6H+=2Mn2++5SO +3H2O
+3H2O①判断滴定终点的依据为。
②计算Na2S2O5样品的纯度,写出计算过程。



