反应热和焓变 知识点题库

 2H2+O2
D . 每产生氢气44.8L,转移电子数目为4NA
2H2+O2
D . 每产生氢气44.8L,转移电子数目为4NA
-
(1) 某制革厂含硫废水中主要含有物是Na2S.
①测得该废水溶液pH=12,用离子方程式解释溶液呈碱性的原因.
②含硫废水的处理过程中可以采用纯氧将Na2S转化为Na2SO4 , 则反应中还原剂与氧化剂的物质的量之比为.已知1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s)+4H2(g)⇌Na2S(s)+4H2O(g),已知该反应的平衡常数K1000℃<K1400℃ , 则该反应的△H0(填“>”“=”或“<”).
-
(2) 含硫燃料中间体废水中主要含有物为Na2SO3 , 回收废水中的硫化物,以减少资源的浪费,可采用以下方法:

①中和含酸废水工业常用的试剂x是.
②写出H2S气体与足量NaOH溶液反应的化学方程式.
③铁屑与石墨能形成微型原电池,SO32﹣在酸性条件下放电生成H2S进入气相从而达到从废水中除去Na2SO3的目的,写出SO32﹣在酸性条件下放电生成H2S的电极反应式:.
④已知:2H2S(g)+O2(g)═2S(s)+2H2O(l)△H=﹣632.8kJ/mol
SO2(g)═S(s)+O2(g)△H=+269.8kJ/mol
H2S与O2反应生成SO2和H2O的热化学方程式为.
回答下列问题:
-
(1) 科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应N2(g)+3H2(g)
 2NH3(g)的∆H=kJ∙mol-1。该历程中速率最快的一步的活化能(E)为 kJ∙mol-1。
2NH3(g)的∆H=kJ∙mol-1。该历程中速率最快的一步的活化能(E)为 kJ∙mol-1。 -
(2) 工业合成氨反应为:N2(g)+3H2(g)
 2NH3(g),当进料体积比V(N2)∶V(H2)=1∶3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2)∶V(H2)=1∶3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:

①500℃时,反应的平衡常数Kp(100MPa) Kp(30MPa)。(填“<”、“=”、“>”)
②500℃、30MPa时,氢气的平衡转化率为(保留3位有效数字),Kp=(MPa)-2(列出计算式)。
[Kp为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
-
(3) 科学家利用电解法在常温常压下合成氨,工作时阴极区的微观示意图如图,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。

①阴极区生成NH3的电极反应式为。
②下列说法正确的是(填标号)。
A.该装置用金(Au)作催化剂,目的是降低N2的键能
B.三氟甲磺酸锂的作用是增强导电性
C.选择性透过膜可允许N2和NH3通过,防止H2O进入装置


-
(1) 若t1=15 min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=。
-
(2) t4~t5阶段改变的条件为,B的起始物质的量为。各阶段平衡时对应的平衡常数如表所示:
t1~t2
t2~t3
t3~t4
t4~t5
t5~t6
K1
K2
K3
K4
K5
则K1=(计算式),K1、K2、K3、K4、K5之间的关系为(用“>”“<”或“=”连接)。
-
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式:2A(g) + B(g)⇌3C(g) ΔH,用含有a的代数式表达 ΔH = 。
-
(4) 在相同条件下,若起始时容器中加入4mol A、2 mol B和1.2 mol C,达到平衡时,体系中 C的百分含量比t1时刻C的百分含量(填“大于”“小于”“等于”)。
-
(5) 能说明该反应已达到平衡状态的是。
a.v(A)=2v(B) b.容器内压强保持不变
c.2v逆(c)=3v正(A) d.容器内密度保持不变
-
(6) 为使该反应的反应速率增大,且平衡向正反应方向移动的是。
a.及时分离出C气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂


 ,
,  B . 熵变
B . 熵变  ,
,  C . 焓
C . 焓  (s,石墨),
(s,石墨),  (s,金刚石)
D . 焓变
(s,金刚石)
D . 焓变  ,
, 
 。请回答下列问题:
。请回答下列问题:
-
(1) 煤是一种(填“可”或“不可”)再生能源,写出直接用煤作燃料可能带来的环境问题:(填两条即可)。
-
(2) 某些共价键的键能如下表:
化学键
C-O
C-H
H-H
C=O
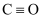
E/(kJ/mol)
358
413
436
799
1072
该反应的
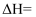 。
。 -
(3) 向容积为1L的恒容密闭容器中,充入
 和
和 , 在t℃下发生反应,实验测得
, 在t℃下发生反应,实验测得 的物质的量(n)随时间变化的曲线如图1所示。
的物质的量(n)随时间变化的曲线如图1所示。
①
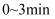 内,反应速率
内,反应速率
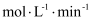 。达到平衡时,压强为0.8MPa,Kp为用平衡分压代替平衡浓度表示的平衡常数(分压=总压×物质的量分数),则该温度下的平衡常数Kp为
。达到平衡时,压强为0.8MPa,Kp为用平衡分压代替平衡浓度表示的平衡常数(分压=总压×物质的量分数),则该温度下的平衡常数Kp为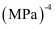 。
。②下列说法能判断该反应达到平衡状态的是(填标号)
A.单位时间内断裂
 的同时断裂
的同时断裂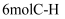 B.
B.
C.3v正(CO)=v逆(CO2) D.混合气体的密度不再变化
-
(4) 恒压条件下,H2的平衡转化率与起始投料比
 、温度的变化关系如图2所示,则三条曲线对应温度最高的是。测得B点CO的转化率为30%,则x1=。
、温度的变化关系如图2所示,则三条曲线对应温度最高的是。测得B点CO的转化率为30%,则x1=。
 CO(g)+H2O(g),其化学平衡常数(K)与温度(T)的关系如表:
CO(g)+H2O(g),其化学平衡常数(K)与温度(T)的关系如表:T/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
关于该反应的说法错误的是( )
 2CO(g)+2H2(g) ΔH。回答下列问题:
2CO(g)+2H2(g) ΔH。回答下列问题:
-
(1) 已知:

则ΔH=(用ΔH1和ΔH2表示)。
-
(2) 采用“HSD-2型”催化剂时,该重整反应的速率方程为v正=k·p(CH4)[p(CH4)表示CH4气体分压、k为速率常数],下列说法正确的是____(填标号)。A . 改变催化剂,ΔH不变 B . 升高温度,v正增大 C . 增大CO2的分压时,v正变大 D . 在反应达到平衡时,v正=0
-
(3) 该重整反应的浓度平衡常数的表达式,Kc=,已知,Kc与温度(T)的关系如图,则ΔH0(填“>”、“<”或“=”),判断的理由是。

-
(4) 在T℃、压强为P时,将CH4和CO2按投料比
 加入恒容容器中,当反应达平衡时CH4的转化率为80%,CO2的转化率为90%。经分析,该容器中同时发生了副反应:CO2(g)+H2(g)
加入恒容容器中,当反应达平衡时CH4的转化率为80%,CO2的转化率为90%。经分析,该容器中同时发生了副反应:CO2(g)+H2(g)  CO(g)+H2O(g),则平衡时H2和H2O的物质的量之比为,若温度、压强和投料比一定,为了提高重整反应的速率和H2的选择性,应当。
CO(g)+H2O(g),则平衡时H2和H2O的物质的量之比为,若温度、压强和投料比一定,为了提高重整反应的速率和H2的选择性,应当。
-
(5) 工业上已实现利用H2处理废水中的氮氧化合物,如下图所示。

该电池正极的电极反应式为。
 (Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①
(Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①
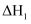
②

③

④

总反应为

下列说法正确的是( )
 (Ⅲ)晶面铁原子簇能够有效降低合成氨反应的活化能和焓变
B . 相同条件下,若1mol氢原子所具有的能量为E1 , 1 mol氢分子的能量为E2 , 则
(Ⅲ)晶面铁原子簇能够有效降低合成氨反应的活化能和焓变
B . 相同条件下,若1mol氢原子所具有的能量为E1 , 1 mol氢分子的能量为E2 , 则 C . 反应①和总反应均为放热反应
D . 总反应的
C . 反应①和总反应均为放热反应
D . 总反应的
①已知
 , 则氢气的燃烧热
, 则氢气的燃烧热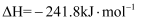 ;
;
②单质A和单质B互为同素异形体,由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定;
③
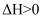 , 恒温恒压条件下达到平衡后加入X,上述反应的
, 恒温恒压条件下达到平衡后加入X,上述反应的 增大;
增大;
④根据下表数据可以计算出3H2+![]()

![]() 的焓变;
的焓变;
|
共价键 |
C-C |
|
C-H |
H-H |
|
键能/( |
348 |
610 |
413 |
436 |
⑤根据盖斯定律可推知在相同条件下,金刚石或石墨燃烧生成1mol (g)时,放出的热量相等;
(g)时,放出的热量相等;
⑥25℃、101kPa时,1mol碳完全燃烧生成 (g)所放出的热量为碳的燃烧热。
(g)所放出的热量为碳的燃烧热。
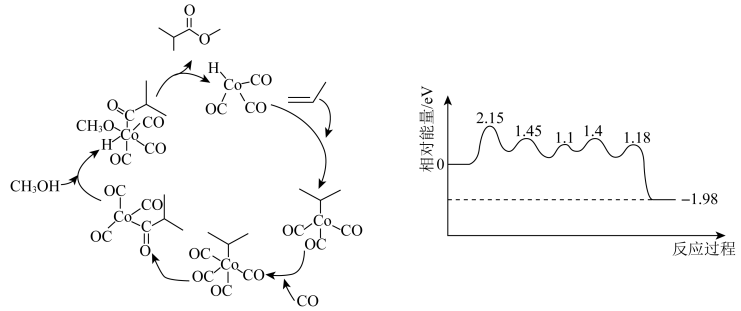

 B . 第一步反应决定了总反应的化学反应速率
C .
B . 第一步反应决定了总反应的化学反应速率
C .  是反应的催化剂
D .
是反应的催化剂
D .  的能量比1mol
的能量比1mol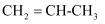 、1molCO、1mol
、1molCO、1mol 的总能量低
的总能量低

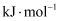 )
)


