金属的通性 知识点题库
下列描述的一定是金属元素的是()
A . 易失去电子的物质
B . 原子核内有11个质子的元素
C . 能与酸反应的物质
D . 原子的最外层只有一个电子的元素
金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的说法不正确的是( )
A . 合金的性质与其成分金属的性质不完全相同
B . 工业上金属Mg、Al都是用电解熔融的氯化物制得的
C . 金属冶炼的本质是金属阳离子得到电子变成金属原子
D . 越活泼的金属越难冶炼,冶炼方法与其活泼性有关
下列关于金属元素特征的叙述,正确的是( )
A . 金属元素的原子只有还原性,离子只有氧化性
B . 金属元素在化合物中一定显正价
C . 金属单质都可以和酸反应置换出氢气
D . 金属元素的单质在常温下均为固体
某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2 .

-
(1) 在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式: MnO2+ FeS+ H2SO4= MnSO4+ Fe2(SO4)3+ S+ H2O
-
(2) 将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如图甲的工业流程进行操作处理得溶液(IV),电解溶液(IV)即得MnO2和Zn.
a、操作①中加Zn粉后发生反应的离子方程式为。
b、操作②中加入适量X的作用是什么 ;X的首选物的化学式是: 。
c、操作③中所加碳酸盐的化学式是 。
-
(3) 为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3 , 工厂设计了如图乙的有关流程图。
a、AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为 。若总共得到n molAl(OH)3 , 则消耗的NaOH和HCl的理论量(mol)分别为 、 。
b、若使用如图丙流程回收处理,请比较两个流程消耗酸碱的用量? 。
下列叙述中,属于金属化学性质的是( )
A . 铝在空气中易与氧气反应生成致密的氧化膜
B . 纯铁是银白色固体
C . 铜容易传热、导电
D . 钨有很高的熔点
不属于金属通性的是( )
A . 延展性
B . 高熔点
C . 导热性
D . 导电性
一定量的锌粉和3mol/L的过量盐酸反应,当向其中加入少量的下列物质时能加快化学反应速率但不影响产生H2总量的是( )
①铁粉 ②银粉 ③石墨粉 ④稀硝酸 ⑤CaCO3 ⑥浓盐酸
A . ②④⑥
B . ①②⑤⑥
C . ②③⑥
D . ②③④⑥
将一定量铁粉和铜粉的混合物加入由稀H2SO4和稀HNO3组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是( )
A . 反应过程中不可能产生H2
B . 剩余的金属粉末中一定有铜
C . 往反应后的溶液中加入KSCN溶液会变红色
D . 往反应后的溶液中加入足量的稀H2SO4 , 则金属粉末的质量一定会减少
与金属的物理性质无关的是()
A . 良好的导电性
B . 反应中易失去电子
C . 延展性
D . 导热性
铁能压成薄片,这是因为()
A . 熔点低
B . 延展性大
C . 硬度小
D . 密度小
下列有关用途的叙述错误的是()
A . 常温下可用铁容器储运浓硫酸
B . 焰色反应可用于检验某些金属元素的存在
C . 氨是制造硝酸的原料
D . 铝制餐具可以长时间盛放咸的食物
下列金属用途和有关性质的对应关系错误的是( )
| 金属用途 | 金属的有关性质 | |
| A | 金可以制成比纸还薄的金箔 | 延展性 |
| B | 生活用铁锅 | 导热性 |
| C | 用铁回收照相定影废液中的银 | 氧化性 |
| D | 用铜制作印刷电路 | 导电性 |
A . A
B . B
C . C
D . D
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
| 金属[ | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
下列有关三种金属的说法正确的是( )
A . 三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B . 若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C . 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D . Cu和稀盐酸不发生化学反应
下列有关金属及其合金的说法正确的是( )
A . 用焰色反应鉴别NaCl、KCl和Na2SO4
B . 合金与各组分金属相比一般具有更低的熔点
C . 生铁、普通钢和不锈钢中的碳含量依次增加
D . Fe2O3是磁铁矿的主要成分,属于碱性氧化物
金属材料在日常生活、生产中有着广泛的运用,下列关于金属的说法错误的是( )
A . 工业上金属Mg、Al都是用电解熔融的氯化物制得的
B . 合金的性质与其成分金属的性质不完全相同
C . 金属冶炼的本质是金属阳离子得到电子变成金属原子
D . 越活泼的金属越难冶炼
关于金属元素的特征,下列叙述正确的是( )
①金属元素的原子只有还原性,离子只有氧化性②金属元素在化合物中一般显正价 ③金属性越强的元素相应的低价离子氧化性越弱④价电子越多的金属原子的金属性越强
A . ①②
B . ②③
C . ①④
D . ③④
下列有关金属及其合金的说法中,错误的是( )
A . 硬铝、青铜、不锈钢都属于合金,合金的许多性能优于纯金属,而熔点低于成分金属
B . 合金中用量最大的是钢,其含碳量越大,韧性越好
C . 日用铝制品表面覆盖着致密的氧化膜,对内部金属起保护作用
D . 纳米铜的水溶液具有丁达尔效应
下列说法错误的是( )
A . 常温下,铁在浓硫酸中发生钝化,可用铁槽车贮运浓硫酸
B . 金属铜具有良好的导电性,可用来制作导线
C . MgO的熔点很高,可用做耐高温材料
D . SO2具有漂白性,可用于木耳食品的漂白
根据所学知识回答下列问题:
-
(1) 常温下镁、铝都具有较强的抗腐蚀性,主要原因是。
-
(2) 标准状况下,
 与同条件下
与同条件下 含有相同的氢原子数。
含有相同的氢原子数。
-
(3) 标准状况下,
 的质量为g。
的质量为g。
-
(4) 实验室用
 与100mL足量的浓盐酸制取氯气,发生反应:
与100mL足量的浓盐酸制取氯气,发生反应: (浓)
(浓)
 。当
。当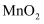 完全反应时,参加反应的HCl的物质的量为
完全反应时,参加反应的HCl的物质的量为 , 假设反应后溶液的体积仍为100mL,则反应后的溶液中生成的
, 假设反应后溶液的体积仍为100mL,则反应后的溶液中生成的 的物质的量浓度为mol/L。
的物质的量浓度为mol/L。
-
(5) 实验室需配制
 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为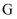 。配制时,其正确的操作顺序是(填标号,每个标号只能用一次)。
。配制时,其正确的操作顺序是(填标号,每个标号只能用一次)。①用
 水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,摇匀
水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,摇匀②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下
 处
处
下列有关金属的用途与相应性质不对应的是( )
A . 用金做饰物是因为金的化学性质稳定、不褪色
B . 用钨做白炽灯灯丝是因为其熔点高、导电性好
C . 用镁合金做汽车部件是因为镁的密度小,化学性质活泼
D . 用铝做包装用的铝箔是因为其延展性好,表面有钝化膜
最近更新



