上海市高三化学期中考试(2018年上半期)在线答题
| 1. 选择题 | 详细信息 |
|
下列有关科学家及其创建理论的描述中,错误的是 A.拉瓦锡阐明了质量守恒定律 B.道尔顿创立分子学说 C.门捷列夫发现了元素周期律 D.勒沙特列发现化学平衡移动原理 |
|
| 2. 选择题 | 详细信息 |
|
对下列化学用语的理解正确的是 A. 原子结构示意图 B. 比例模型 C. 电子式: D. 分子式C2H4O2:可以表示乙酸,也可以表示乙二醇 |
|
| 3. 选择题 | 详细信息 |
|
下列有关化学基本概念的判断正确的是( ) A.含有极性键的分子一定是极性分子 B.含有共价键的化合物一定是共价化合物 C.含有离子键的化合物一定是离子化合物 D.组成上相差n个CH2的分子一定是同系物 |
|
| 4. 选择题 | 详细信息 |
|
天然橡胶与溴接触,橡胶被破坏,主要是因为发生了 A.加成反应 B.取代反应 C.氧化反应 D.聚合反应 |
|
| 5. 选择题 | 详细信息 |
|
某物质有以下性质:①是电解质 ②溶解时有化学键的破坏 ③熔化时没有化学键的破坏,则该物质固态时属于 A. 原子晶体 B. 离子晶体 C. 分子晶体 D. 金属晶体 |
|
| 6. 选择题 | 详细信息 |
|
SiF4与SiCl4分子都是正四面体结构。下列判断正确的是( ) A.键长:Si-F>Si-Cl B.键能:Si-F>Si-Cl C.沸点:SiF4>SiCl4 D.共用电子对偏移程度:Si-Cl>Si-F |
|
| 7. 选择题 | 详细信息 |
|
下列试剂不能用来鉴别SO2和H2S的是 A.新制氯水 B.品红溶液 C.氢氧化钠溶液 D.氢硫酸 |
|
| 8. 选择题 | 详细信息 |
|
下列物质酸性最弱的是 A.CH3COOH B.CH3CH2OH C.H2CO3 D.H2O |
|
| 9. 选择题 | 详细信息 |
|
可逆反应X(g) + Y A.增大压强,平衡体系颜色加深,说明Y必是气体 B.增大压强,当c(X)= c(Z) 时,则再次达到平衡 C.若Y是气体,增大X的浓度会使Y的转化率增大,化学平衡常数也增大 D.升温,Z的质量分数减小,说明正反应是放热反应 |
|
| 10. 选择题 | 详细信息 |
|
下列反应中,水作还原剂的反应是 A.CaO + H2O → Ca(OH)2 B.2Na + 2H2O → 2NaOH + H2↑ C.2F2 + 2H2O → 4HF + O2 D.2Na2O2 + 2H2O → 2NaOH + O2↑ |
|
| 11. 选择题 | 详细信息 |
反应A2(g)+B2(g) →2AB(g)的能量变化如图所示,叙述正确的是  A. 该反应是放热反应 B. 加入催化剂,(b-a)的差值减小 C. 每生成2molAB分子吸收bkJ热量 D. 若反应生成AB为液态,吸收的热量小于(a-b)kJ |
|
| 12. 选择题 | 详细信息 |
|
下列化工生产中未涉及勒沙特列原理的是 A.侯氏制碱法 B.合成氨 C.氯碱工业 D.工业制硫酸 |
|
| 13. 选择题 | 详细信息 |
下列曲线表示F、Cl、Br元素及所形成物质的某种性质随核电荷数的变化趋势,正确的是  A. A B. B C. C D. D |
|
| 14. 选择题 | 详细信息 |
|
将浓度和体积均相同的一元酸HA与一元碱BOH混合,所得溶液呈酸性。下列判断正确的是 A.HA一定不是弱酸 B.BOH一定不是强碱 C.HA一定是强酸 D.BOH一定是强碱 |
|
| 15. 选择题 | 详细信息 |
|
下列烃与氯气反应,只生成一种一氯代物的是 A.2﹣甲基丙烷 B.异戊烷 C.间三甲苯 D.2,2﹣二甲基丙烷 |
|
| 16. 选择题 | 详细信息 |
用如图所示装置电解氯化铜溶液。下列判断正确的是 A.Y电极为正极 B.X电极质量增加 C.Y电极表面有氯气生成 D.X电极表面发生氧化反应 |
|
| 17. 选择题 | 详细信息 |
甲与乙在溶液中的转化关系如下图所示(反应条件省略),甲不可能是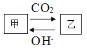 A.NH3 B.AlO2- C.CO32- D.CH3COO- |
|
| 18. 选择题 | 详细信息 | ||||||
下表是25℃时有关弱酸的电离平衡常数,下列叙述正确的是
|
|||||||
| 19. 选择题 | 详细信息 |
|
下列各组物质充分反应后,滴入KSCN溶液一定显红色的是( ) A.FeO加入稀硝酸中 B.FeCl3、CuCl2溶液中加入过量的铁粉 C.生了锈的铁块加入稀硫酸中 D.Fe加入稀硝酸中 |
|
| 20. 选择题 | 详细信息 |
|
某无色溶液可能含有H+、Na+、Al3+、Br- 、HCO3- 、SO42- 和NO3- ,且各离子的物质的量浓度相等。分别取样,①测得该溶液的pH=1;②滴加适量氯水,溶液变为橙色;③滴加过量Ba(OH)2溶液,有沉淀生成。由此可知原溶液中 A.一定含有NO3- B.可能含有Na+ C.可能不含Al3+ D.含有3种离子 |
|
| 21. 解答题 | 详细信息 | ||||||||||||||||||
SO2的催化氧化是工业制取硫酸的关键步骤之一:2SO2 + O2
|
|||||||||||||||||||
| 22. 综合题 | 详细信息 |
|
Na2S常用作皮革脱毛剂,工业上用反应Na2SO4 +2C (1)上述反应中涉及的各元素中原子半径最小的是_______(填元素符号),该原子有_____种不同能量的电子。 (2)羰基硫的化学式为COS,结构和CO2 相似,请写出COS的电子式_________,判断羰基硫分子属于________(选填“极性”或“非极性”)分子。 (3)写出一个能比较S和O非金属性强弱的化学事实_____________________ ;请从原子结构解释原因_____________________________。 (4)将Na2S溶液滴入AlCl3溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解释上述现象__________________________。 |
|
| 23. 推断题 | 详细信息 |
衣康酸M是制备高效除臭剂、粘合剂等多种精细化学品的重要原料,可经下列反应路线得到(部分反应条件已略)。 已知:①R-CH2-Cl + NaCN → R-CH2-CN + NaCl ②R-CH2-CN + NaOH + H2O → R-CH2-COONa + NH3 完成下列填空: (1)A的结构简式是_____________,M中官能团的名称是________________, (2)写出B→ C的化学反应方程式________________________________________。写出G的结构简式______________________________________ (3)反应a与反应b的先后顺序不能颠倒,解释原因:_________________________________________________________________________。 (4)写出由A和1,3—丁二烯1:1共聚所得高聚物的结构简式____________________________ (5)请设计由CH2=CHCH2OH 制备CH2=CHCOOH的合成路线(无机试剂任选)________________________________________。 |
|
| 24. 实验题 | 详细信息 | ||||||||||||||
|
氨气是重要的化工原料。 (1)检验氨气极易溶于水的简单操作是:收集一试管氨气,______________。 (2)往饱和食盐水中依次通入足量的NH3和足量的CO2,生成沉淀的化学式为_________;过滤后,使余液尽可能析出较多NH4Cl晶体的方法是:再通入足量的NH3、冷却并加入________,请说明这样操作为什么可以析出较多NH4Cl的原因:_________________。某NaHCO3晶体中含有NaCl杂质,某同学在测定其中NaHCO3的含量时,称取5.000g试样,定容成100mL溶液,用标准盐酸溶液滴定(用甲基橙做指示剂),测定数据记录如下:
|
|||||||||||||||