枣庄市高二化学下册月考试卷刷题训练
| 1. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 分子间作用力与化学键的大小相当 B. 分子间作用力的大小远大于化学键,是一种很强的作用力 C. 分子间作用力主要影响物质的化学性质 D. 分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作用,称为分子间作用力 |
|
| 2. 选择题 | 详细信息 |
|
下列说法不正确的是( ) A. σ键比π键重叠程度大,形成的共价键强 B. 两个原子之间形成共价键时,最多有一个σ键 C. 气体单质中,一定有σ键,可能有π键 D. N2分子中有一个σ键,2个π键 |
|
| 3. 选择题 | 详细信息 |
|
下列说法中正确的是 A. NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 B. P4和CH4都是正四面体形分子且键角都为109°28′ C. NH4+的电子式为 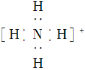 ,离子呈平面正方形结构 ,离子呈平面正方形结构D. NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
|
| 4. 选择题 | 详细信息 |
|
下列关于苯乙炔的说法错误的是 ( ) A. 该分子有8个σ键,5个π键 B. 该分子中碳原子有sp和sp2杂化 C. 该分子存在非极性键 D. 该分子中有8个碳原子在同一平面上 |
|
| 5. 选择题 | 详细信息 |
|
下列事实与氢键有关的是 A. HF、HCl、HBr、HI的热稳定性依次减弱 B. 水加热到很高的温度都难以分解 C. CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 D. 水结成冰体积膨胀 |
|
| 6. 选择题 | 详细信息 |
|
下列中心原子采取sp2杂化且为非极性分子的是 A.CS2 B.H2S C.SO2 D.SO3 |
|
| 7. 选择题 | 详细信息 |
|
固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子层结构,则下列有关说法中,不正确的是( ) A.1 mol NH5中含有5NA个N—H键(NA表示阿伏加德罗常数) B.NH5中既有共价键又有离子键,NH5是离子化合物 C.NH5的电子式为  D.它与水反应的化学方程式为NH5+H2O=NH3·H2O+H2↑ |
|
| 8. 选择题 | 详细信息 |
|
已知原子数和价电子数相同的离子或分子结构相似,如SO3、NO3-都是平面三角形。那么下列分子或离子中与SO42-有相似结构的是( ) A.PCl5 B.CCl4 C.NF3 D.N3- |
|
| 9. 选择题 | 详细信息 |
|
下列有关共价键的叙述中,不正确的是 A. 某原子跟其他原子形成共价键时,其共价键键数一定等于该元素原子的价电子数 B. 水分子内氧原子的电子数已经达到饱和,故一般不能再结合其他氢原子 C. 非金属元素原子之间形成的化合物也可能是离子化合物 D. 所有简单离子的核电荷数与其核外电子数一定不相等 |
|
| 10. 选择题 | 详细信息 |
|
化合物NH3与BF3可以通过配位键形成NH3·BF3,下列说法正确的是( ) A. NH3与BF3都是三角锥形 B. NH3与BF3都是极性分子 C. NH3·BF3中各原子都达到8电子稳定结构 D. NH3·BF3中,NH3提供孤电子对,BF3提供空轨道 |
|
| 11. 选择题 | 详细信息 |
|
下列说法正确的有几句( ) ①离子键与共价键的本质都是静电作用;②任何物质中都存在化学键;③氢键是极弱的化学键;④离子键就是阴、阳离子之间的静电吸引力;⑤活泼金属与活泼非金属化合时能形成离子键;⑥任何共价键中,成键后原子均满足8电子稳定结构;⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电;⑧两种非金属元素形成的化合物不可能含有离子键;⑨化学键断裂,一定发生化学变化 A. 1 B. 2 C. 3 D. 4 |
|
| 12. 选择题 | 详细信息 |
|
下列关于离子键和离子化合物的说法正确的是( ) A. 阴、阳离子通过静电引力形成离子键 B. 阴、阳离子间通过离子键一定能形成离子化合物 C. 离子化合物一定能导电 D. 只有在活泼金属元素和活泼非金属元素化合时,才能形成离子键 |
|
| 13. 选择题 | 详细信息 |
|
共价键、离子键和范德华力是微粒之间的三种作用力。下列晶体中含有两种作用力的是 A.Ar B.SiO2 C.Na2O2 D.金刚石 |
|
| 14. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. HF、HCl、HBr、HI的熔沸点依次升高 B. CH4、CCl4都是含有极性键的非极性分子 C. CS2、H2S、C2H2都是直线形分子 D. 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
|
| 15. 选择题 | 详细信息 |
|
物质结构包括原子结构、分子结构、晶体结构。下列关于物质结构与性质的说法正确的是 A.SiO2晶体为原子晶体,CO2晶体为分子晶体 B.σ键都是由两个p轨道“头碰头”重叠形成的 C.VSEPR模型就是分子的空间构型 D.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
|
| 16. 选择题 | 详细信息 |
|
下列有关离子晶体的数据大小比较不正确的是( ) A. 熔点:NaF>MgF2>AlF3 B. 晶格能:NaF>NaCl>NaBr C. 阴离子的配位数:CsCl>NaCl>CaF2 D. 硬度:MgO>CaO>BaO |
|
| 17. 选择题 | 详细信息 |
|
下列说法中,不正确的是 A. 金属晶体中一定含有金属键 B. 在含有阳离子的化合物的晶体中,一定含有阴离子 C. 含有金属元素的离子不一定是阳离子 D. 金属晶体中原子的堆积方式都是A3或A1型最密堆积 |
|
| 18. 选择题 | 详细信息 |
|
下列说法中正确的是 ( ) ①晶体中分子间作用力越大,分子越稳定 ②原子晶体中共价键越强,熔点越高 ③干冰是CO2分子通过氢键和分子间作用力有规则排列成的分子晶体 ④在Na2O和Na2O2晶体中,阴、阳离子数之比相等 ⑤正四面体构型的分子,键角都是109°28′,其晶体类型可能是原子晶体或分子晶体 ⑥分子晶体中都含有化学键 ⑦含4.8 g碳元素的金刚石晶体中的共价键的物质的量为0.8 mol A.①②③④⑤ B.②④⑦ C.②④⑥⑦ D.③④⑤⑥⑦ |
|
| 19. 选择题 | 详细信息 |
|
根据下列性质判断,属于原子晶体的物质是 A. 熔点2700℃,导电性好,延展性强 B. 无色晶体,熔点3550℃,不导电,质硬,难溶于水和有机溶剂 C. 无色晶体,能溶于水,质硬而脆,熔点为800℃,熔化时能导电 D. 熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电 |
|
| 20. 选择题 | 详细信息 |
氢是重要而洁净的能源。要利用氢气作为能源,必须解决好安全有效地储存氢气的问题。化学家研究出利用合金储存氢气的方法,其中镧(La)镍(Ni)合金是一种储氢材料,这种合金的晶体结构已经测定,其基本结构单元如图所示,则该合金的化学式可表示为( ) A. LaNi5 B. LaNi C. La4Ni24 D. La7Ni12 |
|
| 21. 选择题 | 详细信息 |
|
下列关于微粒间作用力与晶体的说法不正确的是 A. 某物质呈固体时不导电,熔融状态下能导电,则该物质一定是离子晶体 B. H2O和CCl4的晶体类型相同,且每个原子的最外层都达到8电子稳定结构 C. F2、Cl2、Br2、I2的沸点逐渐升高,是因为分子间作用力逐渐增大 D. 干冰溶于水中,既有分子间作用力的破坏,也有共价键的破坏 |
|
| 22. 选择题 | 详细信息 |
四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是(假设金属的摩尔质量为Mg·mol-1金属原子半径为r cm,用NA表示阿伏加德罗常数的值) A.金属Zn采用②堆积方式 B.①和③中原子的配位数分别为:6、8 C.对于采用②堆积方式的金属的晶胞质量为 D.金属锻压时,会破坏密堆积的排列方式 |
|
| 23. 选择题 | 详细信息 |
|
下面有关晶体的叙述中,不正确的是 ( ) A.金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子 B.氯化钠晶体中,每个Na+周围距离相等的Na+共有12个 C.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 D.金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构 |
|
| 24. 选择题 | 详细信息 |
磷化硼是一种超硬耐磨涂层材料,右图为其晶胞,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( ) A. 磷化硼晶体中每个原子均形成4条共价键 B. 磷化硼晶体的化学式为BP,属于离子晶体 C. 磷化硼晶体的熔点很低 D. 磷化硼晶体结构中微粒的空间堆积方式与氯化钠晶体相同 |
|
| 25. 选择题 | 详细信息 |
|
金属具有延展性的原因是 A. 金属原子半径都较大,价电子数较少 B. 金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈的作用 C. 金属中大量自由电子受外力作用时,运动速率加快 D. 自由电子受外力作用时能迅速传递能量 |
|
| 26. 选择题 | 详细信息 |
下图是金属晶体内部的电气理论示意图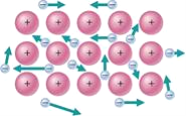 仔细观察并用电气理论解释金属导电的原因是 A. 金属能导电是因为含有金属阳离子 B. 金属能导电是因为含有的自由电子在外电场作用下做定向运动 C. 金属能导电是因为含有电子且无规则运动 D. 金属能导电是因为金属阳离子和自由电子的相互作用 |
|
| 27. 选择题 | 详细信息 |
正硼酸(H3BO3)是一种片层状结构白色晶体,有与石墨相似的层状结构,受热易分解,层内的H3BO3分子通过氢键相连(如图所示),则下列有关说法中不正确的是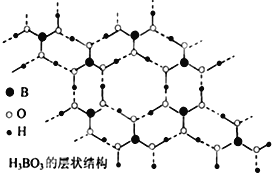 A. 正硼酸晶体属于分子晶体 B. 正硼酸分子的稳定性与氢键无关 C. 1molH3BO3晶体中含有3mol氢键 D. B原子杂化轨道的类型sp2,层间的H3BO3分子通过共价键相连 |
|
| 28. 选择题 | 详细信息 | |||||||||||||||
下列对一些实验事实的理论解释正确的是( )
|
||||||||||||||||
| 29. 选择题 | 详细信息 |
|
下列关于晶体的说法,一定正确的是( ) A. 分子晶体中都存在共价键 B. 金属晶体的熔点都比分子晶体的熔点高 C. SiO2晶体中每个硅原子与两个氧原子以共价键相结合 D. CaTiO3晶体(如图所示)中每个Ti4+与12个O2-紧邻 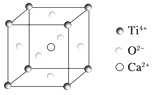 |
|
| 30. 选择题 | 详细信息 |
下列数据是对应物质的熔点(℃): 据此做出的下列判断中错误的是( ) A.铝的化合物的晶体中有的不是分子晶体 B.表中只有BCl3和干冰是分子晶体 C.同族元素的氧化物可形成不同类型的晶体 D.不同族元素的氧化物可形成相同类型的晶体 |
|
| 31. 选择题 | 详细信息 |
|
乙烯分子中含有4个C—H键和1个C=C键,6个原子在同一平面上。下列关于乙烯分子的成键情况分析正确的是( ) A.每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道 B.每个C原子的2s轨道与2个2p轨道杂化,形成3个sp2杂化轨道 C.每个C原子的2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道 D.每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道 |
|
| 32. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. CaCl2晶体中存在共价键 B. H2SO4溶于水能电离出H+和SO42-,所以硫酸是离子化合物 C. SiO2属于原子晶体,熔化破坏共价键和分子间作用力 D. I2是分子晶体,加热升华过程中只需克服分子间作用力 |
|
| 33. 选择题 | 详细信息 |
第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如下图所示,下列关于RCl5分子的说法中正确的是( ) A. 每个原子都达到8电子稳定结构 B. 分子中5个R—Cl键键能不相同 C. 键角(Cl—R—Cl)有90°、120°、180°几种 D. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子 |
|
| 34. 选择题 | 详细信息 |
BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R: 反应过程中新形成的化学键中无( ) A.离子键 B.配位键 C.非极性共价键 D.氢键 |
|
| 35. 选择题 | 详细信息 |
|
关于晶体的叙述中,正确的是 A. 分子晶体中,共价键的键能越大,熔、沸点越高 B. 分子晶体中,分子间的作用力越大,该分子越稳定 C. 原子晶体中,共价键的键能越大,熔、沸点越高 D. 某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
|
| 36. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.水分解和二氧化硅熔化克服的化学键类型不相同 B.Mg3N2和MgCl2晶体中均存在只存在离子键 C.C2H4和N2H4两种分子中都含有单键和双键 D.HF、HCl、HBr、HI的分子间作用力依次增大,沸点依次升高 |
|
| 37. 选择题 | 详细信息 |
(双选)下图所示是晶体结构中具有代表性的最小重复单元(晶胞)的排列方式,其对应的化学式正确的是(图中: A. A B. B C. C D. D |
|
| 38. 选择题 | 详细信息 |
|
下列说法中错误的是 A. 从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 B. 1 mol金刚石晶体中,平均含有2 mol C—C键 C. 水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 D. 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE  |
|
| 39. 选择题 | 详细信息 |
|
(双选)下列描述中正确的是( ) A. CS2为V形的极性分子 B. ClO C. SF6中有6对完全相同的成键电子对 D. SiF4和SO |
|
| 40. 选择题 | 详细信息 |
钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列有关说法中正确的是 A. 该晶体属于离子晶体 B. 晶体的化学式为Ba2O2 C. 该晶体的晶胞结构与CsCl相似 D. 与每个Ba2+距离相等且最近的Ba2+共有12个 |
|
最近更新



