甘肃高二化学2019年前半期月考测验在线答题
| 1. 选择题 | 详细信息 |
|
未来新能源的特点是资源丰富,使用时对环境无污染或很少污染,且有些可以再生,下列全部属于新能源的是一组是( ) ①天然气 ②煤 ③核能 ④石油 ⑤海洋能 ⑥地热能 ⑦风能 ⑧氢能. A. ①②③④ B. ⑤⑥⑦⑧ C. ③④⑤⑥ D. 除①②外 |
|
| 2. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 需要加热才能发生的反应一定是吸热反应 B. 化学反应中的能量变化都表现为热量变化 C. 任何放热反应在常温下一定能发生 D. 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
|
| 3. 选择题 | 详细信息 |
|
下列说法正确的是 A. 增大反应物浓度,可增大单位体积内活化分子的百分数从而使有效碰撞次数增大 B. 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 C. 催化剂不影响活化能但能增大单位体积内活化分子百分数,从而增大反应速率 D. 升温能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
|
| 4. 选择题 | 详细信息 |
|
在2A+B A. v(A)=0.5mol·L-1·s-1 B. v(B)=0.3mol·L-1·s-1 C. v(C)=0.6mol·L-1·s-1 D. v(D)=1mol·L-1·s-1 |
|
| 5. 选择题 | 详细信息 |
|
已知下列反应的平衡常数:①H2(g)+S(s) A. K1+K2 B. K1-K2 C. K1×K2 D. K1/K2 |
|
| 6. 选择题 | 详细信息 |
|
已知中和热的热化学方程式为H + (aq)+OH - (aq)=H2O(l)△H=-57.3kJ·mol-1。下列反应均在稀溶液中进行,其中△H=-57.3kJ·mol-1的是 A. NaOH(aq)+ HNO3 (aq)= NaNO3(aq) + H2O(l) △H B. NH3·H2O(aq)+ HCl(aq)= NH4Cl(aq)+ H2O(l) △H C. HF(aq)+ KOH(aq)= KF(aq)+ H2O(l) △H D. ½H2SO4(aq)+ ½Ba(OH)2(aq)= ½BaSO4(s)+ H2O(l) △H |
|
| 7. 选择题 | 详细信息 |
|
反应A(g)+ 3B(g) A. 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 B. 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 C. 正反应速率和逆反应速率都减小,平衡向正反应方向移动 D. 正反应速率和逆反应速率都减小,平衡向逆反应方向移动 |
|
| 8. 选择题 | 详细信息 |
|
已知①NO + NO=N2O2(快反应),②N2O2 + H2= N2O + H2O(慢反应),③N2O + H2=N2 + H2O(快反应)。下列说法正确的是 A. 整个过程中,反应速率由快反应步骤 ①、③ 决定 B. N2O2、N2O是该反应的催化剂 C. 当 v(NO)正 =v(N2)逆 时反应达到平衡状态 D. 总反应的化学方程式为2NO + 2H2=N2 + 2H2O |
|
| 9. 选择题 | 详细信息 |
|
一定温度下,可逆反应2NO2(g) A. ①④⑤⑥ B. ①③④⑥ C. ①②③⑤ D. ②⑤⑥ |
|
| 10. 选择题 | 详细信息 |
|
已知反应mX(g)+nY(g) 时,下列说法正确的是( ) A. 通入稀有气体使压强增大,平衡将正向移动 B. X的正反应速率是Y的逆反应速率的m/n倍 C. 降低温度,混合气体的平均相对分子质量变小 D. 若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m |
|
| 11. 选择题 | 详细信息 |
|
当密闭容器中合成氨反应N2+3H2 A. 容器内的总压强为原来的2倍 B. N2的浓度比原来平衡浓度小 C. H2的转化率为原来的2倍 D. 气体的密度为原来的2倍 |
|
| 12. 选择题 | 详细信息 |
反应H2(g) + I2(g) ①增大H2浓度 ②缩小容器体积 ③恒容时充入Ar气 ④使用催化剂 A. ①② B. ③④ C. ②④ D. ①④ |
|
| 13. 选择题 | 详细信息 |
研究小组发现一种化合物在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4min~8min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是 A. 2.5μmol·L-1·min-1和2.0μmol·L-1 B. 2.5μmol·L-1·min-1和2.5μmol·L-1 C. 3.0μmol·L-1·min-1和3.0μmol·L-1 D. 3.0μmol·L-1·min-1和2.5μmol·L-1 |
|
| 14. 选择题 | 详细信息 |
一定温度下,在2L的密闭容器中,X、 Y、Z三种气体的物质的量随时间变化的曲线如图所示: 下列描述正确的是( ) A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)-1 B. 反应开始到l0s,X的物质的量浓度减少了0.79mol/L C. 反应开始到10s时,Y的转化率为79.0% D. 反应的化学方程式为:X(g)+Y(g) |
|
| 15. 选择题 | 详细信息 |
|
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡: CO(g)+H2S(g) 反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是 A. 升高温度,H2S浓度增加,表明该反应是吸热反应 B. 通入CO后,正反应速率逐渐增大 C. 反应前H2S物质的量为7mol D. CO的平衡转化率为80% |
|
| 16. 选择题 | 详细信息 |
|
已知:2C(s)+O2(g)===2CO(g) ΔH=-Q1 kJ·mol-1; C(s)+O2(g)===CO2(g) ΔH=-Q2 kJ·mol-1; S(s)+O2(g)===SO2(g) ΔH=-Q3 kJ·mol-1。 CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( ) A. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-2Q2+Q3) kJ·mol-1 B. S(s)+2CO(g)===SO2(g)+2C(s) ΔH=(Q1-Q3) kJ·mol-1 C. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(Q1-2Q2+Q3) kJ·mol-1 D. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-Q2+2Q3) kJ·mol-1 |
|
| 17. 选择题 | 详细信息 |
|
在密闭容器中充入4 mol A,在一定温度和体积可变的密闭容器中发生如下反应:4A(g) A. 若向密闭体系内再加入3molB、2molC,达平衡时C的百分含量与原平衡相同 B. 达到平衡时气体的总物质的量、密度都不发生变化 C. 反应达平衡的过程中,释放出的热量不发生变化 D. 升高温度A的转化率大于30% |
|
| 18. 选择题 | 详细信息 |
|
已知:4NH3(g) + 5O2(g) =4NO(g) + 6H2O(g),△H= —1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是 A. 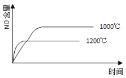 B. 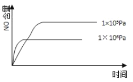 C. 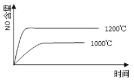 D.  |
|
| 19. 填空题 | 详细信息 |
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题: (1)图中A、C分别表示____,___,E的大小对该反应的反应热__(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___(填“升高”或“降低”),ΔH___(填“变大”“变小”或“不变”)。 (2)图中ΔH=____kJ·mol-1。 (3)依据事实,写出下列反应的热化学方程式。 ①1molN2(g)与适量H2(g)反应,生成NH3(g),放出92.2kJ热量:_____。 ②1molCu(s)与适量O2(g)反应,生成CuO(s),放出157kJ热量:_____。 ③在25℃、101kPa时,8 g CH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式是_____。 |
|
| 20. 实验题 | 详细信息 |
|
50mL0.5mol·L-1盐酸跟50 mL0.55mol·L-1NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题: (1)实验目的:_____。 (2)实验用品:烧杯(500mL和100mL各1只)、温度计、塑料泡沫板(或硬纸板)、泡沫塑料或纸条、____(填写所缺的实验仪器);0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液 (3)实验步骤:(略) (4)问题与结论: ①完整地做一次这样的实验,需测定____次温度。 ②大、小烧杯间填满碎纸条、大烧杯上加盖硬纸板的作用是_____。 ③该实验中NaOH溶液的浓度大于盐酸浓度的作用是____。 ④改用60mL1.0mol·L-1盐酸跟50mL1.1mol·L-1NaOH溶液进行反应,与上述实验相比,所放热量是否相等:___(填相等或不等),所求中和热数值是否相等:___(填相等或不等)。 |
|
| 21. 填空题 | 详细信息 |
|
回答下列问题: (1)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g) + B(g) ①A在5min末的浓度是____________。 ②v(B)=____________。 ③x=____________。 (2)在25℃时,向100mL含氯化氢14.6g的盐酸溶液中,放入5.6g纯铁粉,反应进行到2min末收集到氢气1.12 L(标准状况),在此后又经过4min,铁粉完全溶解。若不考虑溶液体积的变化,则: ①前2min内用FeCl2表示的平均反应速率是______________。 ②后4min内用HCl表示的平均反应速率是________________。 ③前2min与后4min相比,反应速率__________较快,其原因是__________________。 |
|
| 22. 计算题 | 详细信息 |
|
在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达到平衡,此时容器中气体的平均分子量为58。请计算(写出计算过程): (1)10min内SO2的转化率; (2)容器内反应前与平衡时的压强之比(最简整数比) ; (3)该温度下的平衡常数。 |
|
最近更新



