2018吉林高一上学期人教版高中化学期末考试
| 1. | 详细信息 |
|
我国自主研发的载人潜水器“蛟龙号”进行多次海试,圆满完成深潜任务。潜水器若要潜入海底,潜水器的表面每平方米需承受近万吨的压强,这需要使用特殊材料才能达到要求。下列有关材料的说法正确的是() A.铝合金是应用最广泛的合金材料 B.目前太阳能电池的主要材料是硅单质 C.光导纤维的材料是硅单质 D.合金材料的组成元素一定全部是金属元素
|
|
| 2. | 详细信息 |
|
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( ) B.铁红的化学式:Fe3O4 C.Mg2+结构示意图: D.铁丝在氯气中燃烧的化学方程式:Fe+Cl2
|
|
| 3. | 详细信息 |
|
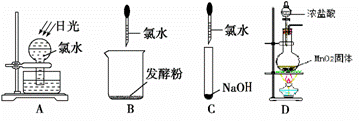
下列药品可用无色带玻璃塞的试剂瓶存放的是() A.盐酸 B. C.氯水 D.
|
|
| 4. | 详细信息 |
|
下列物质中含有Cl-的是 ( ) A.液氯 B.KClO3 C.NaClO D.氯水
|
|
| 5. | 详细信息 |
|
进入秋冬季节后,雾霾这种环境污染问题逐渐凸显。从物质分类来看雾霾属于胶体,它区别于溶液等其它分散系的本质特征是( ) A.胶粒可以导电 B.胶体具有丁达尔效应 C.胶体粒子大小在1~100nm之间 D.胶体的分散剂为气体
|
|
| 6. | 详细信息 |
|
氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气,下列说法错误的是( ) A.氧化产物为N2 B.该反应NH3被还原 C.该反应利用了Cl2的强氧化性 D.生成1 mol N2有6 mol电子转移
|
|
| 7. | 详细信息 | |||||||||||||||||||||||||
|
下列表格中有关物质的分类对应正确的一组是( )
|
||||||||||||||||||||||||||
| 8. | 详细信息 |
|
下列离子方程式正确的是( ) A. 氢氧化钡溶液与硫酸反应:OH+H+= H2O B. 碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑ C. 硫酸铝和氨水反应:Al3++3OH-=Al(OH)3↓ D. Na与H2O反应:2Na+2H2O=2Na++2OH-+H2↑
|
|
| 9. | 详细信息 |
|
在无色溶液中,下列离子能大量共存的是( ) A.Mg2+、SO42-、K +、Cl- B. Na+、NH4+ 、NO3-、MnO4- C.K +、Cu2+ 、Cl-、Br- D.Ba2+ 、Na+ 、OH-、HCO3-
|
|
| 10. | 详细信息 |
|
下列物质中,既能与NaOH溶液又能与盐酸反应的单质是( ) A.Al2O3 B.Al C.Al(OH)3D.Fe
|
|
| 11. | 详细信息 |
|
下列除杂质的方法不正确的是() A.铜粉中混有铁粉:加入过量盐酸充分反应,过滤 B.CO2中混有HCl:将其通入NaOH溶液,洗气 C.NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 D.FeCl2溶液中混有少量FeCl3:加入Fe粉
|
|
| 12. | 详细信息 | |||
|
下列实验中,所选装置不合理的是()
A.分离 C.粗盐提纯,选①和② D.用
|
||||
| 13. | 详细信息 |
|
称取两份铝粉,第一份加足量NaOH溶液,第二份加足量硫酸,如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比是( ) A.1:1 B.1:3 C.3:2 D.1:2
|
|
| 14. | 详细信息 |
|
下列说法正确的是() A.在标准状况下,22.4L水所含分子数目为NA B.11.2L HCl气体其物质的量为0.5mol C.9克Al转变成Al3+时,得到电子数目为NA D.常温时时28g氮气所含氮原子数为2NA
|
|
| 15. | 详细信息 |
|
在FeCl3和CuCl2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子是( ) A.Fe2+和 Fe3+B.Fe2+C.Cu2+和Fe2+ D.Cu2+
|
|
| 16. | 详细信息 |
|
下列说法正确的是() A. B. C. D.硅胶常用于做干燥剂
|
|
| 17. | 详细信息 |
|
下列各组中的两种物质相互作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是() A. C.
|
|
| 18. | 详细信息 |
|
铊(Tl)盐与氰化钾(KCN)被列为A级危险品.已知下列反应在一定条件下能够发生:①Tl3++2Ag=Tl++2Ag+,②Ag++Fe2+=Ag+Fe3+,③Fe+2Fe3+=3Fe2+,下列离子氧化性比较顺序正确的是( ) A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+ C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe2+
|
|
| 19. | 详细信息 |
|
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的原因是() A.向容量瓶中转移溶液时,瓶事先用蒸馏水洗涤过 B.称量时NaOH已经潮解 C.定容时俯视容量瓶的标线 D.摇匀后发现液面低于标线,未做处理。
|
|
| 20. | 详细信息 |
|
现有FeO、Fe2O3、Fe3O4组成的混合物mg,向其中加入l00mL2mol/L硫酸,恰好完全溶解,若mg该混合物在过量CO气流中加热充分反应,则冷却后剩余固体的质量为( ) A.(m﹣1.6)g B.(m﹣2.4)g C.(m﹣3.2)g D.无法计算
|
|
| 21. | 详细信息 |
|
用于提纯或分离物质的方法有: A.萃取分液 B.加热分解 C.蒸发结晶D.分液 E.蒸馏 F.过滤G.渗析等,请将提纯或分离的序号填在后面横线上。 (1)分离饱和食盐水与泥沙的混合物______________________ (2)分离水和汽油的混合物______________________ (3)海水淡化______________________ (4)除去碳酸钠中的碳酸氢钠______________________ (5)除去氢氧化铁胶体中混有的氯离子、钠离子______________________。
|
|
| 22. | 详细信息 |
|
油画所用颜料含有某种白色铅化物,此颜料置于空气中长时间后就会变成黑色PbS,从而使油画的色彩变暗,若用双氧水H2O2来清洗,则可将PbS变成PbSO4,从而使油画复原。 上述清洗反应的化学方程式为PbS+ 4H2O2 = PbSO4 + 4M(已配平) (1)生成物M的化学式为 (2)在此反应中,PbS作剂,H2O2作剂 (3)若发生转移的电子数目2mol时,参加反应的H2O2的质量为。
|
|
| 23. | 详细信息 | |||||||||
|
(1)实验室制取、净化并收集氯气涉及以下几个主要阶段:
现有以下3种试剂:A.饱和食盐水 B.NaOH溶液 C.浓硫酸 请在以上试剂中选择填空: ①X、Y溶液分别应选用(填“A”、“B”或“C”)、 ②尾气处理过程中,多余的氯气可用(填“A”、“B”或“C”)吸收。 (2)某化学兴趣小组为了探究Cl2的相关性质,设计了如下的实验。
①写出Cl2与水反应的离子方程式 ②通入Cl2后,从集气瓶A、B的现象可得出的结论是。 (3)
如图所示,上述实验过程中,不会产生气体的是 写出反应A的化学方程式。 (4)碘是人体中不可缺少的微量元素,碘缺乏病是目前已知的导致人类智力障碍的主要原因,我国在食盐中加入碘元素能有效防止缺碘引起的疾病。
某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如下图: 甲.加入萃取剂后振荡乙.静置分层丙.分离 ①该同学所采用的萃取剂可能是(填“A”、“B”或“C”)。 A.酒精 B.苯C.四氯化碳 ②甲、乙、丙3步实验操作中,不正确的是(填“甲”、“乙”或“丙”)。
|
||||||||||
| 24. | 详细信息 | |||
|
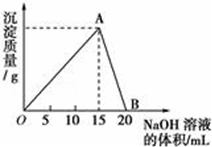
向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
(1)分别用离子方程式表示图中OA段、AB段的反应原理 、. (2)最大沉淀质量为 g (3)所用AlCl3溶液的物质的量浓度是 (4)当所得沉淀量为0.39g时,用去NaOH溶液的体积是 mL或 mL。
|
||||