2019-2020年高二上半年期中考试化学试卷(辽宁省辽河油田第二高级中学)
| 1. 选择题 | 详细信息 |
|
据《本草纲目》记载:“生熟铜皆有青,即是铜之精华,大者即空绿,以次空青也。铜青则是铜器上绿色者,淘洗用之。”生成“铜青”的反应原理为 A.化学腐蚀 B.吸氧腐蚀 C.析氢腐蚀 D.铜与空气中的成分直接发生化合反应 |
|
| 2. 选择题 | 详细信息 |
|
在电解水时,为了增强导电性,加入的电解质最好选用( ) A.Na2SO4 B.CuCl2 C.HCl D.CuSO4 |
|
| 3. 选择题 | 详细信息 |
|
下列有关化学反应速率的判断正确的是 A. 块状大理石、粉状大理石分别与0.1mol/L的盐酸反应,速率相同 B. 常温下,铜片和铁片分别与同浓度的浓硝酸反应,速率:铜片<铁片 C. 同浓度的稀盐酸稀醋酸分别与2mol/L的NaOH溶液反应,开始时反应速率:盐酸>醋酸 D. 不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率 |
|
| 4. 选择题 | 详细信息 |
|
下列有关化学反应与能量的说法正确的是 A.酸碱中和是放热反应 B.炭在氧气中燃烧属于吸热反应 C.化学键的形成需吸收能量 D.化学反应过程中,化学能一定转化成热能 |
|
| 5. 选择题 | 详细信息 |
|
下列过程或现象与盐类水解无关的是 A.向Na2CO3溶液中滴加酚酞试液变红色 B.实验室保存硫酸亚铁溶液时加入少量铁粉 C.加热FeCl3溶液颜色会变深 D.KAl(SO4)2·12 H2O可用于净水 |
|
| 6. 选择题 | 详细信息 |
|
下列对各电解质溶液的分析正确的是( ) A.硫酸铁溶液中能大量共存的离子:K+、Na+、NO3-、CO32- B.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O C.0.1mol•L﹣1Na2S溶液中存在:c(OH-)=c(H+)+c(HS﹣)+2c(H2S) D.NH4HSO4溶液呈酸性的主要原因是:NH4++H2O |
|
| 7. 选择题 | 详细信息 |
|
25℃时,下列事实(或实验)不能证明CH3COOH是弱电解质的是( ) A.CH3COOH溶液与Na2CO3反应生成CO2 B.测定CH3COONa溶液的pH>7 C.取相同pH的盐酸和CH3COOH溶液各稀释100倍,pH变化小的是CH3COOH D.同浓度的盐酸和CH3COOH溶液分别与相同的锌粒反应,CH3COOH溶液的反应速率慢 |
|
| 8. 选择题 | 详细信息 |
|
已知下列热化学方程式:Zn(s) + Hg(l) + 由此可知Zn(s) + HgO(s) = ZnO(s) + Hg(l)的ΔH3,其中ΔH3的值是 A.-260.4 kJ/mol B.-254.6 kJ/mol C.-438.9 kJ/mol D.-441.8 kJ/mol |
|
| 9. 选择题 | 详细信息 |
|
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是 ( ) A.稀NaOH溶液 B.HCl溶液 C.酸性CuSO4溶液 D.酸性AgNO3溶液 |
|
| 10. 选择题 | 详细信息 |
|
在一定温度下的定容密闭容器中,当下列物理量不再随时间变化时,表明反A(s)+2B(g) A.混合气体的压强 B.混合气体的密度 C.混合气体的物质的量 D.混合气体中C和D的物质的量之比 |
|
| 11. 选择题 | 详细信息 |
|
高温下,某反应达到平衡,平衡常数K= A. 该反应是焓变为正值 B. 恒温恒容下,增大压强,H2浓度一定减小 C. 升高温度,逆反应速率减小 D. 该反应化学方程式为CO+H2O |
|
| 12. 选择题 | 详细信息 |
|
某学生欲完成反应2HCl+2Ag=2AgCl+H2↑而设计了下列四个实验,你认为可行的是 A. 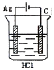 B. B.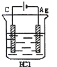 D. D. |
|
| 13. 选择题 | 详细信息 |
|
某温度下,反应SO2(g)+ 1/2O2(g) A. 2500 B. 100 C. 4×10-4 D. 2×10-2 |
|
| 14. 选择题 | 详细信息 |
|
下列物质中能抑制水的电离且使溶液呈现出酸性的是 A.Na2CO3 B.Al2(SO4)3 C.K2SO4 D.NaHSO4 |
|
| 15. 选择题 | 详细信息 |
|
下列离子方程式中,属于水解反应的是( ) A.HCOOH+H2O B.CO2+H2O C.CO32-+ H2O D.HS-+ H2O |
|
| 16. 选择题 | 详细信息 |
|
下列化学电源属于绿色电池的是( ) A.干电池 B.镍镉电池 C.锌锰电池 D.氢氧燃料电池 |
|
| 17. 选择题 | 详细信息 |
|
温总理在十届全国人大四次会议上所作的“政府工作报告”中指出:“抓好资源节约,建设环境友好型社会”,这是我国社会及经济长期发展的重要保证。你认为下列行为中有悖于这一保证的是( ) A.开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料 B.将煤进行“气化”和“液化”处理,提高煤的综合利用效率 C.研究采煤、采油新技术,提高产量以满足工业生产的快速发展 D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
|
| 18. 选择题 | 详细信息 |
|
某温度下,可逆反应mA(g)+nB(g) A. K值越大,表明该反应越有利于C的生成,反应物的转化率越大 B. 若缩小反应器的容积,能使平衡正向移动,则K增大 C. 温度越高,K一定越大 D. 如果m+n=p,则K=1 |
|
| 19. 选择题 | 详细信息 |
|
下列比较中正确的是 A. 相同浓度的三种溶液:①(NH4)2CO3溶液、②NH4HCO3溶液、③NH4NO3溶液中 c(NH4+):③>①>② B. 相同pH的溶液:①NaClO溶液、②NaHCO3溶液、③CH3COONa溶液中 c(Na+):③>②>① C. 同浓度、同体积的溶液:①CH3COONa溶液、②NH4Cl溶液、③NaNO3溶液中 pH:②>③>① D. 相同浓度的溶液:①氨水、②NaOH溶液、③Ba(OH)2溶液 c(H+):②>①>③ |
|
| 20. 综合题 | 详细信息 |
|
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题。 (1)生活中明矾常作净水剂,其净水的原理是_____________(用离子方程式表示)。 (2)常温下,取0.2 mol/L HCl溶液与0.2mol/L MOH溶液等体积混合,测得混合后溶液的pH=5。写出MOH的电离方程式:__________。 (3)0.1mol/L的NaHA溶液,测得溶液显酸性。则 ①该溶液中 c(H2A)________c(A2-)(填“>”、“<”或“=”) ②作出上述判断的依据是_______(用文字解释)。 (4)含Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3 mol/L的Cr2O72-。为了使废水的排放达标,进行如下处理: 绿矾为FeSO4• 7H2O。常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的 pH=______。{Ksp[Cr(OH)3]=6.0×10-31} |
|
| 21. 综合题 | 详细信息 |
|
铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4 (1)该蓄电池的负极材料是_________,放电时发生_________(填“氧化”或“还原”)反应。 (2)该蓄电池放电时,电解质溶液的酸性_________(填“增大”、“减小”或“不变”)。 (3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______(用离子方程式表示)。 (4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为H2SO4溶液,则氢氧燃料电池的正极反应式为______________。 |
|
| 22. 填空题 | 详细信息 |
|
连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。 (1)连二次硝酸中氮元素的化合价为_____________________。 (2)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。 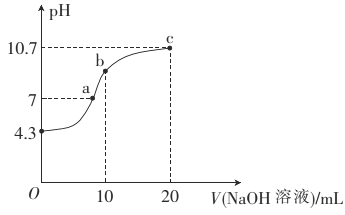 ①写出H2N2O2在水溶液中的电离方程式:______________。 ②b点时溶液中c(H2N2O2)_____(填“>”、“<”或 “=”,下同)c(N2O22-)。 ③a点时溶液中c(Na+)____c(HN2O2-)+c(N2O22-)。 (3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中 |
|
| 23. 综合题 | 详细信息 |
某同学设计一个电池(如下图所示),探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。 (1)通入氢气的电极为________ (填正极或负极),该电极反应式为_______。 (2)石墨电极为________ (填阳极或阴极),乙中总反应离子方程式为________。 (3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_________(填“增大”“减小”或“不变”)。 (4)若甲中消耗0.01molO2,丙中精铜增重_________g。 |
|
最近更新



