黑龙江省大庆市东风中学2020-2021年高一上册期末教学质量检测化学在线测验完整版
| 1. 选择题 | 详细信息 |
|
我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,撒盐可以起到凝血作用,其化学原理涉及胶体的( ) A.丁达尔效应 B.电泳 C.聚沉 D.渗析 |
|
| 2. 选择题 | 详细信息 |
|
下列各组中的离子能在溶液中大量共存的是( ) A.H+、Ca2+、Cl-、 B.K+、Na+、OH-、Cl- C.Na+、Cu2+、 D.Fe3+、Ba2+、Cl-、 |
|
| 3. 选择题 | 详细信息 |
|
下列电离方程式书写正确的是: A.H2SO4=H C.NaOH=Na++O2-+H+ D.Na3PO4=3Na++PO |
|
| 4. 选择题 | 详细信息 |
|
影响1mol气体所占体积大小的主要因素 A.分子直径的大小 B.分子间距离的大小 C.分子间作用力的大小 D.分子数目的大小 |
|
| 5. 选择题 | 详细信息 |
|
2019年是国际化学元素周期表150周年。下列关于元素周期表的说法正确的 A.ⅠA、IIA族的元素全部是金属元素,均能与酸发生反应生成氢气 B.元素周期表包含7个周期、7个主族、7个副族、1个Ⅷ族、1个零族 C.现代元素周期表是按照相对原子量的大小顺序进行对元素进行排列 D.零族元素中所有原子的最外层电子数都是8个,化学性质稳定 |
|
| 6. 选择题 | 详细信息 |
|
下列有关化学用语表示正确的是 A.氯原子的结构示意图: B.铀(U)原子 C.溴原子 D.硫离子的结构示意图: |
|
| 7. 选择题 | 详细信息 |
|
将一小块绿豆大的钠放入滴有酚酞的适量水中,不可能出现的现象是 A.钠浮于水面 B.钠熔成小球 C.钠静止不动 D.溶液变红 |
|
| 8. 选择题 | 详细信息 |
|
每年10月23日上午6︰02到下午6︰02被誉为“摩尔日”(MoleDay),设NA为阿伏伽德罗常数的值,下列说法正确的是 A.3L 0.4mol·L-1 KCl溶液中Cl-物质的量浓度是1.2mol·L-1 B.1molOH-的质量等于17 C.标况下1mol乙醇的体积为22.4L D.2molH2O的摩尔质量为18g·mol-1 |
|
| 9. 选择题 | 详细信息 |
关于以下四个实验相关说法正确的是( )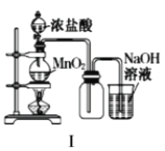 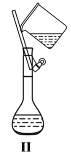  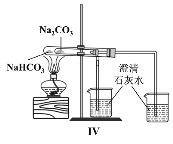 A.图Ⅰ是实验室制备氯气,其中盛装浓盐酸的仪器是长颈漏斗 B.图Ⅱ是配制溶液时向容量瓶中转移溶液的操作 C.图Ⅲ 铜在氯气中燃烧,产生棕黄色的烟 D.图Ⅳ 用于验证碳酸钠和碳酸氢钠的稳定性 |
|
| 10. 选择题 | 详细信息 |
|
下列关于钠的化合物的说法中不正确的是 ①溶解性:Na2CO3>NaHCO3 ②在Na2CO3与NaHCO3混合溶液中滴加少量稀盐酸,则稀盐酸先与NaHCO3反应 ③钠蒸气充入灯泡中制成钠灯,常用于公路照明 ④Na2O和Na2O2晶体中阴、阳离子的数目比不相同 ⑤分别向Na2CO3和NaHCO3的水溶液中滴加BaCl2稀溶液,均可产生白色沉淀 A.②④⑤ B.①②④ C.②③⑤ D.③④⑤ |
|
| 11. 选择题 | 详细信息 |
|
《本草图经》在“绿矾”项载:“盖此矾色绿,味酸,烧之则赤……”,下列关于“绿矾”的说法正确的是 A.绿矾的主要成分为Fe2(SO4)3·7H2O B.绿矾的溶液中能电离出H+,所以“味酸” C.“烧之则赤”时,绿矾被氧化 D.可以用KSCN溶液检验绿矾是否已经全部变质 |
|
| 12. 选择题 | 详细信息 |
铁与水蒸气反应的实验装置如图,下列说法正确的是( )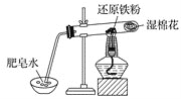 A.实验时,试管口应高于试管底 B.加热时试管内生成黑色物质,点燃肥皂泡可听到爆鸣声 C.反应的化学方程式为2Fe+3H2O(g) D.试管中发生化合反应 |
|
| 13. 选择题 | 详细信息 |
|
黑火药爆炸反应的化学方程式为:2KNO3+S+3C A.该反应的氧化剂是 KNO3,还原剂为 S 和 C B.氧化剂与还原剂的物质的量之比为 1:1 C.氧化产物只有 CO2,还原产物只有 N2 D.每消耗 0.1molS,反应中共转移电子 0.2mol 电子 |
|
| 14. 选择题 | 详细信息 |
|
X、Y分别代表两种非金属元素,下列不能说明非金属性X比Y强的是( ) A.X的氧化物对应水溶液的酸性比Y的氧化物对应水溶液的酸性强 B.Y-的还原性强于X- C.X的单质X2能将Y的阴离子Y-氧化为Y2 D.X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价 |
|
| 15. 选择题 | 详细信息 |
如图所示,元素周期表中的金属和非金属元素的分界线处用虚线表示。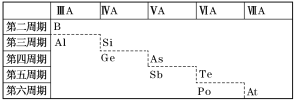 下列说法正确的是( ) A.虚线左下方的元素均为非金属元素 B.紧靠虚线两侧的元素都是具有金属性和非金属性的金属元素 C.可在虚线附近寻找半导体材料(如Ge、Si等) D.可在虚线的右上方,寻找耐高温材料 |
|
| 16. 填空题 | 详细信息 |
|
按要求回答下列问题: (1)有以下几种物质:①铁 ②液态的HCl ③蔗糖 ④酒精 ⑤稀盐酸 ⑥H2SO4 ⑦KOH ⑧熔融的KNO3 ⑨O2 ⑩干冰。试回答(填序号):以上物质能导电的是_______,属于电解质的是_______ (2)写出下列反应的离子方程式: 碳酸钠溶液与足量盐酸:_______ 澄清石灰水与足量盐酸:_______ (3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题: 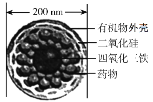 ①“纳米药物分子运输车”分散于水中所得的分散系_______(填“属于”或“不属于”)胶体。 ②从元素组成的角度分析,CO2和Fe3O4可归为同一类物质,其类别属于化合物中的_______ (4)已知反应2F2+2H2O=4HF+O2请用双线桥表示出该反应的电子转移方向和数目_______ (5)计算:①1.5molH2SO4的质量是_______g ②等质量的CO和CO2中氧原子个数之比为_______ |
|
| 17. 实验题 | 详细信息 |
|
健康人体内含铁元素大约 2~3g,人体内铁元素以亚铁离子和三价铁离子的形式存在,Fe2+易被吸收,所以给贫血者补充铁元素时,应补充含 Fe2+的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验: (1)试剂1的名称是_______。 (2)加入新制氯水,溶液中发生反应的离子方程式是_______。 (3)加入试剂2 时溶液为淡红色说明 “速力菲”中的 Fe2+已部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______性。 (4)溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式_______ (5)实验室用下图装置制备并收集干燥纯净的Cl2。 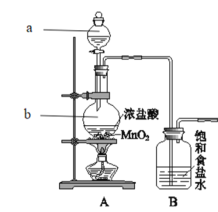 ①装置A中反应的化学方程式是_______ ②装置B的作用是_______ ③向干燥氯气中分别加入一块干燥的有色纸条和一块湿润的有色纸条,观察到的现象为_______ ④Cl2有毒,未反应的Cl2可用NaOH溶液吸收,请写出反应的离子方程式_______ |
|
| 18. | 详细信息 |
|
Q、W、X、Y、Z为短周期元素,Q是原子半径最小的元素,W是地壳中含量最高的元素,X原子的质子数等于Z与Y的质子数之和: Z与Y位于同一周期, Y原子核外最外层电子比次外层多3个电子,非金属Z的一种固体单质可导电。回答下列问题: (1)Y、 Z的元素名称分别为_______、_______ (2)X在周期表中的位置是_______,其离子结构示意图为_______ (3)W元素有多种核素,请写出中子数为10的W元素的一种核素符号_______ (4)X、Y、Z三种元素原子半径由大到小的顺序为_______(填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,写出X单质与氢氧化钠溶液反应的化学方程式 _______ (5)Y和W两种元素形成的最简单的氢化物中,更稳定的是_______(用化学式表示) |
|
| 19. | 详细信息 |
下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒以及有色物质的漂白;化合物G的焰色试验呈黄色,化合物F通常状态下呈气态。请回答下列问题。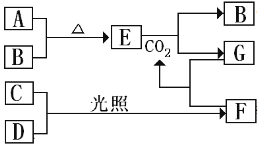 (1)写出B和G的化学式: B_______;G_______ (2)向饱和的G的溶液中通入足量CO2,会出现的现象是_______,有关反应的化学方程式为_______ (3)生活中大多使用漂白粉漂白物质,请用化学方程式解释漂白粉的漂白原理_______ (4)设计实验方案检验F溶液中阴离子_______ (5)实验室欲配制460mL0.100mol/L的G溶液,现有下列仪器:烧杯、100mL量筒、药匙、玻璃棒、天平,还缺少的仪器是_______,应用托盘天平称取固体G的质量为_______。 |
|
最近更新



