2017湖北高一下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
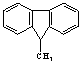
下列有关化用语表示正确的是( ) A.乙酸的结构 C.比例模型 |
|
| 2. | 详细信息 |
|
下列有关物质的性质与应用不相对应的是( ) A.明矾能水解生成Al(OH)3胶体,可用作净水剂 B.FeCl3溶液能与Cu反应;可用于蚀刻印刷电路 C.SO2具有氧化性,可用于漂白纸浆 D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
|
| 3. | 详细信息 |
|
设NA表示阿伏加德罗常数的值。下列说法正确的是( ) A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA B.常温常压下,18 g H2O中含有的原子总数为3NA C.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
|
| 4. | 详细信息 |
|
短周期元素W、X、Y、Z的原子序数依次增大。m、n、p、r是由W、X、Z这三种元素组成的二元化合物。其中m、p具有漂白性;q是元素Z形成的黄色单质;X与Z位于同主族;在第三周期中Y元素所形成的简单离子半径最小。上述物质在常温下的转化关系如图所示,下列说法不正确的是( ) A.工业上常用电解Y的熔融盐的方法制备Y的单质 B.Z的最高价氧化物的水化物为强酸 C.以上四种元素形成的简单离子中,Z离子半径最大 D.m与p可以发生化合反应 |
|
| 5. | 详细信息 | ||||||||||
|
已知反应2X(g)+Y(g)⇌2Z(g),某研究小组将4molX和2molY置于一容积不变的密闭容器中,测定不同时间段内X的转化率,得到的数据如下表,下列判断正确的是( )
A.随着反应的进行,混合气体的密度不断增大 B C.6min时,容器中剩余1.4molY D.其他条件不变,将X的物质的量改为10mol,则可得4molZ |
|||||||||||
| 6. | 详细信息 | ||||||||||||||
|
一定温度下,10mL0.40mol/LH2O2溶液发生
下列说法不正确的是(溶液体积变化忽略不计)( ) A.0~6min的平均反应速率v(H2O2)≈0.033 mol/(L·min) B.6~10min的平均反应速率v(H2O2) <0.033 mol/(L·min) C.反应至6min时,c(H2O2)=0.30 mol/L D.反应至6min时,H2O2分解了50% |
|||||||||||||||
| 7. | 详细信息 |
|
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,下列说法不正确的是( ) A.O2在电极b上发生还原反应 B.反应消耗的NH3与O2的物质的量之比为4:5 C.溶液中OH-向电极a移动 D.负极的电极反应式为2NH3+6OH--6e-=N2+6H2O |
|
| 8. | 详细信息 |
|
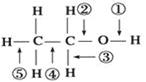
乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
B. 在铜催化共热下与O2反应时断裂①和③ C. 在浓硫酸催化共热下与醋酸反应时断裂② D. 在空气中完全燃烧时断裂①②③④⑤ |
|
| 9. | 详细信息 |
|
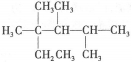
烷烃 A. 4种 B. 5种 C. 6种 D. 7种 |
|
| 10. | 详细信息 |
|
甲苯( A.4种 B.5种 C.6种 D.7种 |
|
| 11. | 详细信息 |
|
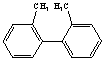
下列说法正确的是( ) A. B.CH3CH=CHCH3分子中的四个碳原子在同一直线上 C.按系统命名法,化合物 D. |
|
| 12. | 详细信息 |
|
乙酸乙酯的同分异构体(只考虑含有一种官能团)的种类数为( ) A.5种 B.6种 C.7种 D.8种 |
|
| 13. | 详细信息 |
|
两种气态烃以某种比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中不符合此条件的是( ) A.CH4、C2H4 B.CH4 、C3H6 C.C2H4、C3H4 D.C2H2、C3H6 |
|
| 14. | 详细信息 |
|
现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是( A. |
|
| 15. | 详细信息 |
|
下列分子中的14个碳原 A. |
|
| 16. | 详细信息 |
|
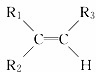
烯烃在一定条件下发生氧化反应,碳碳双键断裂,如:R1CH═CHR2,被氧化为 A.2种 B.3种 C.4种 D.6种 |
|
| 17. | 详细信息 |
|
Ⅰ、现有下列9种微粒: (1) (2)互为同素异形体的微粒是____________。 Ⅱ、已知A、B、C、D均为短周期元素,它们的原子序数依次增大。A是原子最外层有一个电子的非金属元素,C原子的最外层电子数是次外层电子数的3倍;C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。A、B、C三种元素可形成离子化合物,该化合物中各元素原子的物质的量之比为n(A)∶n(B)∶n(C)=4∶2∶3。请回答下列问题: (1)写出C和D形成的淡黄色固体化合物的电子式:___________。 (2)各元素原子的物质的量之比为n(A)∶n(B)∶n(C)=4∶2∶3的化合物的名称为________。 (3)请写出与A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的粒子的符号(举两例)______、_____。 (4)写出由B、C元素组成的元素原子质量比为n(B)∶n(C)=7∶12的化合物的化学式___ |
|
| 18. | 详细信息 |
|
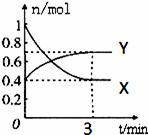
2NO2(g)(红棕色)⇌N2O4(g)(无色),如图所示. (1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。 (2)若降低温度,则v(正) , v(逆) 。 (填“加快”或“减慢”或“不变”) 。 (3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)= 0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快。 (4)在0到3min中内N2O4的反应速率为 。 (5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ; A.v(NO2)=2v(N2O4)B.容器内压强不再发生变化 C.X的体积分数不再发生变化 D.容器内气体原子总数不再发生变化 E.相同时间内消耗n mol的Y的同时生成2n mol的X |
|
| 19. | 详细信息 |
|
(1)写出该烃的分子式 。 (2)该烃的一氯代物是否有同分异构体 。 (3)该烃的四氯代物有多 (4)该烃的同分异构体有多种,其中1种不能使酸性高锰酸钾溶液或溴水褪色,但在一定条件下能跟 液溴、氢气等发生反应,这种同分异构体的结构简式是 。请写出该同分异构 体与氢气、液溴反应的化学方程式并注明反应类型 , , 。
(1)A的摩尔质量是 。 (2)A、B化学式分别为 、 , A、B互 为 。 (3)A分子中碳原子 在一条直线上(填“可能”、“一定”、“一定不”); A分子的二氯代物有 (填数目)种。 |
|
| 20. | 详细信息 |
|
已知A是常用来衡量一个国家石油化工发展水平的标志性物质,A、B、C、D、E、F、G均为有机物,他们之间有如图转化关系,请回答下列问题:
(1)写出A中官能团的名称:A , B中官能团的电子式B 。 (2)在F的同系物中最简单的有机物的空间构型为 。 (3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的物质的结构简式: 。 (4)写出下列编号对应反应的化学方程式,并注明反应类型: ④ , 反应 ; ⑦ , 反应 。 |
|
| 21. | 详细信息 |
|
有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某教师设计了如下图装置(夹持装置仪器已省略),其实验操作为:先按图连接好装置并检查装置的气密性,再关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏地(间歇性)通入气体,即可在M处观察到明显的实验现象。试回答以下问题: (1)A中发生反应的化学方程式是___________,B的作用是___________;C中热水的作用是_________ 。(2)实验过程中铜网出现红色和黑 (3)若试管F中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有 ,要除 |
|


 D.
D.