福建省厦门双十中学2020届高三上期第二次月考化学在线考试题免费练习
| 1. 选择题 | 详细信息 |
|
2019年北京园艺会主题是“绿色生活,美丽家园”。下列有关园艺会说法正确的是( ) A. 大会交通推广使用的是利用原电池原理制成太阳能电池汽车,可减少化石能源的使用 B. 妫汭剧场里使用的建筑材料第五形态的碳单质——“碳纳米泡沫”,与石墨烯互为同分异构体 C. 传统烟花的制作常加入含有铂、铁、钾、钙、铜等金属元素的发光剂,燃放时呈现美丽的颜色,大会庆典禁止使用 D. 秸秆经加工处理成吸水性的材料——植物纤维,可用作食品干燥剂,符合大会主题 |
|
| 2. 选择题 | 详细信息 |
|
化学与生活紧密联系在一起,下列说法正确的是 ①天然气、瓦斯等气体及面粉、煤粉等固体粉尘都容易发生爆炸 ②医院里的血液透析利用了胶体的性质 ③青铜是我国使用最早的合金 ④2019年9月25日发射“云海一号卫星”中使用的碳纤维,是一种新型无机非金属材料 ⑤二氧化硫可用于杀菌、消毒 ⑥金属的冶炼、电镀、钢铁的锈蚀、制玻璃均发生氧化还原反应 A.①②③④⑤ B.①②⑤ C.②⑤⑥ D.①③④ |
|
| 3. 选择题 | 详细信息 | ||||||||||||||||||||
下列各组粒子在溶液中可以大量共存,且加入或通入试剂X后,发生反应的离子方程式也正确的是
|
|||||||||||||||||||||
| 4. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的数值,下列有关说法正确的是 A.标准状况下,22.4L Cl2通入水中,HClO、Cl-、ClO-的粒子数之和为2NA B.1 molAlCl3在熔融状态时含有的离子总数为0.4NA C.标准状况下,22.4 L CO2中所含的电子数目为16NA D.60 g乙酸和葡萄糖混合物充分燃烧消耗O2分子数为2NA |
|
| 5. 选择题 | 详细信息 |
|
下列关于有机物的说法中不正确的是 A.苯与氯气在一定条件下可发生取代反应 B.塑料、纤维都是合成高分子材料 C.乙烯、氯乙烯均可使酸性高锰酸钾溶液褪色 D.油脂、纤维素和蛋白质在一定条件下都能发生水解反应 |
|
| 6. 选择题 | 详细信息 |
|
a、b、c、d四种元素的原子序数依次增大,均为短周期元素,a、c同主族,a的最外层电子数是内层电子数的3倍,b为金属元素,a、c、d的最外层电子数之和为19。下列叙述正确的是 A.a、b可能形成含有共价键的离子化合物 B.简单离子半径大小:d>c>a>b C.含氧酸的酸性强弱:d>c D.b、c的简单离子在水溶液中一定能大量共存 |
|
| 7. 选择题 | 详细信息 |
|
高温高压液态水具有接近常温下弱酸的c(H+)或弱碱的c(OH−),油脂在其中能以较快的反应速率水解。与常温常压水相比,下列说法不正确的是 A. 高温高压液态水中,体系温度升高,油脂水解反应速率加快 B. 高温高压液态水中,油脂与水的互溶能力增强,油脂水解反应速率加快 C. 高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生的酸进一步催化水解 D. 高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同c(H+)的酸或相同c(OH−)的碱的水解 |
|
| 8. 选择题 | 详细信息 |
塑剂DCHP可由环己醇制得。环己醇和DCHP的结构简式如图所示,下列说法中正确的是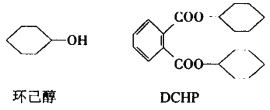 A.DCHP的分子式为C20H24O4 B.环己醇和DCHP的一氯代物均有4种 C.1molDCHP水解时消耗2mol NaOH D.环己醇分子中的所有碳原子可能共平面 |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
下列关于各图的叙述正确的是 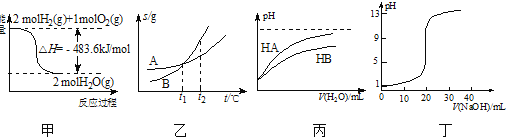 A.A.甲表示 B.乙表示A、B两物质的溶解度随温度变化情况,将 C.丙表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度NaB溶液的pH D.丁表示 |
|
| 11. 选择题 | 详细信息 |
氯化镁晶体具有如下转化关系: 下列说法错误的是 A.固体I可溶于饱和NH4Cl溶液 B.气体I能使无水CuSO4变蓝色 C.溶液I和溶液Ⅱ常温下均能与Cu反应 D.在固体Ⅱ的浊液中加入KI溶液可产生黄色沉淀 |
|
| 12. 选择题 | 详细信息 | ||||||||||||
下列实验装置设计正确,且能达到目的的是
|
|||||||||||||
| 13. 选择题 | 详细信息 |
|
某化学兴趣小组进行两组电解实验。 实验一:已知固体电解质只有特定离子才能移动。按照下图装置研究α-AgI固体电解质导体是Ag+导电还是I-导电; 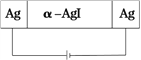 实验二:用惰性电极电解硫酸铜和盐酸混合液,对产生的气体进行研究。 关于以上实验,下列说法正确的是 A. 实验一:若α-AgI固体是Ag+导电,则通电一段时间后的晶体密度不均匀 B. 实验一:若α-AgI固体是I-导电,则通电一段时间后的晶体密度仍均匀 C. 实验二:若阳极为纯净气体,阴、阳两极产生的气体体积比可能≥1 D. 实验二:若阳极为混合气体,阴、阳两极产生的气体体积比可能≥1 |
|
| 14. 选择题 | 详细信息 | ||||||
将SO2分别通入无氧、有氧的浓度均为0.1 mol·L-1的 BaCl2溶液和Ba(NO3)2溶液中,探究体系中微粒间的相互作用,实验记录如下:
|
|||||||
| 15. 选择题 | 详细信息 |
向1000 mL 3mol/LNaOH中通入适量CO2气体,溶液中有关阴离子的物质的量变化曲线如图所示: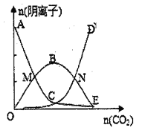 下列说法正确的是 A.CD段反应的离子方程式为OH-+CO2=HCO B.水的电离程度先增大后减小 C.溶液的pH先减小后增大 D.M、N两点对应的溶液中离子种类不同 |
|
| 16. 选择题 | 详细信息 |
如图,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由B向左移动,当移至C处时容器体积缩小至最小,为原体积的9/10,随着CO2的继续通入,活塞又逐渐向右移动。下列说法中正确的是( )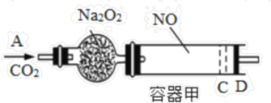 A.活塞从D处移动到C处的过程中,通入的CO2气体为2.24L(标准状况) B.NO2转化为N2O4的转化率为20% C.容器甲中NO已反应完 D.活塞移至C处后,继续通入a molCO2,此时活塞恰好回至D处,则a小于0.01 |
|
| 17. | 详细信息 |
硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下: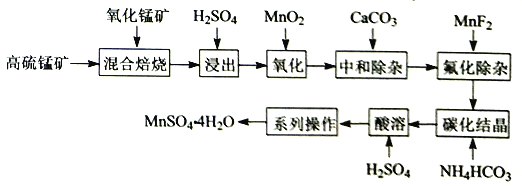 已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。 ②金属离子在水溶液中的平衡浓度与pH的关系如图所示(25℃): 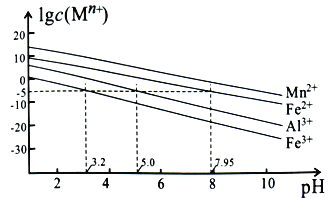 ③此实验条件下Mn2+开始沉淀的pH为7.54;离子浓度≤10-5mol·L-1时,离子沉淀完全。 请回答: (1)传统工艺处理高硫锰矿时,不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为___________。 (2)“氧化”时,发生反应的离子方程式为_________________________________。若省略“氧化”步骤,造成的后果是_________________________________。 (3)“中和除杂”时,生成沉淀的主要成分为______________________(填化学式)。 (4)“氟化除杂”时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于___________。(已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12) (5)“碳化结晶”时,发生反应的离子方程式为______________________。 (6)“系列操作”指___________、过滤、洗涤、干燥 (7)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为___________。 |
|
| 18. 实验题 | 详细信息 | ||||||||||||||||||||
|
叠氮化钾( I.制备 步骤1:制备亚硝酸丁酯( 反应装置如图1(夹持装置略去),向烧杯中依次加入稀硫酸、丁醇、亚硝酸钠溶液,待反应完全后,分离出上层油状物,用 步骤2:制备叠氮化钾 反应装置如图2(夹持及加热装置路去),向仪器A中加入 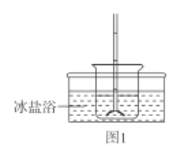  相关物质性质如下:
|
|||||||||||||||||||||
| 19. 实验题 | 详细信息 |
三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2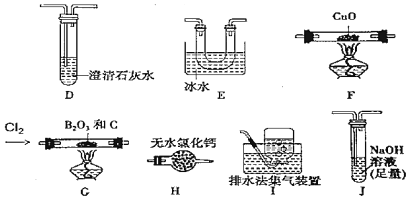 实验Ⅰ:制备BCl3并验证产物CO (1)该实验装置中合理的连接顺序为G→______→______→______→______→F→D→I;其中装置E的作用是______。 (2)BCl3接触潮湿空气时会形成白雾,请写出该反应的化学方程式______。 (3)能证明反应中有CO生成的现象是______。 实验Ⅱ:产品中氯含量的测定 ①准确称取少许m g产品,置于蒸馏水中完全水解,并配成100 mL溶液。 ②取10.00 mL溶液于锥形瓶中 ③加入V1 mL浓度为c1mol/L AgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。 ④以硝酸铁为指示剂,用c2 mol/LKSCN标准溶液滴定过量的AgNO3溶液。重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。 已知:Ksp(AgCl)>Ksp(AgSCN)。 (4)步骤②移取溶液时所需仪器名称为______,步骤④中达到滴定终点的现象为______。 (5)产品中氯元素的质量分数为______。 (6)下列操作,可能引起测得产品中氯含量偏高是______。 A.步骤③中未加硝基苯 B.步骤①中配制100 mL溶液时,定容时俯视刻度线 C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡 D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴 |
|
| 20. | 详细信息 |
|
环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下: 解聚反应:  氢化反应: 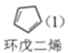 +H2(g) +H2(g)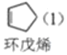 ,△H=-100.5 kJ/mol ,△H=-100.5 kJ/mol副反应: 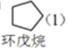 ,△H=-109.4 kJ/mol ,△H=-109.4 kJ/mol回答下列问题: (1)反应 (2)解聚反应在刚性容器中进行。 ①其他条件不变,有利于提高双环戊二烯平衡转化率的条件是________(填标号)。 A 升高温度 B 降低温度 C 增大压强 D 减小压强 ②实际生产中常常以通入水蒸气以降低双环戊二烯的沸点。某温度下,若通入总压为100 kPa的双环戊二烯和水蒸气,测得达到平衡后总压为160 kPa,双环戊二烯的转化率为80%,则p(H2O)=____kPa,平衡常数Kp=_____kPa(Kp为以分压表示的平衡常数)。 (3)一定条件下,将环戊二烯溶于有机溶剂中进行氢化反应,反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如下图所示。 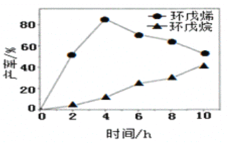 ①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是______。 ②最佳的反应时间为____h。活化能较大的是_____(填“氢化反应”或“副反应")。 (4)已知氢化反应平衡常数为1.6×1012,副反应的平衡常数为2.0×1012,在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,则环戊二烯的含量随时间变化趋势是_________(不考虑环戊二烯的二聚反应)。 |
|