贵州省2020年普通高等学校招生适应性测试理综化学
| 1. 选择题 | 详细信息 |
|
化学品在抗击新型冠状病毒的战役中发挥了重要作用。下列说法不正确的是( ) A.医用防护口罩中熔喷布的生产原料主要是聚丙烯,聚丙烯的单体是丙烯 B.“84”消毒液的主要成分是次氯酸钠 C.用硝酸铵制备医用速冷冰袋是利用了硝酸铵溶于水快速吸热的性质 D.75%的医用酒精常用于消毒,用95%的酒精消毒效果更好 |
|
| 2. 选择题 | 详细信息 |
|
己知NA是阿伏加德罗常数的值。下列说法正确的是( ) A.1molOD-中含有的质子数和中子数均为9NA B.60g正戊烷与12g新戊烷的混合物中共价键数为17NA C.11.2L氯气与足量镁粉充分反应,转移的电子数为NA D.1L0.1mo1·L-1CH3COONa溶液中,CH3COO-数目为0.1NA |
|
| 3. 选择题 | 详细信息 |
|
两个单环共用一个碳原子的多环化合物称为螺环化合物,共用的碳原子称为螺原子。螺[5,5]十一烷的结构为 A.一溴代物有三种 B.与十一碳烯互为同分异构体 C.分子中所有碳原子不可能在同一平面 D.1mo1该化合物完全燃烧需要16mo1O2 |
|
| 4. 选择题 | 详细信息 |
短周期元素X、Y、Z、W的原子序数依次增大,Y与W同族,W的核电荷数是Y的两倍,四种元素组成的一种化合物如图所示。下列说法一定正确的是( )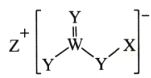 A.简单离子半径:Z>W>Y>X B.最简单氢化物的稳定性:W>Y C.X与Z可形成离子化合物ZX D.W的氧化物对应的水化物为强酸 |
|
| 5. 选择题 | 详细信息 |
|
利用如图的实验装置和方法进行实验,能达到目的的是( ) A.甲装置可将FeC12溶液蒸干获得FeC12晶体 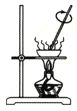 B.乙装置可证明浓硫酸具有脱水性和氧化性  C.丙装置可除去CO2中的SO2 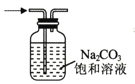 D.丁装置可将NH4Cl固体中的I2分离 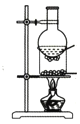 |
|
| 6. 选择题 | 详细信息 |
某锂离子电池充电时的工作原理如图所示,LiCoO2中的Li+穿过聚内烯微孔薄膜向左迁移并嵌入石墨(C6表示)中。下列说法错误的是( ) A.充电时,阳极电极反应式为LiCoO2-xe-=xLi++Lil-xCoO2 B.放电时,该电池将化学能转化为电能 C.放电时,b端为负极,发生氧化反应 D.电池总反应为LixC6+Lil-xCoO2 |
|
| 7. 选择题 | 详细信息 |
实验测得0.1mo1·L-1Na2SO3溶液pH随温度升高而变化的曲线如图所示。将b点溶液冷却至25℃,加入盐酸酸化的BaC12溶液,能明显观察到白色沉淀。下列说法正确的是( )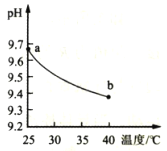 A.Na2SO3溶液中存在水解平衡SO32-+2H2O B.温度升高,溶液pH降低的主要原因是SO32-水解程度减小 C.a、b两点均有c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] D.将b点溶液直接冷却至25℃后,其pH小于a点溶液 |
|
| 8. 实验题 | 详细信息 |
|
ClO2是一种具有强氧化性的黄绿色气体,也是优良的消毒剂,熔点-59℃、沸点11℃,易溶于水,易与碱液反应。ClO2浓度大时易分解爆炸,在生产和使用时必须用稀有气体或空气等进行稀释,实验室常用下列方法制备:2NaC1O3+Na2SO3+H2SO4 (1)H2C2O4可代替Na2SO3制备ClO2,该反应的化学方程式为___,该方法中最突出的优点是___。 (2)ClO2浓度过高时易发生分解,故常将其制备成NaClO2固体,以便运输和贮存。 已知:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O,实验室模拟制备NaC1O2的装置如图所示(加热和夹持装置略)。 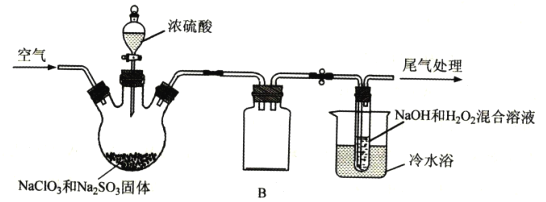 ①产生ClO2的温度需要控制在50℃,应采取的加热方式是___;盛放浓硫酸的仪器为:___;NaC1O2的名称是___; ②仪器B的作用是___;冷水浴冷却的目的有___(任写两条); ③空气流速过快或过慢,均会降低NaC1O2的产率,试解释其原因___。 |
|
| 9. | 详细信息 |
从铜转炉烟灰(主要成分ZnO还有Pb、Cu、Cd、As、Cl、F等元素)中回收锌、铜、铅等元素进行资源综合利用,具有重要意义。以铜转炉烟灰制备重要化工原料活性氧化锌的工艺流程如图所示。 己知:活性炭净化主要是除去有机杂质。 请回答以下问题: (1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为___。 (2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,结合流程图分析,氯化铵适宜的浓度为___ mo1·L-1。 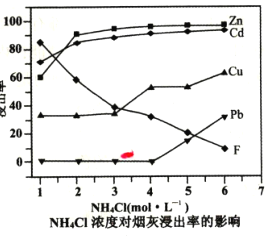 (3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将8.0×10-3mo1•L-1FeC13溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时Ksp(FeAsO4)=2.0×10-22,则反应后溶液中c(AsO43-)=___mo1•L-1。 (4)滤渣II的主要成分为___;除杂3是置换除杂过程,则此过程主要除去的金属有___(填化学式)。 (5)沉锌得到的物质为Zn(NH3)2C12,请写出水解转化的化学方程式___。 (6)该流程中可以循环使用的物质的电子式为___。 (7)取mg活性氧化锌样品,预处理后配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。己知:与1.0mLEDTA标准液[c(EDTA)=1.000mo1•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为___(用代数式表示)。 |
|
| 10. 综合题 | 详细信息 |
|
甲醛(HCHO)俗称蚁醛,在化工、医药、农药等方面有广泛的应用。 I·甲醛的制备 工业上利用甲醇脱氢法制备甲醛,己知:CH3OH(g) (1)该反应的能量变化如图甲所示,△H=___kJ•mol-1。 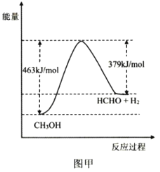 (2)为提高CH3OH转化率,采取的措施有___、___;在温恒容条件下,该反应达到平衡状态的标志有___(填标号)。 a.混合气体的密度保持不变 b.混合气体的总压强保持不变 c.v(CH3OH)消耗=v(H2)生成 d.甲醛的浓度保持不变 (3)选用Ag/SiO2—ZnO作催化剂,在400~750℃区间进行活性评价,图乙给出了甲醇转化率与甲醛选择性(选择性越大,表示生成该物质越多)随反应温度的变化曲线。制备甲醛的最佳反应温度为___(填标号),理由是___。 a.400℃ b.650℃ c.700℃ d.750℃ 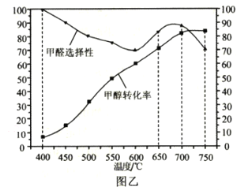 (4)T℃时,在2L恒容密闭容器中充入1mo1甲醇,发生反应: ①CH3OH(g) ②CH3OH(g) 平衡时甲醇为0.2mol,甲醛为0.7mo1。则反应i的平衡常数K=___。 II.甲醛的用途 (5)将甲醛水溶液与硫酸镍(NiSO4)溶液混合,可用于化学镀镍。反应过程中有CO2产生,则该反应的离子方程式为___:若收集到112mLCO2(标准状况),理论上转移电子___ mo1。 |
|
| 11. 综合题 | 详细信息 |
|
元素的性质与原子结构、元素在周期表中的位置有着密切的关系。回答下列问题: (1)如图表示某短周期元素X的前五级电离能(I)的对数值,试推测并写出X的元素符号___。 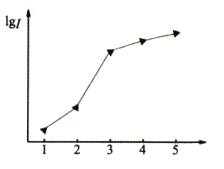 (2)化合物甲与SO2所含元素种类相同,两者互为等电子体,请写出甲的化学式___,甲分子中心原子的杂化类型是___。 (3)配位化学创始人维尔纳发现,将1mo1CoC13·5NH3(紫红色)和1mo1CoC13•4NH3(绿色)溶于水,加入AgNO3溶液,立即沉淀的AgCl分别为2mo1、1mol。则紫红色配合物中配离子的化学式为___,绿色配合物中Co的配位数为___。 (4)某稀土元素M的氧化物晶体为立方晶胞,其结构如图所示,图中小球代表氧离子,大球代表M离子。 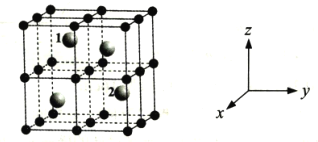 ①写出该氧化物的化学式___。 ②己知该晶体密度为ρg·cm-3,晶胞参数为anm,NA为阿伏加德罗常数的值。则M的相对原子质量Mr=___(用含ρ、a等的代数式表示); ③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1(M原子)的坐标为( |
|
| 12. 推断题 | 详细信息 |
聚酰亚胺是综合性能最佳的有机高分子材料之一,已广泛应用在航空、航天、微电子等领域。某聚酰亚胺的合成路线如图(部分反应条件己略去):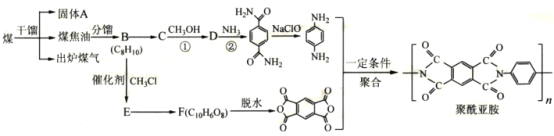 己知下列信息: ①芳香族化合物B的一氯代物有两种 ② 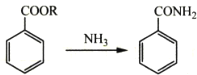 ③ 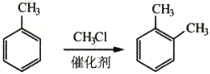 回答下列问题: (1)固体A是___(写名称);B的化学名称是___。 (2)反应①的化学方程式为___。 (3)D中官能团的名称为___;反应②的反应类型是___。 (4)E的分子式为___;己知1mo1F与足量的NaHCO3反应生成4mo1CO2,则F的结构简式是___。 (5)X与C互为同分异构体,写出同时满足下列条件的X的结构简式___。 ①核磁共振氢谱显示四种不同化学环境的氢,其峰面积之比为2:2:1:1 ②能与NaOH溶液反应,1mo1X最多消耗4mo1NaOH ③能发生水解反应,其水解产物之一能与FeC13溶液发生显色反应 (6)参照上述合成路线,以甲苯和甲醇为原料(无机试剂任选)设计合成 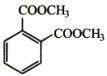 的路线___。 的路线___。 |
|
最近更新



