江西高一化学高考模拟(2019年下册)免费试卷完整版
| 1. 选择题 | 详细信息 |
|
下列情况会对人体健康造成较大危害的是 A.用SO2漂白木耳制成银耳 B.用漂白粉[Ca(ClO)2]稀溶液对餐具进行杀菌消毒 C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) D.用小苏打(NaHCO3)发酵面团制作馒头 |
|
| 2. 选择题 | 详细信息 |
|
X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收.已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种黄绿色气体单质,其水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应.下列说法不正确的是 A.X是SO2,它既有氧化性又有还原性 B.干燥的气体Y不能使干燥的有色布条褪色,其水溶液具有漂泊作用的是HClO C.Z与水反应的化学方程式为:3NO2+H2O=2HNO3+NO D.等物质的量的X与Y同时通入到湿润的有色布条上,有色布条褪色时间变短,漂泊效果增强 |
|
| 3. 选择题 | 详细信息 | |||||||||||||||
化学在生活中有着广泛的应用,下列对应关系错误的是( )
|
||||||||||||||||
| 4. 选择题 | 详细信息 |
|
地壳中含量最多的元素在周期表中的位置是( ) A. 第二周期VIA族 B. 第二周期VA族 C. 第三周期VIA族 D. 第三周期VA族 |
|
| 5. | 详细信息 | ||||||||||||||||||||
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是()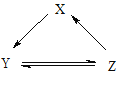
|
|||||||||||||||||||||
| 6. 选择题 | 详细信息 |
如图,A处通入 A. 浓盐酸 B. 饱和NaCl溶液 C. 浓硫酸 D. NaOH溶液 |
|
| 7. 选择题 | 详细信息 | |||||||||||||||
下列有关实验的操作正确的是( )
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
|
下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( ) A. 在空气中敞口久置的浓硫酸,溶液质量增大 B. 在加热条件下铜与浓硫酸反应 C. 蔗糖与浓硫酸反应中有海绵状的炭生成 D. 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色 |
|
| 9. 选择题 | 详细信息 |
|
硅及其化合物应用广泛,下列叙述正确的是( ) A. 硅酸钠可用于制备木材防火剂 B. 水晶项链是硅酸盐制品 C. 光导纤维的主要成分是晶体硅 D. 硅在地壳中主要以游离态形式存在 |
|
| 10. 选择题 | 详细信息 | |||||||||||||||||||||||||||
下列有关SO2性质的探究实验报告记录的实验现象正确的是
|
||||||||||||||||||||||||||||
| 11. 选择题 | 详细信息 |
|
有关元素周期表的说法中错误的是( ) A. 元素周期表中第16个纵行为ⅥA族 B. ⅦA族元素也称为卤族元素 C. 元素周期表中,Ⅷ族包括第8,9,10三个纵行 D. 0族元素的原子最外层电子数均为8,元素化合价为0 |
|
| 12. 选择题 | 详细信息 |
|
实验室制备氨气,检验是否收集满的正确方法是( ) A. 用手扇动收集的气体,有气味则已收集满 B. 将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满 C. 将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满 D. 用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满 |
|
| 13. 选择题 | 详细信息 |
|
下列各组物质相互混合反应后,最终有白色沉淀生成的是 ( ) ①在敞口容器中将金属钠投入到FeC12溶液中 ②向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液 ③向硅酸钠溶液中逐滴加入过量的盐酸 ④向NaAlO2溶液中通入过量CO2 ⑤向饱和Na2CO3溶液中通入过量CO2 A. ①③④⑤ B. 只有①④ C. 只有②③ D. 只有③④⑤ |
|
| 14. 选择题 | 详细信息 |
|
等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是 A. FeO B. Fe2O3 C. FeSO4 D. Fe3O4 |
|
| 15. 选择题 | 详细信息 |
|
将装有60mLNO2、NO混合气体的量筒倒立于水槽中,反应后气体体积缩小为40mL,则混合气体中NO2和NO的体积比是( ) A. 5:3 B. 2:3 C. 1:1 D. 2:1 |
|
| 16. 填空题 | 详细信息 |
(1)已知某元素的原子结构示意图: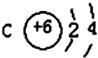 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。(2)已知某元素的原子结构示意图: 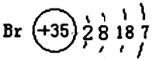 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。 |
|
| 17. 填空题 | 详细信息 |
|
在一支试管里放入一小块铜片,注入一定体积的浓硫酸,再给试管加热,充分反应。 (1)写出反应的化学方程式_________________;若试管中铜片还有剩余,硫酸_________(填“已”或“未”)消耗完毕,其理由是 __________________________; (2)若反应中有0.02molH2SO4被还原,则在标准状况下收集到的气体体积为__________mL,参加反应的铜的质量为____g。 |
|
| 18. 实验题 | 详细信息 |
科学探究的基本程序包括形成问题、建立假设、设计研究方案、检验假设、表达或交流结果等.某同学欲用如图装置可用来探究浓硫酸与木炭粉的加热条件下反应产生的所有气体产物,请填写下列空白: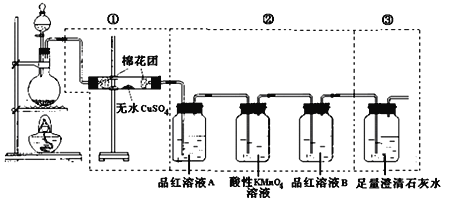 (1)写出木炭粉与浓硫酸反应的化学方程式____________ (2)②中品红溶液A的作用是 ______ .酸性高锰酸钾的作用______品红溶液B的作用是______。 (3)如果将装置中①、②、③三部分仪器的连接顺序改为②、①、③:则可以检出的物质是_____,不能检出的物质是_____ 。 (4)如果将仪器的连接顺序变为①、③、②,则不能检出的物质是 ______。 (5)如果将仪器的连接顺序变为②、③、①,则不能检出的物质是 ______。 |
|
| 19. 推断题 | 详细信息 |
X、Y、Z均为短周期元素组成的物质,其转化关系如下: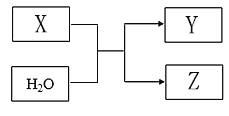 请回答: (1)若X为淡黄色固体,Z是单质。 ①组成Z的元素在周期表中的位置是_____。 ②取少量X与水反应,下列叙述正确的是_____(填字母)。 a.该反应是氧化还原反应 b.向反应后的溶液中滴加酚酞试剂,溶液变红 c.当有1 molX参加反应时,共转移2mol电子 (2)若X由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。Y与X的组成元素相同。 ①X与水反应的化学方程式为_____。 ②X与O2混合通入水中,恰好生成4molZ,则通入的X为____mol,O2为____mol。 |
|
| 20. 填空题 | 详细信息 |
|
有一稀硫酸和稀硝酸的混合溶液,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合液,向其中加入过量的铁粉: 反应过程中发生的离子反应方程式:_______________;____________ 产生的气体的总体积为______ L。 |
|
最近更新




