河北高二上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是 A.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 B.增大压强可加快SO2转化为SO3的速率 C.黄绿色的氯水光照后颜色变浅 D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
|
|
| 2. | 详细信息 | ||||||||||||||||||||
|
将下表中各组的两电极用
|
|||||||||||||||||||||
| 3. | 详细信息 |
|
垃圾处理要遵循三原则,其中不包括 A. 无害化 B. 减量化 C. 资源化 D.白色化
|
|
| 4. | 详细信息 |
|
下列对NaCl的分类正确的是( ) A.混合物 B.化合物 C.氧化物 D.有机物
|
|
| 5. | 详细信息 |
|
一定温度下,反应N2(g)+O2(g) A.缩小体积 B.恒容,充入He C.恒容,充入O2 D.恒压,充入N2
|
|
| 6. | 详细信息 |
|
下列哪些能源属于二次能源( ) A.风力 B.电力 C.原煤 D.流水
|
|
| 7. | 详细信息 |
|
赏心悦目 A.浓硫酸 B.氢氟酸 C.浓硝酸 D.王水
|
|
| 8. | 详细信息 |
|
下列物质在水溶液中的电离方程式错误的是( ) A.Na2CO3= 2Na+ + CO32- B.NaHSO4= Na+ + H+ + SO42- C.KOH= K+ + O2- + H+ D.H2SO4= 2H+ + SO42-
|
|
| 9. | 详细信息 |
|
实验室用溴和苯反应制溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10% NaOH溶液润洗;⑤水洗。正确的操作顺序是( ) A.①②③④⑤ B.②④⑤③① C.④②③①⑤ D.②④①⑤③
|
|
| 10. | 详细信息 |
|
容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度 ② 浓度 ③容量 ④ 压强 ⑤刻度线 ⑥酸式或碱式这六项中的 A.②④⑥
|
|
| 11. | 详细信息 |
|
下列试剂中,能用于检验酒精中是否含有水的是( ) A、CuSO4·5H2O B、无水硫酸铜 C、浓硫酸 D、金属钠
|
|
| 12. | 详细信息 |
|
下列表述中正确的是 A.NH B.分馏、干馏、裂化都是化学变化 C.2—甲基—1—丁烯的结构简式: D.NaHSO4和Na2O2的阴、阳离子个数比均为1:2
|
|
| 13. | 详细信息 |
|
.如图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法错误的是 A.铜片表面有气泡生成 B.装置中存在“化学能→ 电能→ 光能”的转换 C.如果将硫酸换成柠檬汁,导线中不会有电子流动 D.如果将锌片换成铁片,电路中的电流方向不变
|
|
| 14. | 详细信息 |
|
某同学在所收到的信封上发现有收藏价值的邮票,便将邮票剪下来浸入水中,以去掉邮票背面的黏合剂。根据“相似相溶”原理,该黏合剂的成分可能是
|
|
| 15. | 详细信息 |
|
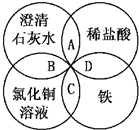
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子方程式书写正确的是
A.OH-+HCl═H2O+Cl - B.Ca(OH)2+Cu2+═Ca2++Cu(OH)2 C.Fe+Cu2+═Cu+Fe2+ D.Fe+2H+═Fe3++H2↑
|
|
| 16. | 详细信息 |
|
下列离子或分子在指定的分散系中一定能够大量共存的是( ) A.c(H+)=10-13 mol/L的溶液中:NO3-、SO42-、K+、Na+ B.含Fe3+的溶液中中: Na+、K+、CH3COO-、HCO3- C.铁与过量稀硫酸反应后的溶液中:[Al(OH)4]-、NH4+、Cl-、NO3- D.空气中:SO2、NO、N2、NH3
|
|
| 17. | 详细信息 |
|
对于4℃时,水中溶解了22.4L HCl气体(标准状况下测得)后形成的溶液200mL,下列说法中正确的是 A.该溶液物质的量浓度为10mol/L B.所用水的体积为177.6L C.根据题干数据,该溶液物质的量浓度无法求得 D.该溶液中溶质的质量分数因溶液的密度未知而无法求得
|
|
| 18. | 详细信息 |
|
某温度下,在固定容积的容器中,可逆反应A(g)+3B(g) A. 刚充入时反应速率υ正减少,υ逆增大 B. 平衡不发生移动 C. 平衡向逆反应方向移动 D. 物质C的质量分数增大
|
|
| 19. | 详细信息 |
|
下列有关物质的应用与性质相对应的说法正确 ①明矾能用于净水是因为 ②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜 ③浓硫酸可用作干燥剂是因为其具有脱水性 ④光导纤维可用作通讯材料是因为其具有导电性 ⑤MgO、Al2O3的熔点很高,可制作耐高温材料 ⑥NaHCO3能与碱反应,因此食品工业上用作焙制糕点的膨松剂 ⑦Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 A.3个 B.2个 C.5个 D.4个
|
|
| 20. | 详细信息 |
|
.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( ) A.甲烷的结构式:CH4 B.NH4Cl的电子式: C.苯的实验式:CH D.乙烯的结构简式:C2H4
|
|
| 21. | 详细信息 |
|
一定条件下硝酸铵受热 A.5:3 B.5:4 C.1:1 D.3:5
|
|
| 22. | 详细信息 |
|
下列叙述正确的是( ) A.随着元素原子序数的递增,原子最外层电子数总是从 1~8 重复出现 B.随着原子序数的递增,元素的最高正化合价从+1到+7,负价从﹣7到﹣1重复出现 C.第3周期中,随着核电荷数的递增,元素的离子半径依次减小 D.随核电荷数递增,ⅦA族元素单质熔、沸点升高,碱金属元素单质熔、沸点降低
|
|
| 23. | 详细信息 |
|
下列溶液中c(Cl—)与150mL 1mol/L NaCl溶液中c(Cl—)相等的是 A.50mL 3mol/L KCl溶液 B.75 mL 2mol/L CaCl2溶液 C.100 mL 0.5mol/L BaCl2溶液 D.50mL 1mol/L AlCl3溶液
|
|
| 24. | 详细信息 |
|
下列有关物质的性质或应用均正确的是 A.二氧化硅为酸性氧化物,可用于制做计算机芯片 B.铜的金属活泼性比铁差,可在海轮外壳上装若干铜块以减缓其腐蚀 C.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 D.浓硫酸具有脱水性,可
|
|
| 25. | 详细信息 |
|
将适量的SO2通入Fe(NO3)3中,溶液逐渐由棕黄色变为浅绿色,但又立即变为棕黄色,继续滴入BaCl2溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的元素是( ) A.S B.Fe C.Cl D.N
|
|
| 26. | 详细信息 |
|
设NA表示阿伏加德罗常数的数值,下列叙述正确的是( ) A.物质的量浓度为0.5 mol·L-1 (NH4)2SO4溶液中,含有NH4
C.3.9gNa2O2晶体中阴阳离子总数为0.2NA D.含4molHCl的浓盐酸和足量MnO2加热反应可生成Cl2分子少于NA个
|
|
| 27. | 详细信息 |
|
分子式C9H10O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体有(不考虑立体异构) A.12种 B.13种 C.14种 D.15种
|
|
| 28. | 详细信息 |
|
在含有FeCl3、FeCl2、AlCl3、NaCl的溶液中,加入足量的NaOH溶液,在空气中充分搅拌,反应,再加入过量的稀盐酸,溶液中离子数目减少的是( ) A.Na+
|
|
| 29. | 详细信息 |
|
被称之为“软电池”的纸质电池总反应为Zn+2MnO2+H2 A.该电池中Zn作负极,发生还原反应 B.该电池反应中MnO2起催化作用 C.该电池工作时电流由Zn经导线流向MnO2 D.该电池正极反应式为:MnO2+e-+H2O=MnOOH+OH-
|
|
| 30. | 详细信息 |
|
甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙十丁→沉淀;乙+丁→无色无味气体。则甲、乙、丙、丁四种溶液依次是 A.BaCl2 、Na2CO3、盐酸 、AgNO3 B.BaCl2 、Na2CO3、、AgNO3 、盐酸 C.Na2CO3、 盐酸 、AgNO3、 BaCl2 D.AgNO3、盐酸、 BaCl2、Na2CO3
|
|
| 31. | 详细信息 |
|
现有含CuSO4和H2SO4的混合溶液200mL,其中CuSO4物质的量浓度为1mol·L-1, H2SO4物质的量浓度为0.5mol·L-1,若向此溶液中加入一定量浓硫酸,使其配成含0.2mol·L-1 CuSO4和2mol·L-1 H2SO4的混合溶液,试求: (1)所得溶液的体积是多少毫升? (2)需加入密度为1.84g/cm3、质量分数为98%的浓硫酸多少毫升?(小数点后保留1位)
|
|
| 32. | 详细信息 |
|
向一定量的NaOH固体中加入由硫酸铜和硫酸组成的混合物的溶液,充分搅拌,恰好完全反应,有蓝色沉淀生成,过滤,所得滤液的质量与加入的原混合物溶液的质量相等。则与硫酸铜反应的氢氧化钠和与硫酸反应的的氢氧化钠的物质的量之比为?
|
|