南充市高三化学下册专题练习模拟考试练习
| 1. 选择题 | 详细信息 |
|
食品检验是保证食品安全的重要措施,下列不属于食品安全检测指标的是( ) A.淀粉的含量 B.二氧化硫的含量 C.亚硝酸盐的含量 D.甲醛的含量 |
|
| 2. 选择题 | 详细信息 |
|
2006年12月1日为世界第19个艾滋病日,联合国艾滋病规划署确定的宣传主题是“遏制艾滋,履行承诺”。医学界通过用放射性14C标记的C60,发现C60的羧酸衍生物在特定条件下可断裂DNA杀死细胞,抑制艾滋病。关于14C的下列说法中正确的是( ) A.14C原子与C60中普通碳原子的化学性质不同 B.14C原子与14N原子所含中子数相同 C.是C60的同素异形体 D.与12C、13C是碳元素的三种同位素 |
|
| 3. 选择题 | 详细信息 |
|
下列化学式既能表示物质的组成,又能表示物质的一个分子的是( ) A. NaOH B. SiO2 C. Fe D. C3H8 |
|
| 4. 选择题 | 详细信息 |
|
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是 A. CO2的电子式  C. 乙烯的结构简式 C2H4 D. 质量数为37的氯原子 |
|
| 5. 选择题 | 详细信息 |
|
下列金属冶炼的反应原理,错误的是( )。 A.2NaCl(熔融) B.MgO+H2 C.Fe3O4+4CO D.2HgO |
|
| 6. 选择题 | 详细信息 |
|
下列各组离子在指定的环境中一定能大量共存的是( )。 A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- B.含有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I- C.加入铝粉能产生H2的溶液:NH4+、Fe2+、SO42-、NO3- D.含有大量ClO-的溶液:H+、Mg2+、I-、SO42- |
|
| 7. 选择题 | 详细信息 |
|
若NA表示阿伏加德罗常数,下列叙述中正确的是 ( ) A.标准状况下,22.4L SO3含NA个分子 B.含0.4mol HCl的浓盐酸与足量二氧化锰反应转移电子数为0.2NA C.32gCu与足量硫完全反应,转移的电子数为0.5NA D.在200mL 5mol·L-1 AlCl3溶液中,Al3+数目为NA,等于Cl-数目的1/3 |
|
| 8. 选择题 | 详细信息 |
|
下列离子方程式书写正确的是 A. 硫酸铝溶液中滴加过量浓氨水:Al3+ + 4OH- = AlO B. NaHCO3溶液水解:HCO C. 浓氢氧化钠溶液吸收少量SO2气体:SO2+ 2OH- = SO D. 向小苏打溶液中加入醋酸溶液:HCO |
|
| 9. 选择题 | 详细信息 |
|
向NaBr、NaI、Na2SO3混合液中,通入过量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是 ( ) A.NaCl Na2SO4 B.NaCl NaBr Na2SO4 C.NaCl Na2SO4 I2 D.NaCl NaI Na2SO4 |
|
| 10. 选择题 | 详细信息 |
|
下列关于热化学反应的描述中正确的是 A. HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol C. 需要加热才能发生的反应一定是吸热反应 D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
|
| 11. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱 C.Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物 D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
|
| 12. 选择题 | 详细信息 |
关于如下图所示装置的叙述,正确的是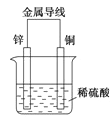 A. 铜是阳极,铜片上有气泡产生 B. 铜片质量逐渐减少 C. 电流从锌片经导线流向铜片 D. 氢离子在铜片表面被还原 |
|
| 13. 选择题 | 详细信息 |
|
下列有关实验的说法正确的是( ) A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
|
| 14. 选择题 | 详细信息 |
|
用高铁酸钠(Na2FeO4)对湖水消毒,是城市饮水处理的新技术。已知反应Fe2O3+ 3Na2O2= 2Na2FeO4 +Na2O。下列说法正确的是 A.Na2O2既是氧化剂又是还原剂 B.Na2FeO4既是氧化产物又是还原产物 C.3molNa2O2发生反应,有12mol电子转移 D.在Na2FeO4中Fe为+4价,只有强氧化性,能消毒杀菌 |
|
| 15. 选择题 | 详细信息 |
|
25 ℃时,水的电离达到平衡:H2O A. 向水中加人稀氨水,平衡逆向移动,c(OH-)降低 B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 C. 向水中加人少量固体CH3COONa ,平衡逆向移动,c(H+)降低 D. 将水加热,Kw增大,pH不变 |
|
| 16. 选择题 | 详细信息 |
|
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( ) ①a-b=n-m ②元素的原子序数a>b>c>d ③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y A.③ B.①②③④ C.①②③ D.②③ |
|
| 17. 选择题 | 详细信息 |
如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )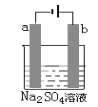 A.逸出气体的体积,a电极的小于b电极的 B.一电极逸出无味气体,另一电极逸出刺激性气味气体 C.a电极附近呈红色,b电极附近呈蓝色 D.a电极附近呈蓝色,b电极附近呈红色 |
|
最近更新



