иҘҝи—ҸиҮӘжІ»еҢәжӢүиҗЁдёӯеӯҰ2020еұҠй«ҳдёүеүҚеҚҠжңҹ第еӣӣж¬ЎжңҲиҖғзҗҶз»јеҢ–еӯҰ
| 1. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜпјҲ пјү A. 60п№Ә-70п№Әзҡ„з”ІйҶӣж°ҙжә¶ж¶Із§°дёәзҰҸ尔马жһ—е…·жңүйҳІи…җжқҖиҸҢзҡ„ж•Ҳжһң B. ж¶ІжәҙеҸҜд»ҘеҠ е°‘йҮҸж°ҙдҝқеӯҳеңЁжЈ•иүІзҡ„иҜ•еүӮ瓶дёӯ C. иӢҜй…ҡжә…еҲ°зҡ®иӮӨдёҠпјҢз«ӢеҚіз”Ёж°ҙеҶІжҙ—пјҢ然еҗҺж¶ӮдёҠзЁҖзЎјй…ёжә¶ж¶І D. жІ№и„ӮдёҚиғҪдҪҝжәҙж°ҙиӨӘиүІ |
|
| 2. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰз”ЁиҜӯжӯЈзЎ®зҡ„жҳҜпјҲ пјү A. йҮҚж°ҙзҡ„еҲҶеӯҗејҸпјҡD2O B. ж¬Ўж°Ҝй…ёзҡ„з»“жһ„ејҸпјҡHвҖ”ClвҖ”O C. д№ҷзғҜзҡ„е®һйӘҢејҸпјҡC2H4 D. дәҢж°§еҢ–зЎ…зҡ„еҲҶеӯҗејҸпјҡSiO2 |
|
| 3. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
йҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјдёәNAгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ A. ж ҮеҮҶзҠ¶еҶөдёӢпјҢ11.2L12C18Oдёӯеҗ«жңүзҡ„дёӯеӯҗж•°дёә8NA B. еёёжё©еёёеҺӢдёӢпјҢ12gйҮ‘еҲҡзҹідёӯеҗ«жңүCпјҚCй”®ж•°дёә4NA C. 1mol Li2OгҖҒNa2O2зҡ„ж··еҗҲзү©дёӯеҗ«жңүзҡ„зҰ»еӯҗжҖ»ж•°еӨ§дәҺ3NA D. 25в„ғж—¶пјҢpH=2зҡ„H2SO4жә¶ж¶Ідёӯеҗ«жңүH+зҡ„ж•°зӣ®дёә0.02NA |
|
| 4. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
еҗ‘еӣӣж”ҜиҜ•з®ЎдёӯеҲҶеҲ«еҠ е…Ҙе°‘йҮҸдёҚеҗҢзҡ„ж— иүІжә¶ж¶ІиҝӣиЎҢеҰӮдёӢж“ҚдҪңпјҢз»“и®әжӯЈзЎ®зҡ„жҳҜ
|
|||||||||||||||||||||
| 5. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
XгҖҒYгҖҒZгҖҒWжҳҜеҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§зҡ„зҹӯе‘Ёжңҹе…ғзҙ гҖӮXзҡ„ж°ўеҢ–зү©еёёз”ЁдәҺеҲ»иҡҖзҺ»з’ғпјҢYеңЁеҗҢе‘ЁжңҹдёӯйҮ‘еұһжҖ§жңҖејәпјҢZзҡ„еҚ•иҙЁжҳҜдәәзұ»е°ҶеӨӘйҳіиғҪиҪ¬еҢ–дёәз”өиғҪзҡ„еёёз”Ёжқҗж–ҷпјҢWдёҺXеҗҢдё»ж—ҸгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ A. з®ҖеҚ•ж°ўеҢ–зү©жІёзӮ№пјҡX>W B. з®ҖеҚ•зҰ»еӯҗеҚҠеҫ„пјҡr(X)<r(Y)<r(W) C. Zе…ғзҙ еҢ–еӯҰжҖ§иҙЁзЁіе®ҡпјҢеңЁиҮӘ然з•Ңд»ҘжёёзҰ»жҖҒеӯҳеңЁ D. Wзҡ„з®ҖеҚ•зҰ»еӯҗдјҡеҪұе“Қж°ҙзҡ„з”өзҰ»е№іиЎЎ |
|
| 6. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
е·ІзҹҘпјҡpOH=пјҚlgc(OHпјҚ)гҖӮе®Өжё©дёӢпјҢе°ҶзЁҖзӣҗй…ёж»ҙеҠ еҲ°жҹҗдёҖе…ғзўұ(BOH)жә¶ж¶ІдёӯпјҢжөӢеҫ—ж··еҗҲжә¶ж¶Ізҡ„pOHдёҺзҰ»еӯҗжө“еәҰзҡ„еҸҳеҢ–е…ізі»еҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—еҸҷиҝ°й”ҷиҜҜзҡ„жҳҜ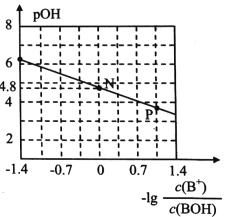 A. BOHеұһдәҺејұзўұ B. BOHзҡ„з”өзҰ»еёёж•°K=1Г—10пјҚ4.8 C. PзӮ№жүҖзӨәзҡ„жә¶ж¶Ідёӯпјҡc(ClпјҚ)>c(B+) D. NзӮ№жүҖзӨәзҡ„жә¶ж¶Ідёӯпјҡc(H+)=c(ClпјҚ)+c(OHпјҚ)пјҚc(BOH) |
|
| 7. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жұЎж°ҙжІ»зҗҶи¶ҠжқҘи¶Ҡеј•иө·дәә们йҮҚи§ҶпјҢеҸҜд»ҘйҖҡиҝҮиҶңз”өжұ йҷӨеҺ»еәҹж°ҙдёӯзҡ„д№ҷй…ёй’ е’ҢеҜ№ж°ҜиӢҜй…ҡ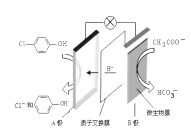 A.з”өжөҒж–№еҗ‘д»ҺBжһҒжІҝеҜјзәҝз»Ҹе°ҸзҒҜжіЎжөҒеҗ‘AжһҒ B.Aдёәз”өжұ зҡ„жӯЈжһҒпјҢеҸ‘з”ҹиҝҳеҺҹеҸҚеә” C.AжһҒзҡ„з”өжһҒеҸҚеә”ејҸдёәпјҡ D.еҪ“еӨ–з”өи·Ҝдёӯжңү0.2moleпјҚиҪ¬з§»ж—¶пјҢиҝӣе…ҘAжһҒеҢәзҡ„H+зҡ„дёӘж•°дёә0.2NA |
|
| 8. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
MnSO4жҷ¶дҪ“жҳҜдёҖз§Қжҳ“жә¶дәҺж°ҙзҡ„еҫ®зәўиүІжҷ¶дҪ“пјҢжҹҗж ЎеҗҢеӯҰи®ҫи®Ўе®һйӘҢеҲ¶еӨҮ并жЈҖйӘҢMnSO4зҡ„жҖ§иҙЁгҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүз”Із»„еҗҢеӯҰи®ҫи®Ўз”ЁSO2е’ҢйҖӮйҮҸзәҜеҮҖзҡ„MnO2еҲ¶еӨҮMnSO4пјҢе…¶иЈ…зҪ®еҰӮдёӢпјҡ  в‘ AиЈ…зҪ®дёӯеӣәдҪ“иҚҜе“ҒXйҖҡеёёжҳҜ______еЎ«еҢ–еӯҰејҸпјүгҖӮ в‘ЎBиЈ…зҪ®дёӯйҖҡSO2зҡ„еҜјз®Ўжң«з«ҜжҺҘеӨҡеӯ”зҗғжіЎзҡ„зӣ®зҡ„жҳҜ______пјӣCиЈ…зҪ®з”ЁдәҺеҗёж”¶е°‘йҮҸзҡ„SO2пјҢеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә______гҖӮ пјҲ2пјүд№ҷз»„еҗҢеӯҰе®ҡжҖ§жЈҖйӘҢз”Із»„еҗҢеӯҰзҡ„дә§е“ҒдёӯMn2+зҡ„еӯҳеңЁпјҢеҸ–е°‘йҮҸжҷ¶дҪ“жә¶дәҺж°ҙпјҢеҠ е…ҘпјҲNH4пјү2S2O8жә¶ж¶ІпјҢж»ҙе…ҘзЎқ酸银пјҲдҪңеӮ¬еҢ–еүӮпјүпјҢеҫ®зғӯжҢҜиҚЎпјҢжә¶ж¶Іжҳҫзҙ«иүІпјҢеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә______гҖӮ пјҲ3пјүдёҷз»„еҗҢеӯҰдёәжЈҖйӘҢж— ж°ҙMnSO4пјҲжҺҘиҝ‘зҷҪиүІпјүзҡ„зғӯеҲҶи§Јдә§зү©пјҢе°ҶMnSO4жҷ¶дҪ“и„ұж°ҙеҗҺж”ҫе…ҘдёӢеӣҫжүҖзӨәзҡ„иЈ…зҪ®дёӯпјҢжү“ејҖK1е’ҢK2пјҢзј“ж…ўйҖҡе…ҘN2пјҢеҠ зғӯпјҢзЎ¬иҙЁзҺ»з’ғз®ЎдёӯжңҖеҗҺеҫ—еҲ°й»‘иүІеӣәдҪ“гҖӮ 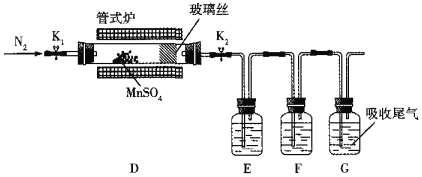 в‘ жЈҖйӘҢеҲҶи§Јзҡ„ж°”жҖҒдә§зү©дёӯжҳҜеҗҰжңүSO2еҸҠSO3пјҢиЈ…зҪ®EгҖҒFдёӯзҡ„жә¶ж¶Ідҫқж¬ЎжҳҜ______гҖҒ______пјҲеЎ«еӯ—жҜҚпјүгҖӮ aпјҺBaпјҲNO3пјү2жә¶ж¶І bпјҺBaCl2жә¶ж¶І cпјҺе“Ғзәўжә¶ж¶І dпјҺжө“зЎ«й…ё в‘ЎиӢҘDдёӯеҫ—еҲ°зҡ„й»‘иүІзІүжң«дёәMn3O4пјҢEгҖҒFдёӯеқҮжңүжҳҺжҳҫзҺ°иұЎпјҢеҲҷDдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә______гҖӮ пјҲ4пјүдёҒз»„еҗҢеӯҰи®ҫи®Ўе®һйӘҢд»Ҙдёҷз»„еҗҢеӯҰеҫ—еҲ°зҡ„й»‘иүІзІүжң«дёәеҺҹж–ҷпјҢеҲ©з”Ёй“қзғӯеҸҚеә”еҺҹзҗҶе°Ҷе…¶иҝҳеҺҹдёәйҮ‘еұһй”°пјҢжүҖйңҖзҡ„иҚҜе“ҒйҷӨж°Ҝй…ёй’ҫеӨ–пјҢиҝҳйңҖиҰҒ______гҖӮ |
|
| 9. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
NF3пјҲдёүж°ҹеҢ–ж°®пјүеңЁеёёжё©еёёеҺӢдёӢжҳҜж— иүІгҖҒж— е‘ізҡ„ж°”дҪ“пјҢжҳҜеҫ®з”өеӯҗе·ҘдёҡдёӯдёҖз§ҚдјҳиүҜзҡ„зӯүзҰ»еӯҗиҡҖеҲ»ж°”дҪ“гҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүNF3зҡ„з”өеӯҗејҸдёә______пјҢNе…ғзҙ зҡ„еҢ–еҗҲд»·дёә______гҖӮ пјҲ2пјүF2дёҺNH3зӣҙжҺҘеҸҚеә”з”ҹжҲҗNF3зҡ„еҢ–еӯҰж–№зЁӢејҸдёә______гҖӮ пјҲ3пјүе®һйӘҢе®ӨжЁЎжӢҹе·ҘдёҡдёҠеҲ©з”Ёз”өи§ЈзҶ”иһҚNH4HF2пјҲNH4FвҖўHFпјүжі•еҲ¶еҸ–NF3пјҢйҳіжһҒдёәд»ҘNiдёәеҹәжң¬жқҗж–ҷзҡ„еҗҲйҮ‘пјҲеҶ…еҗ«е…¶д»–йҮ‘еұһпјҢеҝҪз•Ҙй•ҚеҸҠе…¶д»–йҮ‘еұһзҡ„еҸҚеә”пјүпјҢйҳҙжһҒдёәзўізҙ й’ўпјҢз”өи§Јеәҹж¶ІеҸҜеӣһ收еҶҚеҲ©з”ЁгҖӮ в‘ з”өи§Јж—¶NF3еңЁ______жһҒз”ҹжҲҗпјӣйҳҙжһҒдә§з”ҹзҡ„ж°”дҪ“жҳҜ______пјҲеЎ«еҢ–еӯҰејҸпјүгҖӮ в‘Ўз”өи§ЈеҗҺеәҹж¶ІпјҲеҗ«Niе°‘йҮҸFeе’ҢCuзҡ„еҚ•иҙЁеҸҠNH4HF2зӯүпјүеҸҜз»ҸеҰӮдёӢжөҒзЁӢиҝӣиЎҢеӣһ收еҶҚеҲ©з”Ёпјҡ 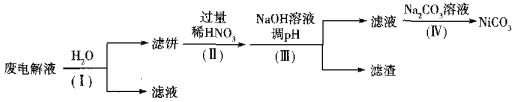 е·ІзҹҘиҜҘе®һйӘҢжқЎд»¶дёӢпјҢйғЁеҲҶйҮ‘еұһзҰ»еӯҗејҖе§ӢжІүж·ҖдёҺжІүж·Җе®Ңе…Ёзҡ„pHеҰӮдёӢиЎЁ
|
||||||||||||||||
| 10. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
ж°ЁжҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҢ–е·ҘеҺҹж–ҷпјҢеҸҜд»Ҙз”ЁжқҘеҲ¶еӨҮж°®еҢ–зЎ…(Si3N4)иӮј(N2H4)гҖҒж°ўж°°й…ё(HCN)гҖӮ (1)е·ІзҹҘпјҡSi(s)+2Cl2(g)====SiCl4(g) в–іH1=akJВ·molпјҚ1 N2(g)+3H2(g) 3Si(s)+2N2(g)====Si3N4(s) в–іH3=ckJВ·molпјҚ1 H2(g)+Cl2(g)====2HCl(g) в–іH4=dkJВ·molпјҚ1 еҲҷеҸҚеә”3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g)зҡ„в–іH=________________kJВ·molпјҚ1(з”ЁaгҖҒbгҖҒcгҖҒdиЎЁзӨә)гҖӮ (2)иӮјзҡ„еҲ¶еӨҮж–№жі•жҳҜз”Ёж¬Ўж°Ҝй…ёй’ ж°§еҢ–иҝҮйҮҸзҡ„ж°ЁгҖӮ е·ІзҹҘClOпјҚж°ҙи§Јзҡ„ж–№зЁӢејҸдёәпјҡClOпјҚ+H2 O=HClO+OHпјҚгҖӮеёёжё©дёӢпјҢиҜҘж°ҙи§ЈеҸҚеә”зҡ„е№іиЎЎеёёж•°дёәK=1.0Г—10пјҚ6molВ·LпјҚ1пјҢеҲҷ1.0molВ· L пјҚ1NaCIOжә¶ж¶Ізҡ„pH=________гҖӮ (3)е·ҘдёҡдёҠеҲ©з”Ёж°Ёж°”з”ҹдә§ж°ўж°°й…ё(HCN)зҡ„еҸҚеә”дёәпјҡCH4(g)+NH3(g) в‘ е…¶д»–жқЎд»¶дёҖе®ҡпјҢиҫҫеҲ°е№іиЎЎж—¶NH3иҪ¬еҢ–зҺҮйҡҸеӨ–з•ҢжқЎд»¶XеҸҳеҢ–зҡ„е…ізі»еҰӮеӣҫжүҖзӨәгҖӮXд»ЈиЎЁзҡ„жҳҜ________(еЎ«вҖңжё©еәҰвҖқжҲ–вҖңеҺӢејәвҖқ)гҖӮ 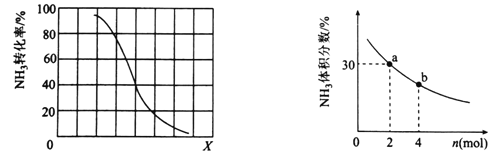 в‘Ўе…¶д»–жқЎд»¶дёҖе®ҡпјҢеҗ‘2LеҜҶй—ӯе®№еҷЁдёӯеҠ дәә n mol CH4е’Ң2 mol NH3пјҢе№іиЎЎж—¶NH3дҪ“з§ҜеҲҶж•°йҡҸnеҸҳеҢ–зҡ„е…ізі»еҰӮеӣҫжүҖзӨәгҖӮиӢҘеҸҚеә”д»ҺејҖе§ӢеҲ°aзӮ№жүҖз”Ёж—¶й—ҙдёә10minпјҢиҜҘж—¶й—ҙж®өеҶ…з”ЁCH4зҡ„жө“еәҰеҸҳеҢ–иЎЁзӨәзҡ„еҸҚеә”йҖҹзҺҮдёә________molВ·LпјҚ1В·minпјҚ1пјӣе№іиЎЎеёёж•°пјҡK(a) ________K(b)(еЎ«вҖң>вҖқвҖң=вҖқжҲ–вҖң<вҖқ) в‘ўе·ҘдёҡдёҠз”Ёз”өи§Јжі•еӨ„зҗҶеҗ«ж°°з”өй•Җеәҹж°ҙ(pH=10)зҡ„иЈ…зҪ®еҰӮеӣҫжүҖзӨәгҖӮ 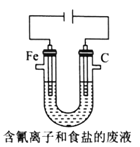 йҳіжһҒдә§з”ҹзҡ„ж°Ҝж°”дёҺзўұжҖ§жә¶ж¶ІеҸҚеә”з”ҹжҲҗClO-пјҢClOпјҚе°ҶCNпјҚж°§еҢ–зҡ„зҰ»еӯҗж–№зЁӢејҸдёәпјҡ_____CNпјҚ+ _____ClOпјҚ+ ________====_____CO32пјҚ+_____N2вҶ‘+________+________иӢҘз”өи§ЈеӨ„зҗҶ2 mol CNпјҚпјҢеҲҷйҳҙжһҒдә§з”ҹж°”дҪ“зҡ„дҪ“з§Ҝ(ж ҮеҮҶзҠ¶еҶөдёӢ)дёә________LгҖӮ |
|
| 11. еЎ«з©әйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
ж°ҹеҸҠе…¶еҢ–еҗҲзү©з”ЁйҖ”йқһеёёе№ҝжіӣгҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүиҒҡеӣӣж°ҹд№ҷзғҜжҳҜдёҖз§ҚеҮҶжҷ¶дҪ“пјҢеҮҶжҷ¶дҪ“жҳҜдёҖз§Қж— е№із§»е‘ЁжңҹеәҸпјҢдҪҶжңүдёҘж јеҮҶе‘ЁжңҹдҪҚзҪ®еәҸзҡ„зӢ¬зү№жҷ¶дҪ“пјҢеҸҜйҖҡиҝҮ______ж–№жі•еҢәеҲҶжҷ¶дҪ“еҮҶжҷ¶дҪ“е’Ңйқһжҷ¶дҪ“гҖӮ пјҲ2пјүеҹәжҖҒFеҺҹеӯҗзҡ„д»·еұӮз”өеӯҗжҺ’еёғеӣҫпјҲиҪЁйҒ“иЎЁиҫҫејҸпјүдёә______гҖӮ пјҲ3пјү[H2F]+[SbF6]-пјҲж°ҹй”‘й…ёпјүжҳҜдёҖз§Қи¶…ејәй…ёпјҢеӯҳеңЁ[H2F]+пјҢиҜҘзҰ»еӯҗзҡ„з©әй—ҙжһ„еһӢдёә______пјҢдёҺ[H2F]+е…·жңүзӣёеҗҢз©әй—ҙжһ„еһӢе’Ңй”®еҗҲеҪўејҸзҡ„еҲҶеӯҗе’ҢйҳҙзҰ»еӯҗеҲҶеҲ«жҳҜ______пјҲеҗ„дёҫдёҖдҫӢпјүгҖӮ пјҲ4пјүNH4FпјҲж°ҹеҢ–й“өпјүеҸҜз”ЁдәҺзҺ»з’ғзҡ„иҡҖеҲ»йҳІи…җеүӮгҖҒж¶ҲжҜ’еүӮгҖӮNH4+дёӯдёӯеҝғеҺҹеӯҗзҡ„жқӮеҢ–зұ»еһӢжҳҜ______пјӣж°ҹеҢ–й“өдёӯеӯҳеңЁ______пјҲеЎ«еӯ—жҜҚпјүгҖӮ AпјҺзҰ»еӯҗй”® BпјҺПғй”® CпјҺПҖй”® DпјҺж°ўй”® пјҲ5пјүSF6иў«е№ҝжіӣз”ЁдҪңй«ҳеҺӢз”өж°”и®ҫеӨҮзҡ„з»қзјҳд»ӢиҙЁгҖӮSF6жҳҜдёҖз§Қе…ұд»·еҢ–еҗҲзү©пјҢеҸҜйҖҡиҝҮзұ»дјјдәҺBorn-HaberеҫӘзҺҜиғҪйҮҸжһ„е»әиғҪйҮҸеӣҫпјҲaпјүи®Ўз®—зӣёе…ій”®иғҪгҖӮеҲҷF-Fй”®зҡ„й”®иғҪдёә______kJвҖўmol-1пјҢS-Fй”®зҡ„й”®иғҪдёә______kJвҖўmol-1гҖӮ 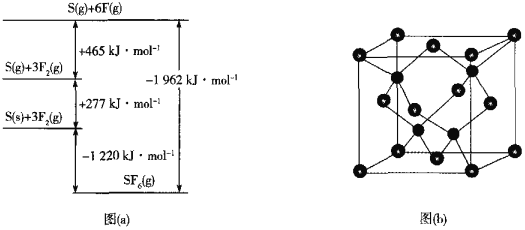 пјҲ6пјүCuClзҡ„зҶ”зӮ№дёә426в„ғпјҢзҶ”еҢ–ж—¶еҮ д№ҺдёҚеҜјз”өпјӣCuFзҡ„зҶ”зӮ№дёә908в„ғпјҢеҜҶеәҰдёә7.1gвҖўcm-3гҖӮ в‘ CuFзҡ„зҶ”зӮ№жҜ”CuClзҡ„й«ҳпјҢеҺҹеӣ жҳҜ______ в‘Ўе·ІзҹҘNAдёәйҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјпјҢCuFзҡ„жҷ¶иғһз»“жһ„еҰӮеӣҫпјҲbпјүжүҖзӨәпјҢеҲҷCuFзҡ„жҷ¶иғһеҸӮж•°a=______nmпјҲеҲ—еҮәи®Ўз®—ејҸпјүгҖӮ |
|
| 12. еЎ«з©әйўҳ | иҜҰз»ҶдҝЎжҒҜ |
2дёҖж°Ё-3вҖ”ж°ҜиӢҜз”Ій…ёжҳҜзҷҪиүІжҷ¶дҪ“пјҢе…¶еҲ¶еӨҮжөҒзЁӢеҰӮдёӢпјҡ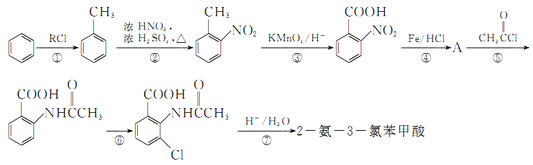 е·ІзҹҘпјҡ  еӣһзӯ”дёӢеҲ—зӣёе…ій—®йўҳ (1) (2)еҸҚеә”в‘ дёӯRд»ЈиЎЁзҡ„жҳҜ_____________пјҢеҸҚеә”в‘Ўзҡ„еҸҚеә”зұ»еһӢдёә_____________гҖӮ (3)еҰӮжһңеҸҚеә”в‘ўдёӯKMnO4зҡ„иҝҳеҺҹдә§зү©дёәMnSO4пјҢиҜ·еҶҷеҮәиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ_____________гҖӮ (4)Aзҡ„з»“жһ„з®ҖејҸдёә_____________пјҢв‘Ҙзҡ„еҸҚеә”жқЎд»¶дёә_____________гҖӮ (5)з¬ҰеҗҲдёӢеҲ—жқЎд»¶зҡ„еҗҢеҲҶејӮжһ„дҪ“зҡ„з»“жһ„з®ҖејҸдёә_____________гҖӮ a.ејҸйҮҸжҜ” b.дёҺй…ёжҖ§KMnO4еҸҚеә”иғҪз”ҹжҲҗдәҢе…ғзҫ§й…ё c.д»…жңү3з§Қзӯүж•Ҳж°ў (6)дәӢе®һиҜҒжҳҺдёҠиҝ°жөҒзЁӢзҡ„зӣ®ж Үдә§зү©зҡ„дә§зҺҮеҫҲдҪҺпјӣжҚ®жӯӨпјҢз ”з©¶дәәе‘ҳжҸҗеҮәе°ҶжӯҘйӘӨв‘Ҙи®ҫи®Ўдёәд»ҘдёӢдёүжӯҘпјҢдә§зҺҮжңүдәҶдёҖе®ҡжҸҗй«ҳгҖӮ  еҲҶжһҗдә§зҺҮжҸҗй«ҳзҡ„еҺҹеӣ жҳҜ_____________гҖӮ |
|
- е№ҝе·һеёӮй«ҳдёүеҢ–еӯҰдёҠеҶҢдё“йўҳз»ғд№ еҗҢжӯҘиҖғиҜ•жЈҖжөӢ
- иҘҝи—ҸиҮӘжІ»еҢәжһ—иҠқеёӮ第дәҢй«ҳзә§дёӯеӯҰ2020еұҠй«ҳдёүдёҠеҚҠе№ҙ第дёҖж¬ЎжңҲиҖғзҗҶ科综еҗҲеҢ–еӯҰиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§Јжһҗ
- е№ҝдёң2020е№ҙй«ҳдёүдёҠжңҹеҢ–еӯҰж— зәёиҜ•еҚ·
- жӯҰжұүеёӮй«ҳдёҖеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•е…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- дёҠжө·еёӮй«ҳдёүеҢ–еӯҰдёҠеҶҢжңҲиҖғиҜ•еҚ·еңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- й«ҳдёҖеҢ–еӯҰдёӢеҶҢеҚ•е…ғжөӢиҜ•еҗҢжӯҘиҖғиҜ•жЈҖжөӢ
- еӨ©жҙҘеёӮ2018е№ҙй«ҳдёүеҢ–еӯҰдёҠеӯҰжңҹжңҲиҖғжөӢйӘҢиҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§Јжһҗ
- е®һйӘҢдёӯеӯҰгҖҒеӨ§иҝһе…«дёӯгҖҒеӨ§иҝһдәҢеҚҒеӣӣдёӯгҖҒйһҚеұұдёҖдёӯгҖҒдёңеҢ—иӮІжүҚеӯҰж Ўй«ҳдёүеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•йўҳеёҰзӯ”жЎҲе’Ңи§Јжһҗ



