天津2019年高三上册化学月考测验网络考试试卷
| 1. | 详细信息 |
|
下列有关物质分类或归类正确的是 ①混合物:漂白粉、水玻璃、Fe(OH)3胶体、水银 ②化合物:CaCl2、NaOH、HCl、HD ③电解质:胆矾、苛性钾、冰醋酸、氧化钠 ④同素异形体:C60、碳纳米管、金刚石、石墨 ⑤煤的干馏、煤的汽化和液化都属于化学变化 A. ③④⑤ B. ②③ C. ③④ D. ②⑤ |
|
| 2. | 详细信息 |
|
下列实验与物质微粒大小无直接关系的是 ( ) A. 过滤  B. 渗析 B. 渗析 C. 萃取  D. 丁达尔效应 D. 丁达尔效应 |
|
| 3. | 详细信息 |
|
下列说法正确的是 ①有化学键破坏的变化一定属于化学变化 ②发生了能量变化的一定是化学变化 ③电解质溶液导电一定发生化学变化 ④无水硫酸铜由白变蓝,一定是化学变化 ⑤用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化 ⑥16O与18O间的相互转化为物理变化,O2和O3的相互转化为化学变化 A. ①③⑤ B. ③④⑤⑥ C. ②③④ D. 全部 |
|
| 4. | 详细信息 |
|
500mL2mol·L-1FeCl3溶液和500mL2mol·L-1明矾溶液分别滴入沸水中,加热制成分散系甲、乙,经测定,甲分散系中分散质的粒子直径大小在1~100nm之间,乙分散系中分散质的粒子直径大小在10-9~10-7m之间,关于甲、乙分散系的判断合理的是 A. 用一束明亮的“强光”照射甲、乙,发现甲有丁达尔效应,乙没有丁达尔效应 B. 向甲、乙中分别滴加过量的氢氧化钠溶液,现象都是“先聚沉,后溶解” C. 向甲、乙中分别滴加过量的氢碘酸,最终现象分别是深褐色溶液、无色溶液 D. 蒸干、灼烧FeCl3溶液和明矾溶液会得到对应的固体盐 |
|
| 5. | 详细信息 |
|
常温下,下列各组离子在指定溶液中一定能大量共存的是 ①pH = 0的溶液:Na+、C2O42-、MnO4-、SO42- ②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32- ③水电离出的H+浓度为10-12mol·L-1的溶液:Cl-、CO32-、NO3-、SO32- ④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42- ⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42- ⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-、S2- A. ①③⑤ B. ②④ C. ②⑤⑥ D. ①④⑤ |
|
| 6. | 详细信息 |
|
在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( ) a. 体积②>③>①>④ b. 密度②>③>④>① c. 质量②>③>①>④ d. 氢原子个数①>③>④>② A. abc B. bcd C. abd D. abcd |
|
| 7. | 详细信息 |
|
由14CO和12CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),则下列关系正确的是 A. 混合气体中,12CO占有的体积等于14CO占有的体积 B. 混合气体中,12CO与14CO分子个数之比为1∶2 C. 混合气体中,12CO与14CO质量之比为15∶14 D. 混合气体中,12CO与14CO密度之比为14∶15 |
|
| 8. | 详细信息 |
|
下列说法正确的是 ①1 mol羟基所含电子数为10NA; ②一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液中含NH4+的物质的量小于0.5NA; ③1 mol臭氧和1.5 mol氧气含有相同的氧原子数; ④58.5 g的NaCl固体中含有NA个氯化钠分子; ⑤在反应KIO3+6HI==KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA; ⑥标准状况下,2.24 L H2O含有的分子数等于0.1NA; ⑦1 mol 乙烷分子中含有8NA个共价键; ⑧78gNa2O2中含有NA个阴离子; ⑨常温下,7.1 g Cl2与足量NaOH溶液反应转移的电子数约为0.2×6.02×1023; ⑩4.0 g重水(D2O)中所含质子数为2NA。 A. ④⑤⑦⑧⑨ B. ②③⑧⑩ C. 只有③ D. 全部 |
|
| 9. | 详细信息 |
下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是 A. 该硫酸的物质的量浓度为 9.2 mol/L B. 1 mol Zn与足量的该硫酸反应产生2 g氢气 C. 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL D. 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L |
|
| 10. | 详细信息 |
|
在 T ℃时,将ag NH3完全溶于水,得到V mL 溶液,假设该溶液的密度为d g/mL,溶质的质量分数为w,其中含 NH4 +的物质的量为b mol。下列叙述中正确的是 A. 溶质的质量分数为 w=1000a/17V×100% B. 溶质的物质的量浓度 c=1000a/17V mol·L-1 C. 溶液中 c(OH-)=1000b/17V mol·L-1 D. 上述溶液中再加入V mL 水后,所得溶液溶质的质量分数大于0.5w |
|
| 11. | 详细信息 |
|
氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4 A. NaAlH4中氢元素为+1价 B. 每生成11. 2 L(标准状况下)H2,转移2NA个电子 C. 在反应中有50%的氢被氧化 D. 反应中氧化产物与还原产物的物质的量之比为1: 1 |
|
| 12. | 详细信息 |
|
下列反应的离子方程式正确的是 A. Fe(OH)3和HI的反应:Fe(OH)3+3H+==Fe3++3H2O B. 1.5mol/L 100ml的FeBr2溶液中通入3.36L(标准状况)Cl2:2Fe2++2Br-+2Cl2==2Fe3++4Cl-+Br2 C. KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3==2FeO42−+3Cl−+4H++H2O D. 向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-==2Al(OH)3↓+3BaSO4↓ |
|
| 13. | 详细信息 |
下列示意图与对应的反应情况符合的是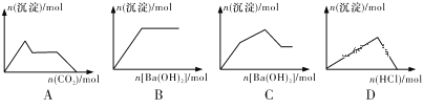 A. 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 D. 向NaAlO2溶液中逐滴加入盐酸至过量 |
|
| 14. | 详细信息 |
|
下列使所配溶液的物质的量浓度偏高的是 ①配制NaOH溶液时,NaOH固体中含有Na2O杂质②量筒量取液体溶质,用水冲洗量筒后,将冲洗液转移到容量瓶中③称量含结晶水的溶质时,溶质已风化④用量筒量取溶质液体时,俯视读数⑤溶解固体溶质或稀释溶液时,未冷却至室温即转入容量瓶进行定容⑥定容摇匀后发现液面下降 A. ①②③④⑤ B. ①②③⑤ C. ①②③⑤⑥ D. ①②③④⑤⑥ |
|
| 15. | 详细信息 |
|
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是 A. 在含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32- B. 含等物质的量的FeBr2、FeI2溶液中,缓慢通入氯气:I-、 Br-、Fe2+ C. 含等物质的量Fe3+、Cu2+、H+溶液中加锌粉: Fe3+、 Cu2+、H+、Fe2+ D. 在含等物质的量的H+、Al3+、NH4+的溶液中,逐滴加入NaOH溶液:H+、NH4+、Al3+ |
|
| 16. | 详细信息 | ||||||||||||
在学习中经常应用类推法。下列表格左边正确,类推法应用于右边也正确的是( )
|
|||||||||||||
| 17. | 详细信息 |
|
铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)可氧化硫酸锰(MnSO4),反应的离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,下列说法错误的是 A. 若有0.1mol氧化产物生成,则转移0.5mol电子 B. 铋酸钠难溶于水 C. 该反应可以用于鉴定Mn2+离子 D. 该反应可以用浓盐酸酸化 |
|
| 18. | 详细信息 |
|
将一定量的氯气通入30 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是 A. 与NaOH反应的氯气一定为0.3 mol B. n(Na+)∶n(Cl-)可能为7∶3 C. 若反应中转移的电子为n mol,则0.15<n<0.25 D. n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1 |
|
| 19. | 详细信息 |
| Fe(OH)3胶体的制备方法:________________________化学方程式为_____________________。FeCl3净水的原理__________(离子方程式解释) | |
| 20. | 详细信息 |
|
下列物质中 a.石墨 b.液氯 c.熔融Na2O d.NO2 e.氨水 f. NaCl溶液 g. CuSO4·5H2O h. 冰醋酸 i.盐酸 j.蔗糖 属于电解质的是____________, 属于非电解质的是 ____________,能导电的是______________。(用序号填写) |
|
| 21. | 详细信息 |
| 某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO和H2O。已知水是反应产物之一,写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目:_________________________。若反应过程中转移了1.2mol电子,则生成水的质量是__________________。 | |
| 22. | 详细信息 |
| 高锰酸钾和氢溴酸溶液可以发生下列反应:KMnO4+HBr→Br2+MnBr2+KBr+H2O,其中还原剂是______(填物质的化学式),若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是______mol。 | |
| 23. | 详细信息 |
|
请按要求书写下列离子方程式: (1)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,反应的离子方程式为______。向Ba(HCO3)2溶液中滴加过量NaOH溶液,反应的离子方程式__________。 (2)向NH4HCO3溶液中,滴加足量的NaOH溶液,反应的离子方程式为_______。在FeI2溶液中,滴加少量稀硝酸。该反应的离子方程式是:_____________。 (3)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O72-还原为Cr3+,该过程的离子反应方程式为_____________________________。 (4)向NaClO溶液中滴加KI溶液,反应后溶液呈黄色,该过程的离子反应方程式为_______________________________。 (5)向CuCl2溶液中通入一定量的SO2,微热,一段时间后可得CuCl白色沉淀。离子方程式为____________________________ (6)Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为_______________________________________________ |
|
| 24. | 详细信息 |
|
(1)在标准状况下3.2g CO与CO2的混合气体,体积为2.24L。则:混合气体的平均摩尔质量是________ CO2和CO的体积之比是________ CO2和CO的质量之比是_______,混合气体中所含氧原子的物质的量是_______ (2)若10 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有4 g Ca2+,则溶液中NO3-的物质的量浓度为____________ (3)在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度(mol·L-1)为 ____________________ (4)在反应3BrF3+5H2O===9HF+Br2+HBrO3+O2↑中,若有2molH2O参加反应,有_____mol水作还原剂,被水还原的溴元素____________mol; (5)把V L含MgSO4和K2SO4的混合溶液分成五等份,一份加入含a mol NaOH的溶液恰好使镁离子完全沉淀;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为_______ (6)3.04g铜镁合金完全溶解于50mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体2240mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,则该浓硝酸中HNO3的物质的量浓度是 ___mol·L-1,镁的质量为______g,NO2和N2O4的混合气体中,NO2的体积分数是___,得到5.08g沉淀时,加入NaOH溶液的体积是____mL。 (7)在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中有1/3的溴元素被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为________。 |
|
| 25. | 详细信息 |
|
(1)实验中需用0.2 mol/L的Na2CO3溶液450 mL,配制时应称取Na2CO3固体的质量为_______ (2)下图是某同学用500 mL容量瓶配制0.10 mol·L-1 NaOH溶液的过程:  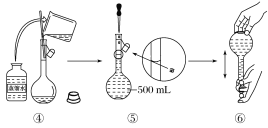 该同学的错误步骤有____________处 (3)配制220 mL 1.0 mol·L-1硫酸溶液: ①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________(计算结果保留一位小数)mL; ②如果实验室有15 mL、20 mL、50 mL量筒,应选用_______mL量筒最好; ③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______________________ (4)在配制4.6 mol/L稀H2SO4的过程中,下列情况对硫酸溶液物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”)? ①容量瓶检漏后未干燥就使用:____________。 ②定容时仰视观察液面:_____。 ③移液后未洗涤烧杯和玻璃棒:_______。 |
|
| 26. | 详细信息 |
I.某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝。回答下列问题: (1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:烧杯、托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是______________。 (2)写出步骤①中发生反应的离子方程式___________ (3)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。 乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?________。若合理,请用离子方程式解释其原因_________________________________(若你认为不合理,该空不作答)。 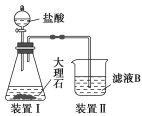 II.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下: 实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝; 实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。 (1)写出实验①中发生反应的离子方程式:_____________________________ (2)实验②的化学反应中转移电子的物质的量是_______________________。 (3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是__________________________________________________________。 |
|
最近更新



