2018еҗүжһ—й«ҳдёҖдёҠеӯҰжңҹдәәж•ҷзүҲй«ҳдёӯеҢ–еӯҰжңҹжң«иҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
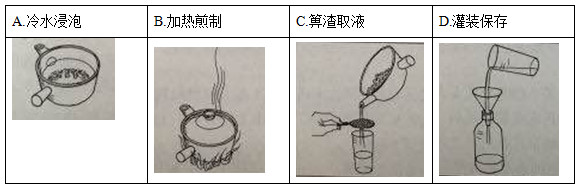
дёӢеҲ—дёӯиҚүиҚҜз…ҺеҲ¶жӯҘйӘӨдёӯпјҢеұһдәҺиҝҮж»Өж“ҚдҪңзҡ„жҳҜпјҲВ В пјү
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ҹжҙ»дёӯйҡҫе…ҚдјҡйҒҮеҲ°дёҖдәӣзӘҒеҸ‘дәӢ件пјҢжҲ‘们иҰҒе–„дәҺеҲ©з”ЁеӯҰиҝҮзҡ„зҹҘиҜҶпјҢйҮҮеҸ–科еӯҰгҖҒжңүж•Ҳзҡ„ж–№ В жі•дҝқжҠӨиҮӘе·ұпјҺеҰӮжһңеҸ‘з”ҹдәҶж°Ҝж°”жі„жјҸпјҢд»ҘдёӢиҮӘж•‘ж–№жі•еҫ—еҪ“зҡ„жҳҜпјҲгҖҖгҖҖпјү В AпјҺи§ӮеҜҹйЈҺеҗ‘пјҢиҝҺйЈҺж’ӨзҰ»В В В В В В В В В В BпјҺеҗ‘ең°еҠҝдҪҺзҡ„ең°ж–№ж’ӨзҰ» В CпјҺеӨҡе–қж°ҙ并еңЁе®ӨеҶ…ж”ҫдёҖзӣҶж°ҙВ В В В В В DпјҺз”Ёж№ҝжҜӣе·ҫжҲ–иҳёжңүзғ§зўұзҡ„жҜӣе·ҫжҚӮдҪҸеҸЈйј»ж’ӨзҰ»
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёӢеҲ—еҗ„ж°§еҢ–иҝҳеҺҹеҸҚеә”дёӯпјҢж°ҙж—ўдёҚдҪңж°§еҢ–еүӮпјҢд№ҹдёҚдҪңиҝҳеҺҹеүӮзҡ„жҳҜпјҲВ В В пјү В AпјҺ2F2 + 2H2O В CпјҺ2Na + 2H2O
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
зЎ…жҳҜвҖң21дё–зәӘзҡ„иғҪжәҗвҖқпјҢдё»иҰҒжҳҜз”ұдәҺдҪңдёәеҚҠеҜјдҪ“жқҗж–ҷзҡ„зЎ…еңЁеӨӘйҳіиғҪеҸ‘з”өиҝҮзЁӢдёӯе…·жңүйҮҚ иҰҒзҡ„дҪңз”ЁгҖӮдёӢеҲ—е…ідәҺзЎ…еҸҠе…¶еҢ–еҗҲзү©зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В В пјү A.еҚ•иҙЁзЎ…жҳҜеҲ¶йҖ е…үеҜјзәӨз»ҙзҡ„жқҗж–ҷ B.Ca2Mg5Si8O22(OH)2еҶҷжҲҗж°§еҢ–зү©зҡ„еҪўејҸдёәпјҡ2CaOВ·5MgOВ·8SiO2В·H2O C.зҹіиӢұгҖҒзҺ»з’ғгҖҒзҺӣз‘ҷйҘ°зү©йғҪжҳҜзЎ…й…ёзӣҗеҲ¶е“ҒгҖҖ D.иҮӘ然з•ҢдёӯзЎ…е…ғзҙ зҡ„иҙ®йҮҸдё°еҜҢпјҢ并еӯҳеңЁеӨ§йҮҸзҡ„еҚ•иҙЁзЎ…е’ҢдәҢж°§еҢ–зЎ…
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
иҝӣиЎҢеҢ–еӯҰе®һйӘҢеҝ…йЎ»жіЁж„Ҹе®үе…ЁпјҢдёӢеҲ—дәӢж•…еӨ„зҗҶж–№жі•жӯЈзЎ®зҡ„жҳҜпјҲВ В В В пјүВ В В В A.й’ еқ—жҺүеҲ°жЎҢйқўдёҠпјҢз«ӢеҚіз”ЁжүӢжӢҝиө·пјҢж”ҫе…Ҙзӣӣж”ҫй’ зҡ„иҜ•еүӮ瓶дёӯВ В В B.й’ еӨұзҒ«ж—¶пјҢз”ЁеӨ§йҮҸзҡ„ж°ҙжҲ–з”ЁжіЎжІ«зҒӯзҒ«еҷЁзҒӯзҒ« C.жө“зЎ«й…ёжә…еҲ°зҡ®иӮӨдёҠпјҢз«ӢеҚіз”ЁзЁҖNaOHжә¶ж¶Іжҙ—ж¶Ө В D.
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В В пјү A.ж¶Іж°ЁгҖҒж°ҜеҢ–ж°ўйғҪжҳҜзәҜеҮҖзү©пјҢжң¬иә«дёҚеҜјз”өдҪҶеұһдәҺз”өи§ЈиҙЁ B.ж°ҙзҺ»з’ғгҖҒжҫ„жё…зҹізҒ°ж°ҙгҖҒзғ§зўұе’ҢзәҜзўұжә¶ж¶ІйғҪйңҖиҰҒзӣӣж”ҫеңЁеёҰж©Ўиғ¶еЎһзҡ„иҜ•еүӮ瓶дёӯ C.й“қж§ҪиҪҰиғҪз”ЁдәҺиҝҗиҫ“еҶ·зҡ„жө“зЎқй…ёжҲ–зЁҖзЎқй…ё D.йқ’й“ңгҖҒй’ўгҖҒж°ҙ银гҖҒзЎ¬й“қйғҪеұһдәҺеҗҲйҮ‘
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
NAиЎЁзӨәйҳҝдјҸдјҪеҫ·зҪ—еёёж•°пјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ пјҲВ В В В пјү В A.0.1mol Cl2дёҺиҝҮйҮҸзЁҖNaOHжә¶ж¶ІеҸҚеә”пјҢиҪ¬з§»зҡ„з”өеӯҗжҖ»ж•°дёә0.1NA В B.1L 1mol/Lзҡ„HClOжә¶ж¶ІдёӯжүҖеҗ«H+зҰ»еӯҗж•°дёәNA В C.60gSiO2жҷ¶дҪ“дёӯеҗ«жңүSiO2еҲҶеӯҗж•°дёәNA D.ж ҮеҮҶзҠ¶еҶөдёӢпјҢ40g SO3зҡ„дҪ“з§ҜжҳҜ11.2L
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
йҖҡеёёжғ…еҶөдёӢиғҪе…ұеӯҳпјҢдё”иғҪз”Ёжө“зЎ«й…ёе№ІзҮҘзҡ„дёҖз»„ж°”дҪ“жҳҜпјҲВ В В пјү В AпјҺSO2гҖҒCl2гҖҒH2S В В В В В В В В В В В В В В В В В BпјҺO2гҖҒH2гҖҒSO2В В В В В В В В В В В В CпјҺNH3гҖҒH2гҖҒHClВ В В В В В В В В В В В В В В В В В DпјҺNOгҖҒHIгҖҒO2
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ | ||
|
.еҲ©з”ЁдёӢеҲ—е®һ
В A.з”ЁдәҺеҲ¶еӨҮ并收йӣҶе°‘йҮҸNO2В В В В В В В В В В В В В В В В В В В В B.еҲҶзҰ»CCl4иҗғеҸ–I2ж°ҙеҗҺзҡ„жңүжңәеұӮе’Ңж°ҙеұӮ NaBr жә¶ж¶І C.еҲ¶еҸ–并收йӣҶе№ІзҮҘзәҜеҮҖзҡ„NH3В В В В В В В В В В В D.жҜ”иҫғMnO2гҖҒCl2гҖҒBr2зҡ„ж°§еҢ–жҖ§
|
|||
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„зү©иҙЁзҡ„зЁҖжә¶ж¶Ізӣёдә’еҸҚеә”пјҢж— и®әжҳҜеүҚиҖ…ж»ҙе…ҘеҗҺиҖ…пјҢиҝҳжҳҜеҗҺиҖ…ж»ҙе…ҘеүҚиҖ…пјҢеҸҚеә” В В В зҺ°иұЎйғҪзӣёеҗҢзҡ„жҳҜпјҲгҖҖгҖҖпјү В В AпјҺNaHSO4е’ҢBaпјҲOHпјү2 В В В В В В BпјҺAlCl3е’ҢNaOHВ В В В CпјҺNaAlO2е’ҢH2SO4В В В В В В В В В В В В В В В В В В В В В В В В В DпјҺNa2CO3е’Ңзӣҗй…ё
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁ8NH3+3Cl2==6NH4Cl+N2еҸҚеә”дёӯпјҢиӢҘеҸҚеә”дёӯиҪ¬з§»6molз”өеӯҗпјҢеҸ‘з”ҹж°§еҢ–еҸҚеә”зҡ„зү©иҙЁ В В В еҸҠзү©иҙЁзҡ„йҮҸ A. 3 molCl2В В В В В B. 4 mol NH3В В В В C. 8 mol NH3В В В В В В D. 2mol NH3
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҪ¬еҢ–дёҚиғҪйҖҡиҝҮдёҖжӯҘеҸҚеә”е®һзҺ°зҡ„жҳҜпјҲВ В В В пјү в‘ FeвҶ’FeCl2В В В В В В В В В в‘ЎF в‘ЈAl2O3вҶ’Al(OH)3В В В В В в‘ӨSiO2 вҶ’ H2SiO3В В В В В В В В в‘ҘSвҶ’SO3 A.в‘Ўв‘ӨВ В В В В В В В В В В B.в‘ в‘Јв‘ӨВ В В В В В В В C.в‘ў
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
В жӢ¬еҸ·еҶ…дёәжқӮиҙЁпјҢйҷӨеҺ»дёӢеҲ—зү©иҙЁдёӯжүҖеҗ«зҡ„жқӮиҙЁпјҢйҖүз”ЁиҜ•еүӮдёҚжӯЈзЎ®зҡ„жҳҜ(В В В В A.C12пјҲHClпјүпјҡйҘұе’ҢNaClжә¶ж¶ІВ В В В В B.CO2(SO2)пјҡйҘұе’ҢNaHCO3жә¶ж¶І В В C.Al2O3(SiO2)пјҡNaOHжә¶ж¶ІВ В В В В В В В В В В В В В D.FeCl2жә¶ж¶І(FeCl3)пјҡFeзІү
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жҺЁж–ӯжӯЈзЎ®зҡ„жҳҜпјҲВ В пјү В В В В BпјҺNa2Oе’ҢNa2O2з»„жҲҗе…ғзҙ зӣёеҗҢпјҢдёҺSO2еҸҚеә”еҺҹзҗҶдёҺдә§зү©д№ҹе®Ңе…ЁзӣёеҗҢ В В CпјҺNOе’Ң В В DпјҺSO2е’Ңж°Ҝж°ҙйғҪиғҪдҪҝе“Ғзәўжә¶ж¶ІиӨӘиүІпјҢдҪҶдәҢиҖ…зҡ„дҪңз”ЁеҺҹзҗҶжҳҜдёҚеҗҢзҡ„
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
|
дёӢеҲ—жңүе…іе®һйӘҢж“ҚдҪңгҖҒзҺ°иұЎе’Ңи§ЈйҮҠжҲ–з»“и®әйғҪжӯЈзЎ®зҡ„жҳҜпјҲВ В В пјү
|
|||||||||||||||||||||
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
иӢҘM2O7xпјҚ+3S2пјҚ+14H+=2M3++3SвҶ“+7H2OпјҢеҲҷM2O7xпјҚдёӯзҡ„Mзҡ„еҢ–еҗҲд»·дёә(гҖҖгҖҖ)В В В В В В В В AпјҺ+2В В В В В В В В В В В В В В В B.+3В В В В В В В В В В В В CпјҺ+4В В В В В В В В В В В В В В В D.+6
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
еҗ‘еҗ«жңүзӣҗй…ёгҖҒ AlCl3е’ҢMgCl2зҡ„ж··еҗҲжә¶ж¶Ідёӯж»ҙе…ҘNaOHжә¶ж¶І,жһҗеҮәзҡ„жІүж·ҖиҙЁйҮҸ(m)дёҺ
В В MgCl2зҡ„зү©иҙЁзҡ„йҮҸд№ӢжҜ”жҳҜпјҲВ В В пјү В A. 1:1В В В В В В В В В В В В B. 3:2В В В В В В В В В В В C. 2:3В В В В В В В В В В В В D. 1:3
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„зҰ»еӯҗеңЁжҢҮе®ҡжә¶ж¶ІдёӯпјҢеҸҜиғҪеӨ§йҮҸе…ұеӯҳзҡ„жҳҜпјҲВ В пјү В В A. дҪҝзҹіи•ҠеҸҳзәўзҡ„жә¶ж¶ІдёӯпјҡFe2+пјҢNa+пјҢK+пјҢNO3-пјҢSO42-пјҢCl В В B. иғҪдҪҝpHиҜ•зәёеҸҳж·ұи“қиүІзҡ„жә¶ж¶ІдёӯпјҡK+пјҢNa+пјҢAlO2-пјҢNO3-пјҢSiO32-пјҢSO32- В В C. еҠ е…ҘAlиғҪж”ҫеҮәH2зҡ„жә¶ж¶ІдёӯпјҡNa+пјҢNH4+пјҢK+пјҢNO3-пјҢCl В В D. еҗ«жңүеӨ§йҮҸFe3+зҡ„жә¶ж¶ІпјҡK+пјҢNH4+пјҢNa+пјҢSO32-пјҢI
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
AгҖҒBгҖҒCгҖҒXеқҮдёәдёӯеӯҰеҢ–еӯҰеёёи§Ғзү©иҙЁпјҢдёҖе®ҡжқЎд»¶дёӢжңүеҰӮеӣҫжүҖзӨәиҪ¬еҢ–е…ізі»(е…¶д»–дә§зү©е·Із•ҘеҺ»)пјҢдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ(гҖҖ
В В BпјҺиӢҘXдёәKOHжә¶ж¶ІпјҢеҲҷAеҸҜдёәAlCl3 В В CпјҺиӢҘXдёәCl2пјҢеҲҷCеҸҜдёәFeCl3 В В DпјҺиӢҘAгҖҒBгҖҒCеқҮдёәз„°иүІеҸҚеә”е‘Ҳй»„иүІзҡ„еҢ–еҗҲзү©пјҢеҲҷXеҸҜдёәCO2
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҖе®ҡйҮҸзҡ„FeгҖҒFeOгҖҒFe2O3гҖҒFe3O4зҡ„ж··еҗҲзү©дёӯеҠ е…Ҙ350 mL 1 molВ·LпјҚ1зҡ„зЁҖзЎқй…ёжҒ°еҘҪдҪҝ ж··еҗҲзү©е®Ңе…Ёжә¶и§ЈпјҢж”ҫеҮә1.12 L NO(ж ҮеҮҶзҠ¶еҶө)пјҢеҫҖжүҖеҫ—жә¶ж¶ІдёӯеҠ е…ҘKSCNжә¶ж¶ІпјҢж— зәўиүІ еҮәзҺ°гҖӮиӢҘз”Ёи¶ійҮҸзҡ„H2еңЁеҠ зғӯжқЎд»¶дёӢиҝҳеҺҹзӣёеҗҢиҙЁйҮҸзҡ„ж··еҗҲзү©пјҢжүҖеҫ—еҲ°зҡ„й“Ғзҡ„иҙЁйҮҸдёәпјҲ пјү A.5.6gВ В В В В В В В В В В B.8.4gВ В В В В В В В В C.11.2gВ В В В В В В В В D.9.8g В В В В В В В В В В В В В В В В В В В В |
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүMgCl2гҖҒFeCl2гҖҒFe(NO3)3гҖҒKClгҖҒAl(NO3)3гҖҒNH4Clе…ӯз§Қжә¶ж¶ІпјҢз”ЁдёҖз§ҚиҜ•еүӮе°ұеҸҜд»Ҙ жҠҠе®ғ们йүҙеҲ«ејҖжқҘ,иҝҷз§ҚиҜ•еүӮжҳҜ(В В В В ) В В В В В В A.ж°ўж°§еҢ–й’ жә¶ж¶ІВ В В В В В В В В В B.KSCNжә¶ж¶ІВ В В В В В C.ж°ҜеҢ–й’ жә¶ж¶ІВ В В В В В В D.зЎқй…ё
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚ В В A.й“қе’Ңж°ўж°§еҢ–й’ ж°ҙжә¶ж¶ІеҸҚеә”пјҡ Al+2OHпјҚ+2H2O пјқAlO2пјҚ+3H2вҶ‘ В В B.жҫ„жё…зҹізҒ°ж°ҙдёҺи¶ійҮҸзҡ„е°ҸиӢҸжү“жә¶ж¶Іж··еҗҲпјҡCa2++2OH-+2HCO3-пјқCaCO3вҶ“+CO32-+2H2O В В C.зўій…ёж°ўй“өжә¶ж¶ІдёҺи¶ійҮҸзҡ„NaOHжә¶ж¶Іж··еҗҲеҗҺеҠ зғӯпјҡNH4++OHпјҚВ В В D.AlCl3жә¶ж¶Ідёӯж»ҙеҠ и¶ійҮҸж°Ёж°ҙпјҡAl3пјӢ+4NH3В·H2OпјқAlO2пјҚ+4NH4++2H2O
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
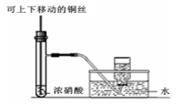
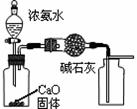
еҰӮдёӢеӣҫжүҖзӨәпјҢAгҖҒBгҖҒCжҳҜе®һйӘҢе®Өеёёз”Ёзҡ„дёүз§ҚеҲ¶еҸ–ж°”дҪ“зҡ„иЈ…зҪ®пјҢжҸҗдҫӣзҡ„иҚҜе“ҒжңүпјҡеӨ§зҗҶзҹігҖҒжө“зӣҗй…ёгҖҒй”ҢзІ’гҖҒзЁҖзӣҗй…ёгҖҒдәҢж°§еҢ–й”°гҖҒж°ҜеҢ–й“өгҖҒзҶҹзҹізҒ°гҖӮзҺ°еҲ©з”ЁиҝҷдәӣиҚҜе“ҒеҲҶеҲ«еҲ¶еҸ–NH3гҖҒCl2гҖҒH2гҖҒCO2еӣӣз§Қж°”дҪ“пјҢиҜ•еӣһзӯ”д»ҘдёӢй—®йўҳпјҡ
(1)йҖүз”ЁAиЈ…зҪ®еҸҜеҲ¶еҸ–зҡ„ж°”дҪ“жңү_____пјӣж–№зЁӢејҸдёәВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В (2)йҖүз”ЁBиЈ…зҪ®еҸҜеҲ¶еҸ–зҡ„ж°”дҪ“жңү________пјӣйҖҡеёёйҖүз”ЁCиЈ…зҪ®еҲ¶еҸ–зҡ„ж°”дҪ“жңү_________пјӣ В В дёүеҘ—иЈ…зҪ®еңЁиЈ…иҚҜе“ҒеүҚйғҪиҰҒиҝӣиЎҢВ В В В В В В В В В В В В В В В В В В зҡ„ж“ҚдҪңгҖӮ (3)ж ҮеҸ·дёәв‘ гҖҒв‘Ўзҡ„д»ӘеҷЁеҗҚз§°дҫқж¬ЎжҳҜВ В В В В В В В В В В В В гҖҒВ В В В В В В В В В В В В В В В В гҖӮ (4)еҶҷеҮәеҲ©з”ЁдёҠиҝ°жңүе…іиҚҜе“ҒеҲ¶еҸ–Cl2зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡВ В В В В В В В В В В В В В В В ________гҖӮ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
|
в… . жҹҗиҜҫеӨ–жҙ»еҠЁе°Ҹз»„дёәдәҶжЈҖйӘҢжө“зЎ«й…ёдёҺжңЁзӮӯеңЁеҠ зғӯжқЎд»¶дёӢеҸҚеә”дә§з”ҹзҡ„SO2е’ҢCO2ж°”дҪ“пјҢ В В В В В и®ҫи®ЎдәҶеҰӮеӣҫжүҖзӨәе®һйӘҢиЈ…зҪ®пјҢaгҖҒbгҖҒcдёәжӯўж°ҙеӨ№пјҢBжҳҜз”ЁдәҺеӮЁж°”зҡ„ж°”еӣҠпјҢDдёӯж”ҫжңүз”ЁI2е’Ңж·ҖзІүзҡ„
В В В В В пјҲ1пјүиЈ…зҪ®AдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ В пјҲ2пјүжӯӨе®һйӘҢжҲҗиҙҘзҡ„е…ій”®еңЁдәҺжҺ§еҲ¶еҸҚеә”дә§з”ҹж°” В В В В В В В В В В зҡ„иЈ…зҪ®пјҢеҲҷжӯЈзЎ®зҡ„ж“ҚдҪңйЎәеәҸжҳҜ В В В В В _________________пјҲз”Ёж“ҚдҪңзј–еҸ·еЎ«еҶҷпјүВ В В В В В в‘ еҗ‘AиЈ…зҪ®дёӯеҠ е…Ҙжө“зЎ«й…ёпјҢеҠ зғӯпјҢдҪҝAдёӯдә§з”ҹзҡ„ж°”дҪ“иҝӣе…Ҙж°”еӣҠBпјҢеҪ“ж°”еӣҠдёӯе……е…ҘдёҖе®ҡйҮҸ В В В В В В В ж°”дҪ“ж—¶пјҢеҒңжӯўеҠ зғӯпјӣ В В В В В в‘Ўжү“ејҖжӯўж°ҙеӨ№aе’ҢcпјҢе…ій—ӯжӯўж°ҙеӨ№bпјӣ В В В В В в‘ўеҫ…иЈ…зҪ®AеҶ·еҚҙпјҢдё”ж°”еӣҠBзҡ„дҪ“з§ҜдёҚеҶҚеҸҳеҢ–еҗҺпјҢе…ій—ӯжӯўж°ҙеӨ№aпјҢжү“ејҖжӯўж°ҙеӨ№bпјҢж…ўж…ўжҢӨеҺӢ В В В В В пјҲ3пјүе®һйӘҢж—¶пјҢиЈ…зҪ®Cдёӯзҡ„зҺ°иұЎдёәВ В В В В В В В В В В В В В пјҢиҜҘиЈ…зҪ®еҸҜд»ҘжЈҖйӘҢВ В В В В В В зҡ„з”ҹжҲҗгҖӮ В пјҲ4пјүDиЈ…зҪ®еңЁжң¬е®һйӘҢдёӯзҡ„дҪңз”ЁжҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ В пјҲ5пјүиӢҘдёәжЈҖйӘҢжө“зЎ«й…ёдёҺжңЁзӮӯеңЁеҠ зғӯжқЎд»¶дёӢз”ҹжҲҗзҡ„ж°ҙи’ёжұҪпјҢеҸҜеңЁBгҖҒCиЈ…зҪ®д№Ӣй—ҙеҠ дёҠдёҖдёӘзӣӣжңү В В В В В В В В В В В В В В В В В В В В В пјҲеЎ«иҚҜе“Ғзҡ„еҗҚз§°пјүзҡ„зЎ¬иҙЁзҺ»з’ғз®ЎгҖӮ в…ЎпјҺ CuдёҺжө“зЎ«й…ёеҸҚеә”еҸҜеҫ—зЎ«й…ёй“ңжә¶ж¶ІгҖӮжҹҗеӯҰд№ е°Ҹз»„е°Ҷй“ңеұ‘ж”ҫе…ҘдёҖе®ҡжө“еәҰзҡ„зЎ«й…ёдёӯпјҢеҠ зғӯ 并дёҚж–ӯйј“е…Ҙз©әж°”д№ҹеҸҜеҫ—зЎ«й…ёй“ңжә¶ж¶ІпјҢе…¶еҸҚеә”еҺҹзҗҶдёә2CuпјӢO2пјӢ2H2SO4 е°Ҷ19.2gй“ңе®Ңе…Ёжә¶и§ЈпјҢеҠ и’ёйҰҸж°ҙеҗҺеҫ—200 mLжә¶ж¶ІгҖӮи®Ўз®—пјҡ пјҲ6пјүеҸӮеҠ еҸҚеә”зҡ„ж°§ж°”еңЁж ҮеҮҶзҠ¶еҶөдёӢзҡ„дҪ“з§ҜжҳҜ___________________ LгҖӮ пјҲ7пјүжүҖеҫ—зЎ«й…ёй“ңжә¶ж¶Ізҡ„зү©иҙЁзҡ„йҮҸжө“еәҰжҳҜ__________________ mol/LгҖӮ
|
|
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеӣҫжҳҜдёҖдәӣдёӯеӯҰеёёи§Ғзҡ„зү©иҙЁд№Ӣй—ҙзҡ„иҪ¬еҢ–е…ізі»(е…¶дёӯйғЁеҲҶеҸҚеә”дә§зү©зңҒз•Ҙ)пјҢе…¶дёӯAе’ҢBеёёжё©дёӢйғҪжҳҜж°”дҪ“пјҢдё”ж°ҙжә¶ж¶ІйғҪжңүжјӮзҷҪжҖ§пјӣ FгҖҒM
пјҲ1пјүеҶҷеҮәдёӢеҲ—зү©иҙЁзҡ„еҢ–еӯҰејҸAВ В В В В В В гҖҒCВ В В В В В В В гҖҒIВ В В В В В В В В В В гҖҒFВ В В В В В В В В В пјҲ2пјүеҶҷеҮәеҸҚеә”в‘ зҡ„зҰ»еӯҗж–№зЁӢејҸ______________________________________ пјҲ3пјүеҶҷеҮәеҸҚеә”в‘Ўзҡ„еҢ–еӯҰж–№зЁӢејҸ_________________________________ пјҲ4пјүеңЁв‘ в‘Ўв‘ўв‘Јв‘Өв‘ҘдёӯпјҢеұһдәҺйқһж°§еҢ–иҝҳеҺҹеҸҚеә”зҡ„жңү:_______________пјҲеЎ«зј–еҸ·пјү пјҲ5пјү FеҫҲдёҚзЁіе®ҡпјҢйңІзҪ®еңЁз©әж°”дёӯе®№жҳ“иў«ж°§еҢ–дёәHпјҢиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә_____________ дҝқеӯҳ Eжә¶ж¶Іж—¶еә”еҠ е…Ҙе°‘йҮҸзҡ„_________пјҢйҳІжӯўе…¶иў«ж°§еҢ–гҖӮ пјҲ6пјүжЈҖйӘҢGжә¶ж¶ІдёӯйҳізҰ»еӯҗзҡ„ж–№жі•пјҡ________гҖҒ_______пјҲеҶҷеҮәеҠ е…ҘиҜ•еүӮзҡ„еҢ–еӯҰејҸе’ҢзҺ°иұЎпјүгҖӮ В |
|
| 26. | иҜҰз»ҶдҝЎжҒҜ |
|
зІүжң«зҠ¶иҜ•ж ·AжҳҜз”ұMgOе’ҢFe2O3з»„жҲҗзҡ„ж··еҗҲзү©гҖӮиҝӣиЎҢеҰӮдёӢе®һйӘҢпјҡ В В В В в‘ еҸ–йҖӮйҮҸAдёҺи¶ійҮҸзҡ„COеңЁй«ҳжё©дёӢеҸ‘з”ҹеҸҚеә”пјҢдә§зү©дёӯеҚ•иҙЁеҸӘжңүBз”ҹжҲҗпјӣВ в‘ЎеҸҰеҸ–20gAе…ЁйғЁжә¶дәҺ0.2L 4.5mol/Lзӣҗй…ёдёӯпјҢеҫ—еҲ°жә¶ж¶ІCпјӣ в‘ўе°Ҷв‘ дёӯеҫ—еҲ°зҡ„еҚ•иҙЁBдёҺжә¶ж¶ІCеҸҚеә”пјҢж”ҫеҮә1.12L(ж ҮеҮҶзҠ¶еҶө)ж°”дҪ“пјҢеҗҢж—¶ в‘Јз”ЁKSCNжә¶ж¶ІжЈҖйӘҢж—¶пјҢжә¶ж¶ІDдёҚеҸҳиүІгҖӮиҜ·еЎ«з©әпјҡ пјҲ1пјүв‘ дёӯдёҺCOеҸ‘з”ҹеҸҚеә”зҡ„зү©иҙЁжҳҜВ В В В В В В В В В В В В гҖӮ пјҲ2пјүв‘ЎдёӯжүҖеҸ‘з”ҹзҡ„еҗ„еҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ пјҲ3пјүжҢүв‘ўдёӯжүҖеҸ‘з”ҹзҡ„еҗ„еҸҚеә”зҡ„е…ҲеҗҺйЎәеәҸеҶҷзҰ»еӯҗж–№зЁӢејҸВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ В В пјҲ4пјүиӢҘжә¶ж¶ІDзҡ„дҪ“з§Ҝд»Қи§Ҷдёә0.2LпјҢеҲҷиҜҘжә¶ж¶Ідёӯc(Mg2пјӢ)=В В В В В В В В В пјҢc(Fe2пјӢ)=В В В В В В В В В гҖӮ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В
|
|
- зҰҸе»әзңҒеҚ—е№іеёӮ2020-2021е№ҙй«ҳдәҢдёҠжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·еңЁзәҝжЈҖжөӢ
- еӨ§йҖҡеӣһж—Ҹеңҹж—ҸиҮӘжІ»еҺҝ第дёҖе®Ңе…ЁдёӯеӯҰ2019е№ҙй«ҳдәҢдёӢеҶҢеҢ–еӯҰжңҹдёӯиҖғиҜ•иҜ•еҚ·еёҰи§ЈжһҗеҸҠзӯ”жЎҲ
- й«ҳдёҖдёҠжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·пјҲ2019-2020е№ҙж№–еҚ—зңҒй•ҝжІҷеёӮйӣЁиҠұеҢәпјү
- 2020еұҠй«ҳиҖғеҢ–еӯҰе°ҸйўҳзӢӮз»ғдё“з»ғ14 еҢ–еӯҰе№іиЎЎ
- 2019-2020е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰиҖғиҜ•пјҲдә‘еҚ—зңҒзҺүжәӘеёӮжұҹе·қеҢәдәҢдёӯпјү
- й«ҳдёүеҢ–еӯҰдёҠеҶҢдё“йўҳз»ғд№ иҖғиҜ•е®Ңж•ҙзүҲ
- жұҹиҘҝзңҒж–°дҪҷеёӮ第еӣӣдёӯеӯҰ2021еұҠй«ҳдёүеҢ–еӯҰдёҠеҚҠе№ҙ第еӣӣж¬ЎиҖғиҜ•иҜ•еҚ·еңЁзәҝз»ғд№
- 2019еұҠй«ҳдёүдёҠеҶҢжңҹдёӯиҖғиҜ•зҗҶ科综еҗҲеҢ–еӯҰе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲпјҲж№–еҢ—зңҒй„Ӯе·һеёӮпјү

 В В В В В В В В В В В В В В В В В В В
В В В В В В В В В В В В В В В В В В В 







