高二上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
2008年9月27日16﹕43,中国人走出由中国人自主研制的航天飞船,进行包括科学实验在内的出舱活动。标志着中国已经成为世界上继俄、美之后第三个能够进行飞船舱外活动的国家。在飞船的火箭推进器中常装有液态肼(用A表示)和过氧化氢(H2O2),它们混合时的反应方程式为:2H2O2+A=N2+4H2O,则肼(A)的化学式为 A.N2H2 B.N2H4 C.NH2 D.N2H4O2
|
|
| 2. | 详细信息 |
|
下列有关阿佛加德罗常数(NA)的说法错误的是 A.32克O2所含的原子数目为2NA B.0.5L 0.2mol/L的NaCl(aq)中含有的Na+数是0.1NA C.标准状况下,22.4L水中含有NA个水分子 D.0.5NA个氯气分子的物质的量是0.5mol
|
|
| 3. | 详细信息 |
|
从原子序数11依次增加到17,下列所叙述的递变关系错误的是 A.电子层数逐渐增多 B. 原子半径逐渐减小 C. 最高正价数值逐渐增大 D. 从硅到氯负价从–4→–1
|
|
| 4. | 详细信息 |
|
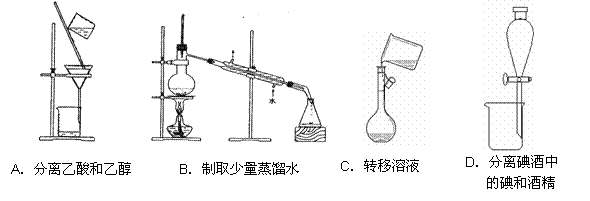
图中三位同学正在讨论某一物质,他们所描述的物质是 A.HCl B.SO2 C.NO2 D. Cl2
|
|
| 5. | 详细信息 |
|
合理使用药物有利身心健康。下列有关说法错误的是 A.氢氧化铝用于治疗胃酸过多 B.非处方药都无毒副作用,可长期大量服用 C.医用酒精用于解热镇痛 D.阿司匹林用于解热镇痛
|
|
| 6. | 详细信息 |
|
下列反应中,属于取代反应的是 C.苯的硝化反应 D.乙烯与溴的四氯化碳溶液反应
|
|
| 7. | 详细信息 |
|
我国著名的化学家、教育家徐光宪先胜因在稀土金属等研究领域做出杰出贡献,荣获了2008年度“国家最高科学技术奖”。 A.质量数为140 B 中子数为82 C.质子数为58 D 核外电子数为198
|
|
| 8. | 详细信息 |
|
对氯化铁溶液和氢氧化铁胶体的说法正确的是 A.分散系颗粒直径都在1~100nm之间 B.能透过半透膜 C 呈红褐色 D.用丁达尔效应可以鉴别
|
|
| 9. | 详细信息 |
|
下列离子在溶液中可大量共存,形成无色透明溶液的一组是 A.K+、Na+、OH-、Cl- B.Ba2+、Cu2+、NO3-、SO42- C.Mg2+、Na+、OH-、SO42- D.H+、Ba2+、NO3-、OH-
|
|
| 10. | 详细信息 |
|
下列说法正确的是 A.物质的量是一种国际基本物理量 B.标准状况下气体摩尔体积约为22.4L C.1mol氧的质量为16g D.在同温同压下相同体积任何气体单质所含原子数相同
|
|
| 11. | 详细信息 |
|
下列操作中,溶液的颜色不发生变化的是 A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液 C.铁丝置于氯化铜溶液中一段时间 D.氯化铁溶液中加入还原性铁粉
|
|
| 12. | 详细信息 |
|
下列操作不能用于检验 A.气体使湿润的酚酞试纸变红 B.气体能使湿润的红色石蕊试纸变蓝 C.气体与浓H2SO4靠近 D.气体与浓盐酸产生白烟
|
|
| 13. | 详细信息 |
|
|
|
| 14. | 详细信息 |
|
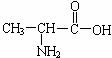
一种二肽的结构简式为: A. C.
|
|
| 15. | 详细信息 |
|
下列物质中,不属于高分子化合物的是 A.纤维素 B.蛋白质 C.油脂 D.塑料
|
|
| 16. | 详细信息 | |||||||||||||||||||||||||
|
下列除去杂质的方法正确的是
|
||||||||||||||||||||||||||
| 17. | 详细信息 |
|
下列各项中表达正确的是 A.F原子结构示意图: C.H、D、T表示同一种核素 D.CH4分子的球棍模型:
|
|
| 18. | 详细信息 |
|
下列反应的离子方程式正确的是 A.向NaOH溶液中加入铝粉来制备H2:Al+2OH-+2H2O===AlO2-+3H2↑ B.用胃舒平治疗胃酸过多:Al(OH)3+3H+===Al3++3H2O C.实验室用氢氧化钠溶液吸收Cl2:Cl2 +OH- === Cl- + ClO-+ H2O D.碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑
|
|
| 19. | 详细信息 |
|
下列情况中,会对人体健康造成较大危害的是 A用SO2漂白食品 B.用小苏打发酵面团制作馒头 C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) D.自来水中通入少量Cl2进行杀菌消毒
|
|
| 20. | 详细信息 |
|
下列反应中,属于吸热反应的是 A.稀硫酸与氢氧化钾溶液反应 B.氢气还原氧化铜的反应 C.锌与稀盐酸反应 D.生石灰变成熟石灰的反应
|
|
| 21. | 详细信息 |
|
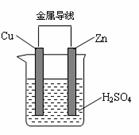
右图为原电池示意图,下列说法中正确的是 A.锌片是正极 B.铜片是负极 C.电子由锌片通过导线流向铜片 D.该装置能够将电能转化为化学能
|
|
| 22. | 详细信息 |
|
在一条件下,反应N2+3H2 A.1.2mol/(L·min) B.1.0 mol/(L·min) C.0.6 mol/(L·min) D.0.4 mol/(L·min)
|
|
| 23. | 详细信息 |
|
为了验证食盐的的主要成分,将食盐溶于水,然后进行焰色反应,焰色呈黄色,说明含有__________离子;往食盐溶液中加入AgNO3溶液和稀HNO3,有白色沉淀产生,说明含有___________离子。
|
|
| 24. | 详细信息 |
|
(1)现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素, F.阿司匹林 请按下列要求填空(填序号)。 富含维生素C的是 ;可直接进入血液,补充能量的是 ;应用最广泛的抗生素之一的是 ;既可作为调味剂,又可作为防腐剂的是 ;食用过多会引起血压升高、肾脏受损的 ,使用最早的解热镇痛药 。 (2)蛋白质缺乏是可以致命的。人体内蛋白质约占体重的16%。一个体重为60kg的人,体内含有10~11kg的蛋白质。如果人体丢失体内20%以上的蛋白质,生命活动有可能会被迫停止。常见的蛋白质缺乏症表现为代谢下降,生命变得脆弱易病。蛋白质的生理功能与它的化学性质密切相关。人体摄入的蛋白质,在酶的催化作用下发生水解,最终生成氨基酸。这些氨基酸一部分重新合成人体所需的蛋白质、糖或脂类物质,以满足生命活动的需要;另一部分则发生氧化反应,释放能量。 ①蛋白质溶液遇到浓的硫酸铵等无机盐溶液,会析出沉淀;再加适量水后,蛋白质重新溶解,仍然具有原来的活性。这个过程称为 。 ②蛋白质遇到酸、碱、重金属盐、乙醇等化学物质时会发生凝结,失去原来的活性,这个变化称为 。
|
|
| 25. | 详细信息 |
|
配制100mL 0.1mol/L的盐酸溶液,必须选用规格为100mL的__________(填仪器名称);中和上述盐酸溶液25mL需0.1mol/L NaOH溶液___________mL。
|
|
| 26. | 详细信息 |
|
在标准状况下,1mol任何气体的体积都约为___________L,28gCO在标准状况下的体积约为______________L。
|
|
| 27. | 详细信息 |
|
乙酸是生活中的一种常见有机物,
(1)乙酸分子中-COOH原子团的名称是___________, 乙醇分子中的官能团是___________(写结构简式) (2)乙酸与 (3)一定条件下,乙酸能与乙醇发生反应成一种具有香味的油状液体, 该有机反应的类型是___________反应。 请写出反应的化学方程式(不要求写反应条件) ____________________________________________________________。
|
|
| 28. | 详细信息 | ||||||||||||||||||||||||||||||||||||
|
下表列出了①~⑥六种元素在周期表中的位置:
请按要求回答下列问题。 (1)元素①的元素符号是 。 (2)元素②的单质电子式是 。 (3)元素⑤的原子结构示意图是 。 (4)这六种元素中,位于第三周期且原子半径最小的是(填元素符号) 。 (5)这六种元素的最高价氧化物中,属于两性氧化物的是(填化学式) 。 (6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为: ;向上述反应后的溶液中再加入元素④的单质,发生反应的化学方程式为: 。
|
|||||||||||||||||||||||||||||||||||||
| 29. | 详细信息 | ||||||||||
|
为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中。
供选择的化学试剂: A.酸性高锰酸钾B.硝酸银溶液和硝酸C.氢氧化钠溶液D.无水硫酸铜粉末
|
|||||||||||
| 30. | 详细信息 | |||
|
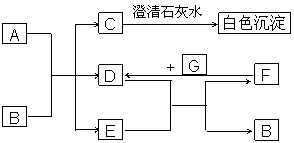
下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系。其中A、G为非金属单质,A为黑色固体、G为气态;D、F都是大气污染物,主要来源于汽车尾气,而且D为红棕色。
请回答以下问题: ⑴A的元素在元素周期表中位于 ,C的化学式是_______________。 ⑵写出D与E反应转化为F和B的化学方程式_________________________________。 ⑶在常温下,B的稀溶液也可与Cu反应生成F。此反应的离子方程式:
|
||||
| 31. | 详细信息 |
|
开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责。请回答下面关于海洋的几个问题:
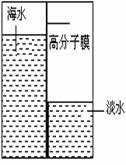
(2)海水中资源丰富,含量最多的金属阳离子是 (填符号),含量最多的分子是 (填分子式)。 (3)海水淡化是国际上研究的热点问题,我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩。如图,左侧为海水,右侧为经过一段时间后由左侧经高分子膜渗透得到的淡水,该变化是 变化(填“物理”或“化学”)。
|
|


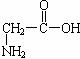
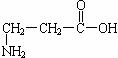 B
B