2020安徽高二上学期人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
在日常生活中,与化学反应速率无关的做法是: A.用热水溶解蔗糖以加速溶解 B.把块状煤碾成粉状再燃烧 C.真空包装食品以延长保质期 D.低温冷藏使食品延缓变质
|
|
| 2. | 详细信息 |
|
将FeCl3溶液和KI溶液混合,发生反应: 2Fe3+(aq)+2I-(aq) 下列各项能判断上述可逆反应达到平衡状态的是: A.c(Fe3+)与c(Fe2+)之和不再变化 B.c(K+)不再变化 C.溶液颜色不再变化 D.v正(I-)=2v正(I2)
|
|
| 3. | 详细信息 |
|
向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小顺序排列正确的是: 甲.在500 ℃时,10 mol SO2和10 mol O2 乙.在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2 丙.在450 ℃时,8 mol SO2和5 mol O2 丁.在500 ℃时,8 mol SO2和5 mol O2 A.乙、甲、丁、丙 B.乙、甲、丙、丁 C.甲、乙、丙、丁 D.丁、丙、乙、甲
|
|
| 4. | 详细信息 |
|
已知下列反应的平衡常数:①H2(g)+S(s) A.K1+K2 B.K1−K2 C.K1×K2 D.K1/K2
|
|
| 5. | 详细信息 |
|
下列说法中,可以证明反应N2(g)+3H2 (g) A.1个N≡N键断裂的同时,有3个H—H键形成 B.1个N≡N键断裂的同时,有3个H—H键断裂 C.3个H—H键形成的同时,有6个N—H键断裂 D.1个N≡N键断裂的同时,有6个N—H键形成
|
|
| 6. | 详细信息 | |||||||||||||||
|
一定条件下,可逆反应2A(g)
|
||||||||||||||||
| 7. | 详细信息 |
|
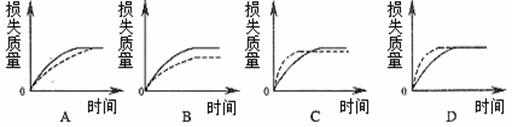
将A g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将B g粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是(已知A>B):
|
|
| 8. | 详细信息 | |||
|
对于反应,N2O4(g)
|
||||
| 9. | 详细信息 |
|
密闭容器中N2与H2合成NH3的反应可以表示为: N2+3H2 1/2N2+3/2H2 下列说法正确的是( ) A.两个化学方程式的化学平衡常数相同 B.两个化学方程式表示的意义相同 C.①和②的化学平衡常数单位相同 D ①和②的化学平衡常数互为倒数
|
|
| 10. | 详细信息 |
|
将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g) ②2 s内用物质A表示的平均反应速率______________ ⑤该反应的平衡常数为____________(保留两位有效数字)
|
|
| 11. | 详细信息 | ||||||||||||
|
已知A(g)+B(g)
回答下列问题: (1)该反应的平衡常数表达式K= , (2)900℃时,向一个固定容器为2L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始到2s内A浓度变化0.05mol·L−1.则A的平均反应速率v(A)= ______ .该反应达到平衡时A的转化率为 ______ (3)判断反应是否达到平衡的依据为 ______ (填字母代号)。 a.压强不随时间改变 b.气体的密度不随时间改变 c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等 (4)1200℃时,若向另一相同容器中充入0.30molA、0.40mol B、0.40mol C和0.50molD,此时v正 ______ v逆(填”大于“、”小于“或”等于“)。
|
|||||||||||||
| 12. | 详细信息 |
|
在2L密闭容器中,将2mol CO与10mol H2O混合加热到800℃,达到下列平衡: CO(g)+H2O(g)⇌CO2(g)+H2(g) K=1.0, 求:(1)平衡时氢气的物质的量是多少? (2)CO的转化率为是多少?(写出解题过程)
|
|