2018ж№–еҢ—й«ҳдәҢдёӢеӯҰжңҹдәәж•ҷзүҲй«ҳдёӯеҢ–еӯҰеҗҢжӯҘз»ғд№
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
2017е№ҙдё–з•ҢзҺҜеўғж—ҘжҲ‘еӣҪзҡ„дё»йўҳдёә"з»ҝж°ҙйқ’еұұе°ұжҳҜйҮ‘еұұ银еұұвҖқгҖӮдёӢеҲ—иҜҙжі•еә”иҜҘжҸҗеҖЎзҡ„жҳҜ( гҖҖ) AпјҺжҺЁе№ҝдҪҝз”Ёз”өеӯҗж”Ҝд»ҳВ В В BпјҺзҰҒжӯўдҪҝз”ЁеЎ‘ж–ҷеҲ¶е“Ғ CпјҺжҷ®еҸҠдҪҝ用家еәӯиҪҝиҪҰВ В В DпјҺеЎ«еҹӢеӨ„зҗҶеәҹж—§з”өжұ
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…іжңүжңәеҢ–еҗҲзү©зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺвҖңең°жІҹжІ№вҖқвҖңеЎ‘еҢ–еүӮвҖқеқҮеұһдәҺй«ҳеҲҶеӯҗеҢ–еҗҲзү©пјҢйғҪеҜ№еҒҘеә·жңүе®і BпјҺзҹіжІ№зҡ„иЈӮеҢ–е’Ңз…Өзҡ„е№ІзҶҳйғҪеұһдәҺеҢ–еӯҰеҸҳеҢ– CпјҺзӯүиҙЁйҮҸзҡ„и‘Ўиҗ„зі–е’Ңжһңзі–еңЁдәәдҪ“еҶ…е®Ңе…Ёж°§еҢ–йҮҠж”ҫзҡ„иғҪйҮҸзӣёзӯү DпјҺиҒҡж°Ҝд№ҷзғҜеҲ¶е“Ғжҳ“йҖ жҲҗзҷҪиүІжұЎжҹ“пјҢеҸҜйҮҮз”Ёз„ҡзғ§жі•еӨ„зҗҶ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗж°”жҖҒзҡ„зғ·зғғдёҺзғҜзғғзҡ„ж··еҗҲж°”дҪ“9 gпјҢе…¶еҜҶеәҰдёәеҗҢзҠ¶еҶөдёӢH2еҜҶеәҰзҡ„11.25еҖҚпјҢе°Ҷж··еҗҲж°”дҪ“йҖҡиҝҮи¶ійҮҸзҡ„жәҙж°ҙпјҢжәҙж°ҙеўһйҮҚ4.2 gпјҢеҲҷеҺҹж··еҗҲж°”дҪ“зҡ„з»„жҲҗдёә(гҖҖгҖҖ)В AпјҺз”Ізғ·пјҢд№ҷзғҜВ В В BпјҺд№ҷзғ·пјҢд№ҷзғҜВ В В CпјҺз”Ізғ·пјҢдёҷзғҜВ В В DпјҺз”Ізғ·пјҢдёҒзғҜ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ(гҖҖгҖҖ) A.зҹіжІ№дёӯеҗ«жңүC5пҪһC11зҡ„зғ·зғғпјҢйҖҡиҝҮзҹіжІ№зҡ„еҲҶйҰҸеҸҜеҫ—еҲ°жұҪжІ№ B.еҗ«C20д»ҘдёҠзҡ„йҮҚжІ№з»ҸеӮ¬еҢ–иЈӮеҢ–еҸҜд»Ҙеҫ—еҲ°жұҪжІ№ C.ејҖйҮҮеӨ©з„¶ж°”еә”еҒҡеҲ°е®ү全规иҢғең°ж“ҚдҪң D.з…Өдёӯеҗ«жңүиӢҜе’Ңз”ІиӢҜпјҢеҸҜз”ЁеҲҶйҰҸзҡ„ж–№жі•жҠҠе®ғ们еҲҶзҰ»еҮәжқҘ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ЁеӣәжҖҒй”ӮзЎ«з”өжұ иғҪйҮҸеҜҶеәҰй«ҳгҖҒжҲҗжң¬дҪҺпјҢе…¶е·ҘдҪңеҺҹзҗҶеҰӮеӣҫжүҖзӨәпјҢе…¶дёӯз”өжһҒaеёёз”ЁжҺәжңүзҹіеўЁзғҜзҡ„S8жқҗж–ҷпјҢз”өжұ еҸҚеә”дёәпјҡ16LiпјӢxS8===8Li2Sx(2вүӨxвүӨ8)гҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ(гҖҖгҖҖ)
AпјҺз”өжұ е·ҘдҪңж—¶пјҢжӯЈжһҒеҸҜеҸ‘з”ҹеҸҚеә”пјҡ2Li2S6пјӢ2LiпјӢпјӢ2eпјҚ===3Li2S4 BпјҺз”өжұ е·ҘдҪңж—¶пјҢеӨ–з”өи·ҜдёӯжөҒиҝҮ0.02 molз”өеӯҗпјҢиҙҹжһҒжқҗж–ҷеҮҸйҮҚ0.14 g CпјҺзҹіеўЁзғҜзҡ„дҪңз”Ёдё»иҰҒжҳҜжҸҗй«ҳз”өжһҒaзҡ„еҜјз”өжҖ§ DпјҺз”өжұ е……з”өж—¶й—ҙи¶Ҡй•ҝпјҢз”өжұ дёӯLi2S2зҡ„йҮҸи¶ҠеӨҡ
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗзғғжңүдёӨз§ҚжҲ–дёӨз§Қд»ҘдёҠзҡ„еҗҢеҲҶејӮжһ„дҪ“пјҢе…¶дёӯдёҖз§Қзғғзҡ„дёҖж°Ҝд»Јзү©еҸӘжңүдёҖз§ҚпјҢеҲҷиҝҷз§ҚзғғеҸҜиғҪжҳҜ(гҖҖгҖҖ)В в‘ еҲҶеӯҗдёӯеҗ«7дёӘзўіеҺҹеӯҗзҡ„иҠійҰҷзғғВ В В в‘ЎеҲҶеӯҗдёӯеҗ«4дёӘзўіеҺҹеӯҗзҡ„зғ·зғғ в‘ўеҲҶеӯҗдёӯеҗ«6дёӘзўіеҺҹеӯҗзҡ„еҚ•зғҜзғғВ В В в‘ЈеҲҶеӯҗдёӯеҗ«8дёӘзўіеҺҹеӯҗзҡ„зғ·зғғ AпјҺв‘ўв‘Ј В В BпјҺв‘Ўв‘ўВ В CпјҺв‘ в‘ЎВ DпјҺв‘Ўв‘Ј
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||||||
|
дёәдәҶжҺўз©¶жё©еәҰгҖҒзЎ«й…ёй“ңеҜ№й”ҢдёҺзЁҖзЎ«й…ёеҸҚеә”йҖҹзҺҮзҡ„еҪұе“Қ规еҫӢпјҢжҹҗеҗҢеӯҰи®ҫи®ЎеҰӮдёӢж–№жЎҲпјҡ
дёӢеҲ—жҺЁж–ӯеҗҲзҗҶзҡ„жҳҜ(гҖҖгҖҖ) AпјҺдёәдәҶйҖүжӢ©в…Ўе’Ңв…ўе®һйӘҢжҺўз©¶зЎ«й…ёй“ңеҜ№еҸҚеә”йҖҹзҺҮзҡ„еҪұе“ҚпјҢеҝ…йЎ»жҺ§еҲ¶tпјқ25 BпјҺеҫ…жөӢзү©зҗҶйҮҸжҳҜ收йӣҶзӯүдҪ“з§Ҝ(зӣёеҗҢжқЎд»¶)ж°”дҪ“жүҖйңҖиҰҒзҡ„ж—¶й—ҙпјҢж—¶й—ҙи¶Ҡй•ҝпјҢеҸҚеә”и¶Ҡеҝ« CпјҺж №жҚ®иҜҘж–№жЎҲпјҢиҝҳеҸҜд»ҘжҺўз©¶зЎ«й…ёжө“еәҰеҜ№еҸҚеә”йҖҹзҺҮзҡ„еҪұе“Қ DпјҺж №жҚ®иҜҘе®һйӘҢж–№жЎҲеҫ—еҮәеҸҚеә”йҖҹзҺҮеӨ§е°ҸеҸҜиғҪжҳҜв…ў>в…Ў>в… >в…Ј
|
||||||||||||||||||||||||||
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
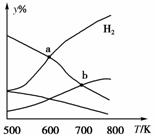
д»ҘдәҢж°§еҢ–зўіе’Ңж°ўж°”дёәеҺҹж–ҷеҲ¶еҸ–д№ҷйҶҮзҡ„еҸҚеә”дёәпјҡ2CO2(g)пјӢ6H2 (g)
AпјҺaзӮ№зҡ„е№іиЎЎеёёж•°е°ҸдәҺbзӮ№В В В В В В В В В В BпјҺbзӮ№пјҢvжӯЈ(CO2)пјқvйҖҶ(H2O) CпјҺaзӮ№пјҢH2е’ҢH2Oзү©иҙЁзҡ„йҮҸзӣёзӯүВ В В В В DпјҺе…¶д»–жқЎд»¶жҒ’е®ҡпјҢе……е…ҘжӣҙеӨҡH2пјҢv(CO2)дёҚеҸҳ
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
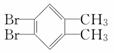
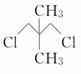
жңүдёӨз§Қжңүжңәзү©Q( AпјҺдәҢиҖ…зҡ„ж ёзЈҒе…ұжҢҜж°ўи°ұдёӯеқҮеҸӘеҮәзҺ°дёӨз§Қеі°дё”еі°йқўз§Ҝд№ӢжҜ”дёә3вҲ¶2 BпјҺдәҢиҖ…еңЁNaOHйҶҮжә¶ж¶ІдёӯеқҮеҸҜеҸ‘з”ҹж¶ҲеҺ»еҸҚеә” CпјҺдёҖе®ҡжқЎд»¶дёӢпјҢдәҢиҖ…еңЁNaOHжә¶ж¶ІдёӯеқҮеҸҜеҸ‘з”ҹеҸ–д»ЈеҸҚеә” DпјҺQзҡ„дёҖж°Ҝд»Јзү©еҸӘжңү1з§ҚпјҢPзҡ„дёҖжәҙд»Јзү©жңү2з§Қ
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ғзҙ вҖңж°ҰгҖҒй“·гҖҒй“ҜвҖқзӯүжҳҜз”ЁдёӢеҲ—е“Әз§Қ科еӯҰж–№жі•еҸ‘зҺ°зҡ„(гҖҖгҖҖ) AпјҺзәўеӨ–е…үи°ұВ В В BпјҺиҙЁи°ұВ В В В CпјҺеҺҹеӯҗе…үи°ұВ В DпјҺж ёзЈҒе…ұжҢҜи°ұ
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺжүҖжңүйқһйҮ‘еұһе…ғзҙ йғҪеҲҶеёғеңЁpеҢә BпјҺжңҖеӨ–еұӮз”өеӯҗж•°дёә2зҡ„е…ғзҙ йғҪеҲҶеёғеңЁsеҢә CпјҺе…ғзҙ е‘ЁжңҹиЎЁдёӯ第ⅢBж—ҸеҲ°з¬¬в…ЎBж—Ҹ10дёӘзәөиЎҢзҡ„е…ғзҙ йғҪжҳҜйҮ‘еұһе…ғзҙ DпјҺеҗҢдёҖдё»ж—Ҹе…ғзҙ д»ҺдёҠеҲ°дёӢпјҢйҮ‘еұһжҖ§е‘Ҳе‘ЁжңҹжҖ§еҸҳеҢ–
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
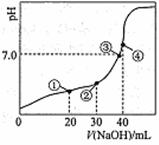
AпјҺзӮ№в‘ гҖҒв‘ўгҖҒв‘ЈжүҖзӨәжә¶ж¶ІдёӯпјҢзӮ№в‘ўжүҖзӨәжә¶ж¶ІH2Oзҡ„з”өзҰ»зЁӢеәҰжңҖе°Ҹ BпјҺзӮ№в‘ЎжүҖзӨәжә¶ж¶Ідёӯпјҡ2c(H+)+c(HC2O4-)+3c(H2C2O4)=2c(OH-)+c(C2O42-) CпјҺзӮ№в‘ўжүҖзӨәжә¶ж¶Ідёӯпјҡc(HC2O4-)+2c(C2O42-)=2c(Na+) DпјҺж»ҙе®ҡиҝҮзЁӢдёӯеҸҜиғҪеҮәзҺ°пјҡc(Na+)>c(HC2O4-)=c(C2O42-)>c(OH-)>c(H+)
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
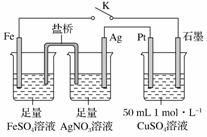
жҹҗе°Ҹз»„з”ЁеҰӮеӣҫиЈ…зҪ®иҝӣиЎҢе®һйӘҢпјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ(гҖҖ) AпјҺзӣҗжЎҘдёӯзҡ„з”өи§ЈиҙЁеҸҜд»Ҙз”ЁKCl BпјҺй—ӯеҗҲKпјҢзҹіеўЁз”өжһҒдёҠеҸӘз”ҹжҲҗй“ң CпјҺй—ӯеҗҲKпјҢз”өеӯҗжөҒеҠЁж–№еҗ‘дёәAgз”өжһҒвҶ’зӣҗжЎҘвҶ’Feз”өжһҒ
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
е®Өжё©дёӢпјҢе°Ҷ0.05 mol Na2CO3еӣәдҪ“жә¶дәҺж°ҙй…ҚжҲҗ100 mLжә¶ж¶ІпјҢеҗ‘жә¶ж¶ІдёӯеҠ е…ҘдёӢеҲ—зү©иҙЁпјҢжңүе…із»“и®әжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ)В
|
||||||||||||||||
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүе…ізі–зұ»зү©иҙЁзҡ„еҸҷиҝ°дёӯжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺзі–зұ»зү©иҙЁеҸҲеҸ«зўіж°ҙеҢ–еҗҲзү©пјҢе…¶еҲҶеӯҗејҸйғҪеҸҜз”ЁCm(H2O)nиЎЁзӨә BпјҺзі–зұ»дёҖиҲ¬жҳҜеӨҡзҫҹеҹәйҶӣжҲ–еӨҡзҫҹеҹәй…®пјҢд»ҘеҸҠиғҪж°ҙи§Јдә§з”ҹе®ғ们зҡ„зү©иҙЁ CпјҺи‘Ўиҗ„зі–гҖҒи”—зі–гҖҒж·ҖзІүйғҪиғҪеҸ‘з”ҹж°ҙи§ЈеҸҚеә” DпјҺи”—зі–ж°ҙи§ЈеҗҺеҗ‘ж··еҗҲж¶ІдёӯеҠ е…Ҙж–°еҲ¶Cu(OH)2жӮ¬жөҠж¶ІпјҢеҠ зғӯеҗҺеҸҜеҫ—зәўиүІжІүж·Җ
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
пјҺдёӢеҲ—еҜ№ж°Ёеҹәй…ёе’ҢиӣӢзҷҪиҙЁзҡ„жҸҸиҝ°жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺиӣӢзҷҪиҙЁж°ҙи§Јзҡ„жңҖз»Ҳдә§зү©жҳҜж°Ёеҹәй…ё BпјҺж°Ёеҹәй…ёе’ҢиӣӢзҷҪиҙЁйҒҮйҮҚйҮ‘еұһзҰ»еӯҗеқҮдјҡеҸҳжҖ§ CпјҺОұВӯж°Ёеҹәдёҷй…ёдёҺОұВӯж°ЁеҹәиӢҜдёҷй…ёж··еҗҲзү©и„ұж°ҙжҲҗиӮҪпјҢеҸӘз”ҹжҲҗ2з§ҚдәҢиӮҪ DпјҺж°Ёеҹәй…ёжә¶дәҺиҝҮйҮҸж°ўж°§еҢ–й’ жә¶ж¶Ідёӯз”ҹжҲҗзҡ„зҰ»еӯҗпјҢеңЁз”өеңәдҪңз”ЁдёӢеҗ‘иҙҹжһҒ移еҠЁ
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҷиҝ°й”ҷиҜҜзҡ„жҳҜ(гҖҖгҖҖ)В AпјҺз”ЁйҮ‘еұһй’ еҸҜеҢәеҲҶд№ҷйҶҮе’Ңд№ҷйҶҡВ В В В В В BпјҺз”Ёй…ёжҖ§й«ҳй”°й…ёй’ҫжә¶ж¶ІеҸҜеҢәеҲҶе·ұзғ·е’Ң3Вӯе·ұзғҜ CпјҺз”Ёж°ҙеҸҜеҢәеҲҶиӢҜе’ҢжәҙиӢҜВ В В В В В В В В В В В DпјҺз”Ёж–°еҲ¶зҡ„银氨жә¶ж¶ІеҸҜеҢәеҲҶз”Ій…ёз”Ій…Ҝе’Ңд№ҷйҶӣ
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
еҲҶеӯҗејҸдёәC5H10O2зҡ„жңүжңәзү©еңЁй…ёжҖ§жқЎд»¶дёӢеҸҜж°ҙи§Јдёәй…ёе’ҢйҶҮпјҢиӢҘдёҚиҖғиҷ‘з«ӢдҪ“ејӮжһ„пјҢиҝҷдәӣйҶҮе’Ңй…ёйҮҚж–°з»„еҗҲеҸҜеҪўжҲҗзҡ„й…Ҝе…ұжңү(гҖҖгҖҖ) AпјҺ15з§ҚВ В В В BпјҺ28з§ҚВ В В В В В CпјҺ32з§ҚВ В В В DпјҺ40з§Қ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
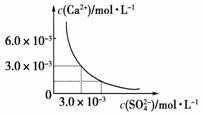
AпјҺжә¶ж¶ІдёӯжһҗеҮәCaSO4еӣәдҪ“жІүж·ҖпјҢжңҖз»Ҳжә¶ж¶Ідёӯc(SO42-)жҜ”еҺҹжқҘзҡ„еӨ§ BпјҺжә¶ж¶Ідёӯж— жІүж·ҖжһҗеҮәпјҢжә¶ж¶Ідёӯc(Ca2пјӢ)гҖҒc(SO42-)йғҪеҸҳе°Ҹ CпјҺжә¶ж¶ІдёӯжһҗеҮәCaSO4еӣәдҪ“жІүж·ҖпјҢжә¶ж¶Ідёӯc(Ca2пјӢ)гҖҒc(SO42-)йғҪеҸҳе°Ҹ DпјҺжә¶ж¶Ідёӯж— жІүж·ҖжһҗеҮәпјҢдҪҶжңҖз»Ҳжә¶ж¶Ідёӯc(SO42-)жҜ”еҺҹжқҘзҡ„еӨ§
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺжңүжңәеҢ–еҗҲзү©зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺзі–зұ»гҖҒжІ№и„ӮгҖҒиӣӢзҷҪиҙЁйғҪеұһдәҺеӨ©з„¶й«ҳеҲҶеӯҗеҢ–еҗҲзү© BпјҺеҲҶеӯҗејҸдёәC2H6OгҖҒC4H10зҡ„жңүжңәзү©йғҪжңү2з§ҚеҗҢеҲҶејӮжһ„дҪ“ CпјҺд№ҷзғҜе’ҢиӢҜйғҪиғҪдҪҝй…ёжҖ§KMnO4жә¶ж¶ІиӨӘиүІ DпјҺеҸҜз”Ёзғӯзҡ„NaOHжә¶ж¶ІйҷӨеҺ»д№ҷй…ёд№ҷй…Ҝдёӯзҡ„д№ҷй…ёжқӮиҙЁ
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
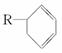
жҢүиҰҒжұӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1) (2) (3)жҹҗзғғзҡ„еҲҶеӯҗејҸдёәC4H4пјҢе®ғжҳҜеҗҲжҲҗж©Ўиғ¶зҡ„дёӯй—ҙдҪ“пјҢе®ғжңүеӨҡз§ҚеҗҢеҲҶејӮжһ„дҪ“гҖӮ в‘ иҜ•еҶҷеҮәе®ғзҡ„дёҖз§Қй“ҫејҸз»“жһ„зҡ„еҗҢеҲҶејӮжһ„дҪ“зҡ„з»“жһ„з®ҖејҸ____________________гҖӮ в‘Ўе®ғжңүдёҖз§ҚеҗҢеҲҶејӮжһ„дҪ“пјҢжҜҸдёӘзўіеҺҹеӯҗеқҮиҫҫйҘұе’ҢпјҢдё”зўідёҺзўізҡ„еӨ№и§’зӣёеҗҢпјҢиҜҘеҲҶеӯҗдёӯзўіеҺҹеӯҗеҪўжҲҗзҡ„з©әй—ҙжһ„еһӢдёә____________еҪўгҖӮ (4)еҢ–еҗҲзү©AжҳҜеҗҲжҲҗеӨ©з„¶ж©Ўиғ¶зҡ„еҚ•дҪ“пјҢеҲҶеӯҗејҸдёәC5H8гҖӮAзҡ„з»“жһ„з®ҖејҸдёәпјҲжҸҗзӨәпјҡжңүз”Іеҹәж”Ҝй“ҫзҡ„дәҢзғҜзғғпјү____________________гҖӮ (5)еҶҷеҮә
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
В (1) зӯүзү©иҙЁзҡ„йҮҸжө“еәҰзҡ„дёӢеҲ—жә¶ж¶ІдёӯпјҢв‘ NH4ClВ В в‘ЎNH4HCO3 в‘ў NH4HSO4 в‘Ј (NH4)2SO4В pHз”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜ(еЎ«зј–еҸ·пјҢдёӢеҗҢ)__________________пјӣNH4+зҡ„жө“еәҰз”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜ_____________
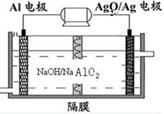
(3)й“қз”өжұ жҖ§иғҪдјҳи¶ҠпјҢAlВӯAg2Oз”өжұ еҸҜз”ЁдҪңж°ҙдёӢеҠЁеҠӣз”өжәҗпјҢе…¶еҺҹзҗҶеҰӮеӣҫжүҖзӨәгҖӮ в‘ жӯӨз”өжұ зҡ„иҙҹжһҒз”өжһҒеҸҚеә”ејҸжҳҜВ В В В В В В В В В В В В В В В В В пјӣ в‘Ўжә¶ж¶Ідёӯзҡ„йҳҙзҰ»еӯҗеҗ‘________з”өжһҒ移еҠЁпјҢпјҲеЎ«вҖңAlвҖқжҲ–вҖңAg2O/AgвҖқпјҢдёӢеҗҢпјүеҗ‘еӨ–з”өи·ҜйҮҠж”ҫз”өеӯҗзҡ„з”өжһҒжҳҜ_________________ гҖӮ
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
еёёжё©дёӢеңЁ20 mL 0.1 molВ·LпјҚ1Na2CO3жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…Ҙ0.1 molВ·LпјҚ1HClжә¶ж¶І40 mLпјҢжә¶ж¶Ідёӯеҗ«зўіе…ғзҙ зҡ„еҗ„з§Қеҫ®зІ’(CO2еӣ йҖёеҮәжңӘз”»еҮә)зү©иҙЁзҡ„йҮҸеҲҶж•°(зәөиҪҙ)йҡҸжә¶ж¶ІpHеҸҳеҢ–зҡ„йғЁеҲҶжғ…еҶөеҰӮеӣҫжүҖзӨәгҖӮ еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ в‘ еңЁеҗҢдёҖжә¶ж¶ІдёӯпјҢH2CO3гҖҒHCO3гҖҒCO в‘ЎеҪ“pHпјқ7ж—¶пјҢжә¶ж¶Ідёӯеҗ«зўіе…ғзҙ зҡ„дё»иҰҒеҫ®зІ’дёә____________________пјҢжә¶ж¶Ідёӯеҗ„з§ҚзҰ»еӯҗзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰзҡ„еӨ§е°Ҹе…ізі»дёә__________________________________пјӣ в‘ўе·ІзҹҘеңЁ25 в„ғж—¶пјҢCO
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
|
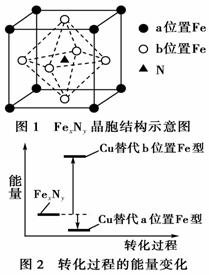
й“Ғж°®еҢ–еҗҲзү©(FexNy)еңЁзЈҒи®°еҪ•жқҗж–ҷйўҶеҹҹжңүзқҖе№ҝжіӣзҡ„еә”з”ЁеүҚжҷҜгҖӮжҹҗFexNyзҡ„еҲ¶еӨҮйңҖй“ҒгҖҒж°®ж°”гҖҒдёҷй…®е’Ңд№ҷйҶҮеҸӮдёҺгҖӮ (1)Fe3пјӢеҹәжҖҒж ёеӨ–з”өеӯҗжҺ’еёғејҸдёә__________гҖӮ (2)дёҷй…®( (3)CгҖҒHгҖҒOдёүз§Қе…ғзҙ зҡ„з”өиҙҹжҖ§з”ұе°ҸеҲ°еӨ§зҡ„йЎәеәҸдёә________гҖӮ (4)д№ҷйҶҮзҡ„жІёзӮ№й«ҳдәҺдёҷй…®пјҢиҝҷжҳҜеӣ дёә________гҖӮ (5)жҹҗFexNyзҡ„жҷ¶иғһеҰӮеӣҫ1жүҖзӨәпјҢCuеҸҜд»Ҙе®Ңе…Ёжӣҝд»ЈиҜҘжҷ¶дҪ“дёӯaдҪҚзҪ®FeжҲ–иҖ…bдҪҚзҪ®FeпјҢеҪўжҲҗCuжӣҝд»ЈеһӢдә§зү©Fe(xпјҚn)CunNyгҖӮFexNyиҪ¬еҢ–дёәдёӨз§ҚCuжӣҝд»ЈеһӢдә§зү©зҡ„иғҪйҮҸеҸҳеҢ–еҰӮеӣҫ2жүҖзӨәпјҢе…¶дёӯжӣҙзЁіе®ҡзҡ„Cuжӣҝд»ЈеһӢдә§зү©зҡ„еҢ–еӯҰејҸдёә________гҖӮ
|
|
| 25. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
|
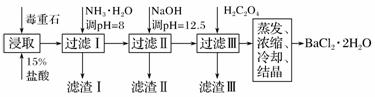
жҜ’йҮҚзҹізҡ„дё»иҰҒжҲҗеҲҶBaCO3(еҗ«Ca2пјӢгҖҒMg2пјӢгҖҒFe3пјӢзӯүжқӮиҙЁ)пјҢе®һйӘҢе®ӨеҲ©з”ЁжҜ’йҮҚзҹіеҲ¶еӨҮBaCl2В·2H2Oзҡ„жөҒзЁӢеҰӮдёӢпјҡ
(1)
еҠ е…ҘNH3В·H2Oи°ғиҠӮpHпјқ8еҸҜйҷӨеҺ»________(еЎ«зҰ»еӯҗз¬ҰеҸ·)пјҢж»ӨжёЈв…Ўдёӯеҗ«________(еЎ«еҢ–еӯҰејҸ)гҖӮеҠ е…ҘH2C2O4ж—¶еә”йҒҝе…ҚиҝҮйҮҸпјҢеҺҹеӣ жҳҜ_________________________гҖӮ е·ІзҹҘпјҡKsp(BaC2O4)пјқ1.6Г—10пјҚ7пјҢKsp(CaC2O4)пјқ2.3Г—10пјҚ9гҖӮ (2)еҲ©з”Ёй—ҙжҺҘй…ёзўұж»ҙе®ҡжі•еҸҜжөӢе®ҡBa2пјӢзҡ„еҗ«йҮҸпјҢе®һйӘҢеҲҶдёӨжӯҘиҝӣиЎҢгҖӮ е·ІзҹҘпјҡ2CrO жӯҘйӘӨв… з§»еҸ–x mLдёҖе®ҡжө“еәҰзҡ„Na2CrO4жә¶ж¶ІдәҺй”ҘеҪўз“¶дёӯпјҢеҠ е…Ҙй…ёзўұжҢҮзӨәеүӮпјҢз”Ёb molВ·LпјҚ1зӣҗй…ёж ҮеҮҶж¶Іж»ҙе®ҡиҮіз»ҲзӮ№пјҢжөӢеҫ—ж»ҙеҠ зӣҗй…ёдҪ“з§ҜдёәV0 mLгҖӮ жӯҘйӘӨв…Ўпјҡ移еҸ–y mL BaCl2жә¶ж¶ІдәҺй”ҘеҪўз“¶дёӯпјҢеҠ е…Ҙx mLдёҺжӯҘйӘӨв… зӣёеҗҢжө“еәҰзҡ„Na2CrO4жә¶ж¶ІпјҢеҫ…Ba2пјӢе®Ңе…ЁжІүж·ҖеҗҺпјҢеҶҚеҠ е…Ҙй…ёзўұжҢҮзӨәеүӮпјҢз”Ёb molВ·LпјҚ1зӣҗй…ёж ҮеҮҶж¶Іж»ҙе®ҡиҮіз»ҲзӮ№пјҢжөӢеҫ—ж»ҙеҠ зӣҗй…ёзҡ„дҪ“з§ҜдёәV1 mLгҖӮ ж»ҙеҠ зӣҗй…ёж ҮеҮҶж¶Іж—¶еә”з”Ёй…ёејҸж»ҙе®ҡз®ЎпјҢвҖң0вҖқеҲ»еәҰдҪҚдәҺж»ҙе®ҡз®Ўзҡ„________(еЎ«вҖңдёҠж–№вҖқжҲ–вҖңдёӢж–№вҖқ)гҖӮBaCl2жә¶ж¶Ізҡ„жө“еәҰдёә________ molВ·LпјҚ1пјҢиӢҘжӯҘйӘӨв…Ўдёӯж»ҙеҠ зӣҗй…ёж—¶жңүе°‘йҮҸеҫ…жөӢж¶Іжә…еҮәпјҢBa2пјӢжө“еәҰжөӢйҮҸеҖје°Ҷ________(еЎ«вҖңеҒҸеӨ§вҖқжҲ–вҖңеҒҸе°ҸвҖқ)гҖӮ
|
|||||||||||||
| 26. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҗ«иӢҜзҺҜзҡ„еҢ–еҗҲзү©AпјҢе…¶зӣёеҜ№еҲҶеӯҗиҙЁйҮҸдёә104пјҢзўізҡ„иҙЁйҮҸеҲҶж•°дёә92.3%гҖӮ (1)Aзҡ„еҲҶеӯҗејҸдёә________________гҖӮ (2)AдёҺжәҙзҡ„еӣӣж°ҜеҢ–зўіжә¶ж¶ІеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә________________________________________пјҢ еҸҚеә”зұ»еһӢжҳҜ________________гҖӮ (3)е·ІзҹҘпјҡ (4)дёҖе®ҡжқЎд»¶дёӢпјҢAдёҺж°ўж°”еҸҚеә”пјҢеҫ—еҲ°зҡ„еҢ–еҗҲзү©дёӯзўізҡ„иҙЁйҮҸеҲҶж•°дёә85.7%пјҢеҶҷеҮәжӯӨеҢ–еҗҲзү©зҡ„з»“жһ„з®ҖејҸпјҡ______________________________гҖӮ (5)еңЁдёҖе®ҡжқЎд»¶дёӢпјҢз”ұAиҒҡеҗҲеҫ—еҲ°зҡ„й«ҳеҲҶеӯҗеҢ–еҗҲзү©зҡ„з»“жһ„з®ҖејҸдёә__________гҖӮ
|
|
- еұұиҘҝзңҒиҝҗеҹҺеёӮжҷҜиғңдёӯеӯҰ2020-2021е№ҙй«ҳдёҖдёҠеҶҢе…ҘеӯҰж‘ёеә•иҖғиҜ•еҢ–еӯҰж— зәёиҜ•еҚ·е®Ңж•ҙзүҲ
- 2019еұҠй«ҳдёүдёҠеҚҠжңҹжңҹжң«иҖғиҜ•AеҚ·зҗҶ科综еҗҲеҢ–еӯҰиҖғиҜ•е®Ңж•ҙзүҲпјҲжІіеҢ—зңҒе”җеұұеёӮпјү
- ж№–еҢ—зңҒйҫҷжіүдёӯеӯҰгҖҒиҚҶе·һдёӯеӯҰгҖҒе®ңжҳҢдёҖдёӯ2021еұҠй«ҳдёү9жңҲиҒ”иҖғеҢ–еӯҰеңЁзәҝиҖғиҜ•йўҳе…Қиҙ№з»ғд№
- зҰҸе»әзңҒдёүжҳҺ第дёҖдёӯеӯҰ2020еұҠй«ҳдёүдёҠеҚҠе№ҙ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·
- дә‘еҚ—й«ҳдёҖеҢ–еӯҰ2019е№ҙдёҠеҶҢжңҹжң«иҖғиҜ•еёҰеҸӮиҖғзӯ”жЎҲдёҺи§Јжһҗ
- е®үеҫҪзңҒж·®еҢ—еёӮ第дёҖдёӯеӯҰ2020еұҠй«ҳдёүеүҚеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғйўҳ
- йІҒ科зүҲйҖүжӢ©жҖ§еҝ…дҝ®1 第3з« зү©иҙЁеңЁж°ҙжә¶ж¶Ідёӯзҡ„иЎҢдёә еҫ®йЎ№зӣ® жҸӯз§ҳзҙўе°”з»ҙеҲ¶зўұжі•е’ҢдҫҜж°ҸеҲ¶зўұжі•--еҢ–еӯҰе№іиЎЎжҖқжғізҡ„еҲӣйҖ жҖ§еә”
- 2018-2019е№ҙй«ҳдәҢдёҠеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰиҖғиҜ•е®Ңж•ҙзүҲпјҲе№ҝиҘҝеЈ®ж—ҸиҮӘжІ»еҢәжҹіжұҹдёӯеӯҰпјү

 )
) )
)