2018安徽高一上学期人教版高中化学期中考试
| 1. | 详细信息 |
|
下列做法不能体现低碳生活的是( ) A. 注意节约用水 B. 减少食品加工过程 C. 发展氢能和太阳能 D. 大量使用化石燃料
|
|
| 2. | 详细信息 |
|
不能用胶体的知识解释的现象是( ) A. 向FeCl3溶液中加入NaOH溶液,出现红褐色沉淀 B. 石膏点豆腐 C. 一支钢笔使用两种不同牌号的墨水,易出现堵塞 D. 江河入海处,易形成沙洲
|
|
| 3. | 详细信息 |
|
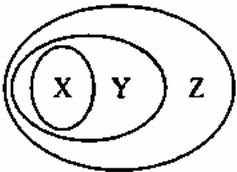
下图所表示的一些物质或概念间的从属关系不正确的是( )
A. A B. B C. C D. D
|
|
| 4. | 详细信息 |
|
下列判断正确的是 ( ) A. 酸性氧化物一定是非金属氧化物 B. 碱性氧化物一定是金属氧化物 C. SO2 溶于水能导电所以SO2 是电解质 D. Na2O是非电解质
|
|
| 5. | 详细信息 |
|
将一小块金属钠长期露置于空气中发生一系列变化,最终产物是( ) A. NaOH B. Na2CO3 C. Na2CO3·10H2O D. Na2O2
|
|
| 6. | 详细信息 |
|
下列说法正确的是( ) A. Cl2具有很强的氧化性,在化学反应中只能作氧化剂 B. 漂白粉的有效成分为CaCl2和Ca(ClO)2 C. 实验室制备Cl2,可用向上排空气法收集 D. 新制氯水只含有氯气和次氯酸分子
|
|
| 7. | 详细信息 |
|
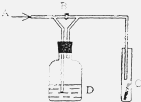
如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
A. 浓H2SO4 B. 饱和NaCl溶液 C. 浓NaOH溶液 D. 饱和纯碱 溶液
|
|
| 8. | 详细信息 |
|
分类是化学研究中常用的方法。下列分类方法中,不正确的是( ) A. 依据分子中含有的氢原子的数目,将酸分为一元酸、二元酸等 B. 依据在水溶液中或熔融状态下能否导电,将化合物分为电解质和非电解质 C. 依据分散质粒子的大小,将分散系分为溶液、胶体、浊液 D. 依据组成的元素的种类,将纯净物分为单质和化合物
|
|
| 9. | 详细信息 |
|
下列说法中正确的是 ( ) A. 1 L 水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L B. 从1 L 2 mol/L的H2SO4 溶液中取出0.5 L,取出溶液的浓度为1 mol/L C. 配制500 mL 0.2 mol/L的CuSO4溶液,需25.0 g CuSO4·5H2O D. 中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4.0 g
|
|
| 10. | 详细信息 |
|
向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)近似的用下图中的曲线表示是( )
|
|
| 11. | 详细信息 |
|
某无色透明的溶液中,能大量共存的离子组是( ) A. Na+、H+、SO42-、HCO3- B. Cu2+、K+、SO42-、NO3- C. Na+、K+、Cl-、NO3- D. Ba2+、K+、SO42-、Cl-
|
|
| 12. | 详细信息 |
|
下列离子方程式正确的是( ) A. 稀盐酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ B. 硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaS04↓ C. 足量盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O D. 物质的量相等的MgCl2、Ba(OH)、 HC1三种溶液混合:Mg2++2OH-═Mg(OH)2↓
|
|
| 13. | 详细信息 |
|
用NA表示阿伏加德罗常数的值,下列叙述中不正确的是( ) A. 标况下,22.4 L氧气的分子数为NA B. 100 g质量分数为98%的浓硫酸中所含氧原子数为4NA C. 常温常压下,92 g NO2和N2O4的混合气体含有的原子数为6NA D. 18 g NH4+含有的电子数为10NA
|
|
| 14. | 详细信息 |
|
标准状况下有①6.72 L CH4 ②3.01×1023个HCl ③13.6 g H2S ④0.2 mol NH3,下列对四种气体的关系从小到大表示不正确的是( ) A. 体积④<①<③<② B. 密度①<④<③<② C. 质量④<①<③<② D. 氢原子数④<②<③<①
|
|
| 15. | 详细信息 |
|
下列反应中,水既不做氧化剂,又不做还原剂的是( ) A. Cl2+H2O=HCl+HClO B. 2H2O C. 2Na+2H2O=2NaOH+H2↑ D. 2F2+2H2O=4HF+O2↑
|
|
| 16. | 详细信息 |
|
下列叙述正确的是( ) A. 金属阳离子被还原后,一定得到该元素的单质 B. 元素由化合态变成游离态时,它可能被氧化,也可能被还原 C. 失电子难的原子,获得电子的能力一定强 D. 有单质参加或生成的反应一定属于氧化还原反应
|
|
| 17. | 详细信息 |
|
宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”的原理是 4Ag +2H2S+O2═2X+2H2O,下列说法正确的是( ) A. X的化学式为AgS B. 银针验毒时,空气中氧气失去电子 C. 反应中Ag和H2S均是还原剂 D. 每生成1mol X,反应转移2mol e-
|
|
| 18. | 详细信息 |
|
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是( ) ①Cl2+2KI═I2+2KCl ②2FeCl3+2HI═I2+2FeCl2+2HCl ③2FeCl2+Cl2═2FeCl3 ④I2+SO2+2H2O═2HI+H2SO4 A. Cl2>I2>Fe3+>SO2 B. Fe3+>Cl2>I2>SO2 C. Cl2>Fe3+>I2>SO2 D. Cl2>Fe3+>SO2>I2
|
|
| 19. | 详细信息 |
|
把200 mL 含有BaCl2和KCl的混合溶液分成2等份,取一份加入含a mol Na2SO4溶液,恰好使钡离子完全沉淀,另取一份加入含b mol AgNO3溶液, 恰好使氯离子完全沉淀,则该混合溶液中钾离子浓度为( ) A. 0.1(b-2a) mol ·L-1 B. 10(2a-b) mol ·L-1 C. 10(b-a) mol ·L-1 D. 10(b-2a) mol ·L-1
|
|
| 20. | 详细信息 |
|
R2O8n- 离子在一定条件下可以把Mn2+ 离子氧化为MnO4-,若R2O8n- 离子变为RO42- 离子,又知反应中氧化剂与还原剂的物质的量之比为5:2,则n的值为( ) A. 4 B. 3 C. 2 D. 1
|
|
| 21. | 详细信息 |
|
(1)写出硫酸氢钾在水溶液中的电离方程式: __________________________________ (2)①写出钠与水反应的离子方程式:___________________________________________ ②写出氢氧化钠与氯气反应的离子方程式: ____________________________________
|
|
| 22. | 详细信息 |
|
下列物质中 : ①盐酸 ②NH3 ③Cu ④乙醇 ⑤NaOH 固体 ⑥石墨 ⑦熔融NaCl (1)属于电解质的是________;(填序号,下同)(2)属于非电解质的是________; (3)能导电的是______。
|
|
| 23. | 详细信息 |
|
已知反应: MnO2 +4HCl(浓) (1)用单线桥法标明该反应中电子转移的方向和数目:______ MnO2 +4HCl(浓) (2)计算反应消耗的MnO2的质量______ ; (3)计算被氧化的HCl物质的量______ 。
|
|
| 24. | 详细信息 |
|
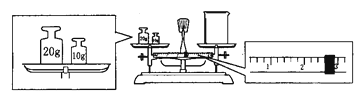
实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL: (1)配制溶液时,一般可以分为以下几个步骤: ①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却 其正确的操作顺序为____________________。 (2)本实验用到的玻璃仪器有________________(至少回答3个)。 (3) 某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为________g,要完成本实验该同学应称出______g NaOH。
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是_____(填序号) ①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线 ⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
|
|
| 25. | 详细信息 |
|
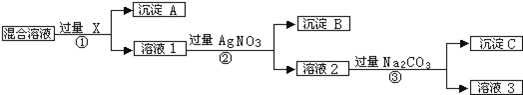
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离.相应的实验过程可用下图表示: 请回答下列问题: 写出实验流程中下列物质的化学式试剂X: ______ 沉淀A: ______ 沉淀B: ______ 上述实验流程中加入过量的Na2CO3的目的是 ______ (3)按此实验方案得到的溶液3中肯定含有 ______ 杂质(填化学式)
|
|