2020江西高一上学期人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
2015年8月12日,位于天津滨海新区塘沽开发区的天津东疆保税港区瑞海国际物流有限公司所属危险品仓库发生爆炸,化学危险品的合理存放引起高度重视。下列标志中,应贴在盛放高锰酸钾容器上的是 ( )
A B C D
|
|
| 2. | 详细信息 |
|
下列叙述正确的是( ) A. BaSO4溶于水的部分能够电离,所以BaSO4是电解质 B. SO2的水溶液能够导电,所以SO2是电解质 C. 液态Cl2不导电,所以Cl2是非电解质 D. 盐酸能导电,所以盐酸是电解质
|
|
| 3. | 详细信息 | ||||||||||||||||||||
|
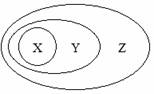
下图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
|
|||||||||||||||||||||
| 4. | 详细信息 |
|
NA表示阿伏加德罗常数,下列说法正确的是( ) A.质量为16g的O2和O3的混合气体中所含的氧原子的个数为NA B.18 g NH4+含有质子数为10NA C.1 mol过氧化钠与足量水反应时,转移电子的数目为2NA D.0.1 mol•L﹣1的NaCl溶液中,Na+与Cl﹣的离子总数为0.2NA
|
|
| 5. | 详细信息 |
|
下列有关气体摩尔体积的描述中正确的是( ) A.相同物质的量的气体摩尔体积一定相同 B.通常状况下的气体摩尔体积约为22.4L C.标准状况下的气体摩尔体积约为22.4L D.单位物质的量的气体所占的体积就是气体摩尔体积
|
|
| 6. | 详细信息 |
|
下列关于胶体,判断不正确的是( ) A.胶体的本质特征是胶粒直径在1nm~100nm B.丁达尔现象可以用来区别胶体和溶液 C.煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体 D.溶液和胶体的分散质都能通过滤纸孔隙
|
|
| 7. | 详细信息 |
|
下列溶液与20mL 1mol•L﹣1 NaNO3溶液中NO3﹣物质的量浓度相等的是( ) A.10mL 1mol•L﹣1 Mg(NO3)2溶液 B.5mL 0.8mol•L﹣1 Al(NO3)3溶液 C.10mL 2mol•L﹣1AgNO3溶液 D.10mL 0.5mol•L﹣1 Cu(NO3)2溶液
|
|
| 8. | 详细信息 |
|
在某澄清透明的酸性溶液中,能大量共存的离子组是( ) A.Na+ 、Al3+、SO42-、HCO3 B.Na+、 Ba2+、Cl、SO42- C.Cu2+、Mg2+、SO42-、NO3 D.Fe3+、K+、NO3、I
|
|
| 9. | 详细信息 |
|
实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O,此反应中氧化剂与还原剂的物质的量之比为( ) A.1︰8 B.1︰5 C.2︰5 D.5︰1
|
|
| 10. | 详细信息 |
|
下列离子方程式书写正确的是( ) A.铝片加入氯化铜溶液中:Al+Cu2+===Al3++Cu B.氢氧化钾溶液加入氯化铁溶液中:3OH-+FeCl3===Fe(OH)3↓+3Cl- C.石灰石加入稀盐酸中:CaCO3+2H+===Ca2++CO2↑+2H2O D.氢氧化钡溶液加入稀硫酸中:Ba2++OH-+H++SO42-===BaSO4↓+H2O
|
|
| 11. | 详细信息 |
|
对于反应8NH3+3Cl2==N2+6NH4Cl,下列说法正确的是( ) A. N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 B. N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 C. 每转移6mol电子就生成22.4L N2 D. NH4Cl是氧化产物,且还原产物与氧化产物物质的量之比是1:6
|
|
| 12. | 详细信息 |
|
在标准状况下有①6.72L CH4,②3.01×1023个HCl分子,③13.6 g硫化氢,④0.2 m0l氨气。下列对这四种气体的关系描述不正确的是( ) A.体积:②>③>①>④ B.密度:②>③>④>① C.质量:②>③>①>④ D.氢原子数:①>④>③>②
|
|
| 13. | 详细信息 |
|
据报道,受不利气象条件影响,北京于12月11日再次陷入雾霾之中。官方当日先后发布霾黄色、空气重污染蓝色预警,当日的空气质量一直维持在重度污染水平。下列为了防止产生雾霾的措施不可行的是( ) A. 停止冬季供暖,减少有害物质排放 B. 退耕还林,改善生态环境 C. 对锅炉和汽车等产生的有害气体和烟尘等进行处理 D. 寻找新能源,减少化石燃料的使用
|
|
| 14. | 详细信息 |
|
下列有关物质的分类或归类正确的一组是( ) ①液氨、液氯、干冰、纯碱均为化合物 ②漂白粉、铝热剂、水玻璃、氨水均为混合物 ③明矾、小苏打、醋酸、烧碱均为电解质 ④碘酒、牛奶、豆浆、肥皂水均为胶体 ⑤Na2O2、Na2CO3、NaHCO3、NaClO均为钠盐 A. ①和② B. ②和③ C. ②③④ D. ②③⑤
|
|
| 15. | 详细信息 |
|
用 N A表示阿伏加德罗常数的值。下列叙述正确的是( ) A.阿伏加德罗常数是指1mol物质中所含有的原子数 B.常温、常压下,10 g H2中约含6.02×1024个电子 C.50 ml 0.1 mol/L的Na2CO3溶液中Na+的物质的量为0.1 mol D.标准状况下,2.24 L CCl4含有的原子数为 0.5 NA
|
|
| 16. | 详细信息 |
|
实验室通常悬挂涂有CuI的滤纸监测空气中汞蒸气的含量,监测原理为:4CuI + Hg = Cu2HgI4 +2Cu,下列叙述正确的是( ) A.在Cu2HgI4中I的化合价为-2价 B.4mol CuI反应中失去4mol电子 C.该反应中Hg 是还原剂 D.CuI既是氧化剂又是还原剂
|
|
| 17. | 详细信息 |
|
用98%的浓硫酸(其密度为1.84g/cm3)配制100mL 1.0mol•L﹣1稀硫酸, (1)需量取浓硫酸的体积为 mL. (2)配制溶液时,一般可以分为以下几个步骤:①量取 ②计算 ③溶解 ④颠倒摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序为 ,本实验必须用到的仪器有量筒、玻璃棒、烧杯、胶头滴管、还有 . (3)在配制过程中,下列操作会引起浓度偏高的是 ,无影响的是 (填序号). ①没有洗涤烧杯和玻璃棒; ②转移溶液时不慎有少量洒到容量瓶外面; ③容量瓶不干燥,含有少量蒸馏水; ④定容时俯视刻度线; ⑤未冷却到室温就将溶液转移到容量瓶并定容; ⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
|
|
| 18. | 详细信息 |
|
某反应体系中反应物和生成物共有7种物质:I2、K2SO4、KI、H2O、H2SO4、CuI(难溶)、Cu(IO3)2.当将反应物混合时,可观察到反应体系中绿色晶体逐步转变为棕黄色沉淀.反应前如果向反应体系中滴加淀粉溶液无明显变化,反应后则得到蓝色溶液.请回答下列问题:
|
|
| 19. | 详细信息 |
|
物质的量是高中化学常用的物理量,请完成以下有关计算: (1)0.6 g H2中含有氢原子的物质的量为 mol. (2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为 . (3)100 mL硫酸钠溶液中n (Na+)=0.2 mol,则其中c (SO42-)= . (4)6.72L(标准状况)CO与一定量的Fe2O3恰好完全反应,生成Fe的质量为 g.
|
|
| 20. | 详细信息 | ||||||||||||
|
用一种试剂除去下列物质中的杂质(括号内物质为杂质),写出试剂名称和有关反应的离子方程式。
|
|||||||||||||
| 21. | 详细信息 |
|
有一包白色粉末,可能含有NaHSO4、KHCO3、Ba(NO3)2、 CaCl2、NaNO3、MgSO4中的一种或几种。 实验步骤如下: ①取少量固体投入水中,既有气体生成,又有沉淀产生。 ②过滤,取少量滤液加AgNO3溶液,无沉淀产生。 ③再取少量滤液,加入足量NaOH溶液,也无沉淀产生。 ⑴ 推断白色粉末中一定有 ,一定没有 。 ⑵ 请写出实验步骤①中产生气体的离子方程式: 。 ⑶ 请写出用实验检验CaCl2中阴离子方程式: 。
|
|