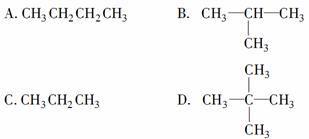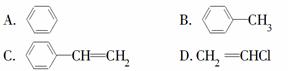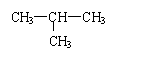2017吉林高一下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列措施一定能使化学反应速率增大的是 A.增大反应物的量 B.增大压强 C.升高温度 D.使用催化剂
|
|
| 2. | 详细信息 |
|
某温度下,反应2N2O5(g)===4NO2(g)+O2(g)开始时,c(N2O5)=0.040 8 mol/L,经1 min后,c(N2O5)=0.030 0 mol/L。则该反应的反应速率为 A.v(N2O5)=5.4×10-3 mol/(L·min) B.v(N2O5)=1.08×10-2 mol/(L·min) C.v(NO2)=1.08 D.v(O2)=1.08×10-2 mol/(L·min)
|
|
| 3. | 详细信息 |
|
已知CaCO3和盐酸反应的化学方程式为CaCO3(s)+2HCl===CaCl2+H2O+CO2↑,下列措施中 A.加大CaCO3的量 B.加大盐酸的浓度 C.加大盐酸的量 D.减小CaCl2的浓度
|
|
| 4. | 详细信息 |
|
用铁片和稀硫酸反应制取H2时,下列措施不能使氢气的生成速率增大的是 A.加热 B.不用稀硫酸,而改用98%的浓硫酸 C.滴加少量浓盐酸 D.不用铁片,改用铁粉
|
|
| 5. | 详细信息 |
|
某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z。反应2min 后,测得参加反应的X2为0.6mol/L,用Y2的变化表示的反应速率v(Y2) =0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应的化学方程式是 A. X2+2Y2 C. 3X2+Y2
|
|
| 6. | 详细信息 |
|
可逆反应2NO2(g) ①单位时间内生成nmol O2的同时生成2nmol NO2 ②单位时间内生成nmol O2的同时生成2nmol NO ③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的压强不再改变的状态 ⑦混合气体的平均相对分子质量不再改变的状态 C.①③④⑤ D.全部
|
|
| 7. | 详细信息 |
|
鉴别甲烷、一氧化碳和氢气3种无色气体的方法,是将 A.先后通入溴水和澄清石灰水 B.点燃后罩上涂有澄清石灰水的烧杯 C.点燃,先后罩上干燥的冷烧杯和涂有澄清石灰水的烧杯 D.点燃后罩上涂有澄清石灰水的烧杯,通入溴水
|
|
| 8. | 详细信息 |
|
若甲烷与氯气以物质的量之比1∶3混合,在光照下得到的有机产物:①CH3Cl,②CH2Cl2, ③CHCl3,④CCl4,其中正确的是
C.①②③的混合物 D.①②③④的混合物
|
|
| 9. | 详细信息 |
|
甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面 A.CHCl3只有一种结构 B.CH2Cl2只有一种结构 C.CH4分子受热分解 D.CH4的四个价键的长度和强度都相等
|
|
| 10. | 详细信息 |
|
下列属于烷烃的是 A.C2H4 B.C3H4 C.C12H26 D.C
|
|
| 11. | 详细信息 |
|
下列烷烃在光照下与氯气反应,只生成一种一氯代物的是
|
|
| 12. | 详细信息 |
|
下列反应属于取代反应的是 A.CH4 B.2HI+Cl2====2HCl+I2 C.CH4+2O2 D.CH4+Cl2
|
|
| 13. | 详细信息 |
|
下列5种烃:①CH3CH2CH(CH3)2 ②CH3C(CH3)3 ③丙 A.①②③④⑤ B.②③④⑤① C.⑤②①③④ D.④①②⑤③
|
|
| 14. | 详细信息 |
|
下列说法中错误的是 A.乙烯与Br2的加成,乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关 B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷 C.相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同 D.利用燃烧的方法可以鉴别乙烯和甲烷
|
|
| 15. | 详细信息 |
|
关于乙烯分子结构的说法中,错误的是 A.乙烯分子里含有碳碳双键 B.乙烯分子里所有的原子共平面 C.乙烯分子中碳碳双键和乙烷分子中碳碳单键相同 D.乙烯分子里共价键之间的夹角为120°
|
|
| 16. | 详细信息 |
|
下列说法正确的是 A.乙烯的分子式可写成(CH2)2 B.乙烯的最简式为CH—CH C.乙烯分子是空间平面结构 D.乙烯的结构简式为CH2CH2
|
|
| 17. | 详细信息 |
|
下列有机物分子中,所有的原子不可能在同一平面上的是
|
|
| 18. | 详细信息 |
|
在下列事实中,各是什么因素影响了化学反应速率。 (1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:________。 (2)黄铁矿煅烧时要粉碎成矿粒:________。 (3)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体 :________。 (4)同样大小的石灰石分别与0.1 mol·L-1盐酸和1 mol·L-1盐酸反应,速率不同: ____ ____。 (5)夏天食品容易变质,而冬天不易发生该现象:_______________。
|
|
| 19. | 详细信息 |
|
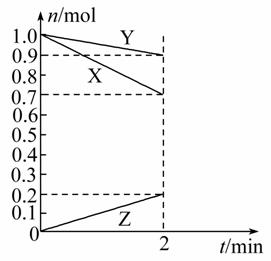
某温度时,在2 L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图 所示。由图中数据分析:该反应的化学方程式为_______________。反应开始至2 min,用Z表示的平均反应速率为________________。
|
|
| 20. | 详细信息 |
|
写出下列各烷烃的分子式。 (1)烷烃A在同温同压下蒸气的密度是H2的43倍, 。 (2)烷烃B的分子中含有200个氢原子, 。 (3)分子中含有26个电子的烷烃C, 。 (4)室温下相对分子质量最大的气态直链烷烃D, 。 (5)0.1 mol烷烃E完全燃烧,消耗标准状况下的O211.2 L,
|
|
| 21. | 详细信息 |
|
有下列各组物质:
C.CH3—CH2—CH2—CH3和
D. 和 E.甲烷和庚烷 ⑴ ______组两物质互为同位素; ⑵ ___组两物质互为同素异形体; ⑶ ____组两物质属于同系物; ⑷ __组两物质互为同分异构体; ⑸ ____组中两物质是同一物质。
|
|
| 22. | 详细信息 |
|
苯是一种重要的化工原料,也是一种重要的溶剂。请回答下列问题: (1)把苯加入到盛有溴水的试管中,液体会出现分层现象,充分振荡、静置,出现橙红色液体的一层在________(填“上”或“下”)层。 (2)把苯加入到盛有少量酸性高锰酸钾溶液的试管中,振荡后,酸性高锰酸钾溶液不褪色,说明苯分子中________(填“有”或“没有”)碳碳双键。 (3)在浓硫酸作用下,苯在水浴加热时可以与浓硝酸反应生成硝基苯,该反应的化学方程式为________________________。 (4)苯在一定条件下生成溴苯的化学方程式为_______________。 (5)苯在一定条件下生成环己烷的方程式为__________________。 (6)乙烯与水的化学方程式__________________。
|
|
| 23. | 详细信息 |
|
下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。
(1)B中溶液褪色,是因为乙烯被________。 (2)C中发生反应的化学方程式为________________________,反应类型为 __________ (3)
|
|