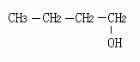2019иҫҪе®Ғй«ҳдёҖдёӢеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
еҲ©з”Ёз”Ізғ·дёҺж°Ҝж°”еҸ‘з”ҹеҸ–д»ЈеҸҚеә”еҲ¶еҸ–еүҜдә§е“Ғзӣҗй…ёзҡ„и®ҫжғіеңЁе·ҘдёҡдёҠе·ІжҲҗдёәзҺ°е®һгҖӮжҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„еңЁе®һйӘҢе®ӨдёӯжЁЎжӢҹдёҠиҝ°иҝҮзЁӢпјҢе…¶и®ҫи®Ўзҡ„жЁЎжӢҹиЈ…зҪ®еҰӮдёӢпјҡ ж №жҚ®и®ҫи®ЎиҰҒжұӮеӣһзӯ”пјҡ пјҲ1пјүAдёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёәпјҡ______________________________ пјҲ2пјүBиЈ…зҪ®жңүдёүз§ҚеҠҹиғҪпјҡв‘ еқҮеҢҖж··еҗҲж°”пјӣв‘Ўе№ІзҮҘж··еҗҲж°”дҪ“пјӣв‘ў______________гҖӮ пјҲ3пјүи®ҫV(Cl2)/V(CH4)пјқxпјҢиӢҘзҗҶи®әдёҠж¬ІиҺ·еҫ—жңҖеӨҡзҡ„ж°ҜеҢ–ж°ўпјҢеҲҷxеҖјеә”вү§________гҖӮ пјҲ4пјүEиЈ…зҪ®зҡ„дҪңз”ЁжҳҜ________________________________гҖӮ пјҲ5пјүеңЁCиЈ…зҪ®дёӯпјҢз»ҸиҝҮдёҖж®өж—¶й—ҙзҡ„ејәе…үз…§е°„пјҢеҸ‘зҺ°зЎ¬иҙЁзҺ»з’ғз®ЎеҶ…еЈҒжңүй»‘иүІе°Ҹйў—зІ’дә§з”ҹпјҢеҶҷеҮәз”ҹжҲҗй»‘иүІе°Ҹйў—зІ’зҡ„еҢ–еӯҰж–№зЁӢејҸ___________________________________гҖӮ пјҲ6пјүDиЈ…зҪ®дёӯзҡ„зҹіжЈүдёҠж”ҫиҫғеӨҡзҡ„KIзІүжң«пјҢе…¶дҪңз”Ёдёә________________________________гҖӮ пјҲ7пјүEиЈ…зҪ®йҷӨз”ҹжҲҗзӣҗй…ёеӨ–пјҢиҝҳеҗ«жңүжңүжңәзү©пјҢд»ҺEдёӯеҲҶзҰ»еҮәжңүжңәзү©зҡ„жңҖдҪіж–№жі•дёә________гҖӮ
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
зҹӯе‘Ёжңҹе…ғзҙ AгҖҒBгҖҒCгҖҒDгҖҒEгҖҒFе…ӯз§Қдё»ж—Ҹе…ғзҙ пјҢAгҖҒBеҗҢе‘ЁжңҹзӣёйӮ»пјҢAгҖҒCеҗҢдё»ж—ҸзӣёйӮ»пјҢAгҖҒBгҖҒCдёүз§Қе…ғзҙ зҡ„еҺҹеӯҗеәҸж•°д№Ӣе’Ңдёә31пјҢDе…ғзҙ дёҺAгҖҒBгҖҒCдёүз§Қе…ғзҙ ж—ўдёҚеҗҢе‘Ёжңҹд№ҹдёҚеҗҢдё»ж—ҸпјҢдҪҶDеҚ•иҙЁдёҺAгҖҒBгҖҒCеҚ•иҙЁеқҮеҸҜд»ҘеҸҚеә”пјҢEжҳҜзҹӯе‘Ёжңҹдё»ж—ҸдёӯеҺҹеӯҗеҚҠеҫ„жңҖеӨ§зҡ„е…ғзҙ пјҢFжҳҜBеҗҢе‘ЁжңҹзӣёйӮ»е…ғзҙ гҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүеҶҷеҮәCзҡ„е…ғзҙ з¬ҰеҸ·пјҡ_______________В DеңЁе‘ЁжңҹиЎЁдёӯзҡ„дҪҚзҪ®____________________гҖӮ пјҲ2пјүBгҖҒDеҸҜзӣҙжҺҘеҢ–еҗҲз”ҹжҲҗеҢ–еҗҲзү©xпјҢ xеҲҶеӯҗдёҺAгҖҒDеҪўжҲҗзҡ„еҲҶеӯҗзҡ„зЁіе®ҡжҖ§жҜ”иҫғ________ __________гҖӮ(з”ЁеҢ–еӯҰејҸиЎЁзӨә) пјҲ3пјүAгҖҒBгҖҒDеҸҜз»„жҲҗзҰ»еӯҗеҢ–еҗҲзү©yзҡ„еҢ–еӯҰејҸдёә__________пјӣEдёҺCжҢү1вҲ¶1еҪўжҲҗзҡ„еҢ–еҗҲзү©зҡ„з”өеӯҗејҸдёә____________ гҖӮ пјҲ4пјүAгҖҒCеҪўжҲҗзҡ„дёҖз§Қж—ўжңүж°§еҢ–жҖ§еҸҲжңүиҝҳеҺҹжҖ§зҡ„еёёи§ҒеҢ–еҗҲзү©пјҢе®ғеҜ№зҺҜеўғзҡ„еҪұе“Қд№ӢдёҖжҳҜ______ ____________________гҖӮ пјҲ5пјүж ҮеҮҶзҠ¶еҶөдёӢ9g FдёҺAзҡ„еҚ•иҙЁе®Ңе…ЁзҮғзғ§дә§з”ҹзҡ„ж°”дҪ“йҖҡе…ҘеҲ°1L 1molВ·LвҲ’1зҡ„NaOH жә¶ж¶ІдёӯпјҢе®Ңе…ЁеҸҚеә”еҗҺжә¶ж¶ІдёӯеӯҳеңЁзҡ„дё»иҰҒзҰ»еӯҗжҳҜ_____________________ гҖӮ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||
|
(1)еңЁжҹҗдёҖе®№з§Ҝдёә2 Lзҡ„еҜҶй—ӯе®№еҷЁдёӯпјҢжҹҗдёҖеҸҚеә”дёӯAгҖҒBгҖҒCгҖҒDеӣӣз§Қж°”дҪ“зҡ„зү©иҙЁзҡ„йҮҸn(mol)йҡҸж—¶й—ҙt(min)зҡ„еҸҳеҢ–жӣІзәҝеҰӮеӣҫжүҖзӨәпјҡ
еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ в‘ иҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә__________________________________гҖӮ в‘ЎеүҚ2minз”ЁAзҡ„жө“еәҰеҸҳеҢ–иЎЁзӨәзҡ„еҢ–еӯҰеҸҚеә”йҖҹзҺҮдёә________гҖӮеңЁ2minж—¶пјҢеӣҫеғҸеҸ‘з”ҹж”№еҸҳзҡ„еҺҹеӣ жҳҜ________(еЎ«еӯ—жҜҚ)гҖӮ AпјҺеўһеӨ§еҺӢејәВ В В В В В В BпјҺйҷҚдҪҺжё©еәҰВ В В В В CпјҺеҠ е…ҘеӮ¬еҢ–еүӮВ В В В В В В DпјҺеўһеҠ Aзҡ„зү©иҙЁзҡ„йҮҸ пјҲ2пјүеңЁ100в„ғж—¶пјҢе°Ҷ0.01molзҡ„еӣӣж°§еҢ–дәҢж°®ж°”дҪ“е……е…Ҙ0.1Lзҡ„еҜҶй—ӯе®№еҷЁдёӯеҸ‘з”ҹеҸҚеә”пјҢйҡ”дёҖе®ҡж—¶й—ҙеҜ№иҜҘе®№еҷЁеҶ…зҡ„зү©иҙЁиҝӣиЎҢеҲҶжһҗпјҢеҫ—еҲ°еҰӮдёӢиЎЁж јпјҡ
иҜ•еЎ«з©әпјҡ в‘ иҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ________________________________пјҢиҫҫеҲ°е№іиЎЎж—¶еӣӣж°§еҢ–дәҢж°®зҡ„иҪ¬еҢ–зҺҮдёә_______гҖӮ в‘ЎеңЁ0пҪһ20sеҶ…пјҢеӣӣж°§еҢ–дәҢж°®зҡ„е№іеқҮеҸҚеә”йҖҹзҺҮдёә______пјҢе“ӘдёҖж—¶й—ҙж®ө______(жҢҮ0пҪһ20гҖҒ20пҪһ40гҖҒ40пҪһ60гҖҒ60пҪһ80гҖҒ80пҪһ100 s)еҸҚеә”йҖҹзҺҮжңҖеӨ§е№¶и§ЈйҮҠ______гҖӮ
|
||||||||||||||||||||||
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
в‘ з”Ізғ·гҖҒв‘Ўд№ҷзғ·гҖҒв‘ўд№ҷзғҜгҖҒв‘ЈиӢҜгҖҒв‘Өз”ІиӢҜгҖҒв‘ҘдәҢз”ІиӢҜгҖҒв‘Ұд№ҷйҶҮгҖҒ⑧д№ҷй…ёпјҢе®ғ们йғҪжҳҜеёёи§Ғзҡ„йҮҚиҰҒеҢ–е·ҘеҺҹж–ҷгҖӮ пјҲ1пјүдёҠиҝ°зү©иҙЁдёӯпјҢж°ўе…ғзҙ зҡ„иҙЁйҮҸеҲҶж•°жңҖеӨ§зҡ„жҳҜ______еЎ«еҲҶеӯҗејҸпјӣ пјҲ2пјүеҲҶеҲ«еҶҷеҮәв‘ҰгҖҒ⑧дёӯжүҖеҗ«е®ҳиғҪеӣўзҡ„еҗҚз§°____________гҖҒ____________дәҢиҖ…еҸ‘з”ҹй…ҜеҢ–еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә_________________________________________________пјҢеҰӮжһңз”Ё4.6gд№ҷйҶҮе’Ң9.0gд№ҷй…ёе……еҲҶеҸҚеә”еҲ¶еҫ—д№ҷй…ёд№ҷй…Ҝ5.28gпјҢеҲҷжң¬е®һйӘҢзҡ„дә§зҺҮжҳҜ__________пјҲдә§зҺҮжҢҮзҡ„жҳҜзӣ®ж Үз”ҹжҲҗзү©зҡ„е®һйҷ…дә§йҮҸдёҺзҗҶи®әдә§йҮҸзҡ„жҜ”еҖјпјүгҖӮ пјҲ3пјүдёҠиҝ°зү©иҙЁдёӯпјҢиғҪеҸ‘з”ҹеҠ жҲҗеҸҚеә”зҡ„зғғзұ»зү©иҙЁжңүпјҡ__________________________еЎ«еәҸеҸ·гҖӮ пјҲ4пјүдёӢеҲ—зү©иҙЁдёӯпјҢдёҚиғҪйҖҡиҝҮд№ҷзғҜеҠ жҲҗеҸҚеә”еҫ—еҲ°зҡ„жҳҜ______еЎ«еәҸеҸ·гҖӮ aпјҺCH3CH3В В В В В В В В В В bпјҺCH3CHCl2В В В В В В В В В В В В cпјҺCH3CH2BrВ В пјҲ5пјүиӢҜгҖҒз”ІиӢҜгҖҒдәҢз”ІиӢҜжҳҜз”ЁйҖ”е№ҝжіӣзҡ„жңүжңәжә¶еүӮгҖӮдәҢз”ІиӢҜзҡ„з»“жһ„жңү______з§ҚгҖӮ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||||||
|
дёӢиЎЁжүҖзӨәдёәйғЁеҲҶзҹӯе‘Ёжңҹе…ғзҙ зҡ„еҺҹеӯҗеҚҠеҫ„еҸҠдё»иҰҒеҢ–еҗҲд»·пјҢж №жҚ®иЎЁдёӯдҝЎжҒҜеҲӨж–ӯдёӢеҲ—еҸҷиҝ°дёҚжӯЈзЎ®зҡ„жҳҜ
AпјҺж°”жҖҒж°ўеҢ–зү©зҡ„зЁіе®ҡжҖ§HGпјһHFпјһH2E BпјҺA+гҖҒB2+гҖҒD3+гҖҒG-еӣӣз§ҚзҰ»еӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғзӣёеҗҢ CпјҺAдёҺж°§ж°”еҸҚеә”зҡ„дә§зү©д№ӢдёҖA2O2пјҢйҳҙзҰ»еӯҗе’ҢйҳізҰ»еӯҗзҡ„жҜ”дҫӢдёә1вҲ¶1 DпјҺCе…ғзҙ зҡ„еҺҹеӯҗжңҖеӨ–еұӮз”өеӯҗж•°зӯүдәҺз”өеӯҗеұӮж•°
|
|||||||||||||||||||||||||
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
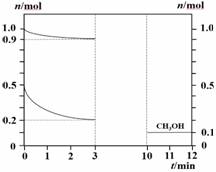
180в„ғж—¶е°Ҷ0.5mol H2е’Ң1mol CO2йҖҡе…Ҙ1Lзҡ„жҒ’е®№еҜҶй—ӯе®№еҷЁдёӯпјҢеҸҚеә”з”ҹжҲҗз”ІйҶҮи’ёжұҪпјҲCH3OHпјүе’Ңжҹҗж— жңәеүҜдә§зү©пјҢжөӢеҫ—еҗ„зү©иҙЁзҡ„зү©иҙЁзҡ„йҮҸйҡҸж—¶й—ҙзҡ„йғЁеҲҶеҸҳеҢ–еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ
AпјҺиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ2CO2+4H2 BпјҺеңЁ0пҪһ3minеҶ…H2зҡ„е№іеқҮеҢ–еӯҰеҸҚеә”йҖҹзҺҮдёә0.1molВ·LвҲ’1В·minвҲ’1 CпјҺеҪ“е®№еҷЁеҶ…ж··еҗҲж°”дҪ“еҜҶеәҰдёҚеҶҚеҸҳеҢ–ж—¶пјҢиЎЁжҳҺеҸҚеә”е·Із»ҸиҫҫеҲ°е№іиЎЎзҠ¶жҖҒ DпјҺеңЁ3пҪһ10minеҶ…пјҢеҸҚеә”д»ҚжңӘиҫҫеҲ°е№іиЎЎзҠ¶жҖҒ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
з”өеӯҗиЎЁдёӯз”өеӯҗи®Ўз®—еҷЁзҡ„з”өжәҗеёёз”Ёеҫ®еһӢ银й”ҢеҺҹз”өжұ пјҢе…¶з”өжһҒеҲҶеҲ«дёә AпјҺй”ҢжҳҜиҙҹжһҒпјҢж°§еҢ–银жҳҜжӯЈжһҒ BпјҺй”ҢеҸ‘з”ҹж°§еҢ–еҸҚеә”пјҢж°§еҢ–银еҸ‘з”ҹиҝҳеҺҹеҸҚеә” CпјҺжә¶ж¶Ідёӯ DпјҺйҡҸзқҖз”өжһҒеҸҚеә”зҡ„дёҚж–ӯиҝӣиЎҢпјҢз”өи§ЈиҙЁжә¶ж¶Ізҡ„pHдјҡеўһеӨ§
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
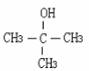
еӮ¬еҢ–ж°§еҢ–зҡ„дә§зү©жҳҜCH3-CH2-CH2-CHOзҡ„йҶҮжҳҜ AпјҺ CпјҺ
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
|
дёәдәҶйҷӨеҺ»жӢ¬еҸ·еҶ…зҡ„жқӮиҙЁпјҢе…¶иҜ•еүӮйҖүжӢ©е’ҢеҲҶзҰ»ж–№жі•йғҪжӯЈзЎ®зҡ„жҳҜ
|
|||||||||||||||||||||
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”дёӯеұһдәҺеҸ–д»ЈеҸҚеә”зҡ„жҳҜ AпјҺCH3CHпјқCH2пјӢBr2вҶ’CH3CHBrCH2Br BпјҺCH3COOHпјӢCH3CH2OH CпјҺ2CH3CH2OHпјӢO2 DпјҺCH3CH2OH
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰз”ЁиҜӯжҲ–жЁЎеһӢжӯЈзЎ®зҡ„жҳҜ AпјҺж°ҜеҢ–ж°ўзҡ„з”өеӯҗејҸпјҡ CпјҺ8дёӘдёӯеӯҗзҡ„зўіеҺҹеӯҗпјҡ12CпјҡВ В В В В В В В В В В В В В DпјҺCH4еҲҶеӯҗзҡ„жҜ”дҫӢжЁЎеһӢпјҡ
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||
|
ж №жҚ®е…ғзҙ е‘ЁжңҹеҫӢпјҢз”ұдёӢеҲ—дәӢе®һиҝӣиЎҢеҪ’зәіжҺЁжөӢпјҢжҺЁжөӢдёҚеҗҲзҗҶзҡ„жҳҜ
|
|||||||||||
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
100mL 6molВ·LвҲ’1зЎ«й…ёжә¶ж¶ІдёҺиҝҮйҮҸй”ҢзІүеҸҚеә”пјҢеңЁдёҖе®ҡжё©еәҰдёӢпјҢдёәдәҶеҮҸзј“еҸҚеә”йҖҹзҺҮдҪҶеҸҲдёҚеҪұе“Қз”ҹжҲҗж°ўж°”зҡ„жҖ»йҮҸпјҢеҸҜеҗ‘еҸҚеә”зү©дёӯеҠ е…ҘйҖӮйҮҸзҡ„ AпјҺзЎ«й…ёй’ҫжә¶ж¶ІВ В В В BпјҺзЎ«й…ёй“ңеӣәдҪ“В В В В В CпјҺзўій…ёй’ В В В В В DпјҺзғ§зўұжә¶ж¶І
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
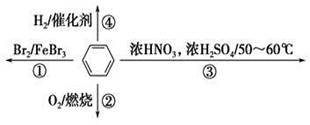
дёӢеҲ—е…ідәҺиӢҜзҡ„еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ
AпјҺеҸҚеә”в‘ дёәеҸ–д»ЈеҸҚеә”пјҢжңүжңәдә§зү©зҡ„еҜҶеәҰжҜ”ж°ҙе°Ҹ BпјҺеҸҚеә”в‘ўдёәеҸ–д»ЈеҸҚеә”пјҢжңүжңәдә§зү©жҳҜдёҖз§Қзғғ CпјҺеҸҚеә”в‘Ўдёәж°§еҢ–еҸҚеә”пјҢеҸҚеә”зҺ°иұЎжҳҜзҒ«з„°жҳҺдә®е№¶еёҰжңүиҫғеӨҡзҡ„й»‘зғҹ DпјҺеҸҚеә”в‘Ј1molиӢҜжңҖеӨҡдёҺ3mol H2еҸ‘з”ҹеҠ жҲҗеҸҚеә”пјҢжҳҜеӣ дёәиӢҜеҲҶеӯҗеҗ«жңүдёүдёӘзўізўіеҸҢй”®
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
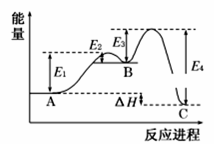
жҹҗеҸҚеә”з”ұдёӨжӯҘеҸҚеә”AвҶ’BвҶ’Cжһ„жҲҗпјҢе®ғзҡ„еҸҚеә”иғҪйҮҸжӣІзәҝеҰӮеӣҫпјҢдёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ
AпјҺдёӨжӯҘеҸҚеә”еқҮдёәеҗёзғӯеҸҚеә” BпјҺAдёҺCзҡ„иғҪйҮҸе·®дёәE4 CпјҺдёүз§ҚеҢ–еҗҲзү©дёӯзҡ„зЁіе®ҡжҖ§Bп№ӨAп№ӨC DпјҺAвҶ’BеҸҚеә”пјҢеҸҚеә”жқЎд»¶дёҖе®ҡиҰҒеҠ зғӯ
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺжІ№и„Ӯзҡ„еҸҷиҝ°дёҚжӯЈзЎ®зҡ„жҳҜ AпјҺжІ№и„ӮжҳҜжҢҮжІ№е’Ңи„ӮиӮӘпјҢе®ғ们дёҚеұһдәҺй…Ҝзұ» BпјҺжІ№и„ӮжІЎжңүеӣәе®ҡзҡ„зҶ”гҖҒжІёзӮ№ CпјҺжІ№и„ӮжҳҜй«ҳзә§и„ӮиӮӘй…ёзҡ„з”ҳжІ№й…Ҝ DпјҺжІ№и„ӮжҳҜдёҖз§Қжңүжңәжә¶еүӮпјҢеҸҜжә¶и§ЈеӨҡз§Қз»ҙз”ҹзҙ
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…із…Өе’ҢзҹіжІ№зҡ„з»јеҗҲеҲ©з”ЁдёҚеұһдәҺеҢ–еӯҰеҸҳеҢ–зҡ„жҳҜ AпјҺз…Өзҡ„ж°”еҢ–В В В В В BпјҺз…Өзҡ„е№ІйҰҸВ В В В В CпјҺзҹіжІ№зҡ„иЈӮи§ЈВ В В В В DпјҺзҹіжІ№зҡ„еҲҶйҰҸ
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еҗҲзү©дёӯпјҢеұһдәҺжһ„жҲҗеӨ©з„¶иӣӢзҷҪиҙЁзҡ„ж°Ёеҹәй…ёзҡ„жҳҜ AпјҺ CпјҺH2NвҖ”вҖ” CH2вҖ”CH2вҖ”COOHВ В В В В В В В В В В DпјҺ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
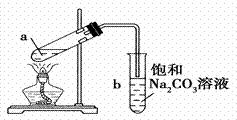
дёӢеӣҫдёәе®һйӘҢе®ӨеҲ¶еҸ–е°‘йҮҸд№ҷй…ёд№ҷй…Ҝзҡ„иЈ…зҪ®еӣҫгҖӮдёӢеҲ—е…ідәҺиҜҘе®һйӘҢзҡ„еҸҷиҝ°дёӯпјҢдёҚжӯЈзЎ®зҡ„
AпјҺиҜ•з®ЎbдёӯеҜјж°”з®ЎдёӢз«Ҝз®ЎеҸЈдёҚиғҪжөёе…Ҙж¶Ійқўзҡ„зӣ®зҡ„жҳҜйҳІжӯўе®һйӘҢиҝҮзЁӢдёӯдә§з”ҹеҖ’еҗёзҺ°иұЎ BпјҺе®һйӘҢж—¶еҠ зғӯиҜ•з®Ўaзҡ„зӣ®зҡ„д№ӢдёҖжҳҜеҠ еҝ«еҸҚеә”йҖҹзҺҮ CпјҺиҜ•з®ЎbдёӯйҘұе’ҢNa2CO3жә¶ж¶Ізҡ„дҪңз”ЁжҳҜеҗёж”¶йҡҸд№ҷй…ёд№ҷй…Ҝи’ёеҮәзҡ„е°‘йҮҸд№ҷй…ёе’Ңд№ҷйҶҮпјҢ并еҮҸе°‘д№ҷй…ёд№ҷй…Ҝзҡ„жә¶и§Ј DпјҺaиҜ•з®Ўдёӯе…ҲеҠ е…Ҙжө“зЎ«й…ёпјҢ然еҗҺиҫ№ж‘ҮеҠЁиҜ•з®Ўиҫ№ж…ўж…ўеҠ е…Ҙд№ҷйҶҮпјҢеҶҚеҠ еҶ°йҶӢй…ё
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ AпјҺи”—зі–гҖҒжһңзі–е’ҢйәҰиҠҪзі–еқҮдёәеҸҢзі– BпјҺе•Ҷд»ЈеҗҺжңҹй“ёйҖ еҮәе·ҘиүәзІҫж№ӣзҡ„еҸёжҜҚжҲҠйјҺпјҢиҜҘйјҺеұһдәҺй“ңеҗҲйҮ‘еҲ¶е“Ғ CпјҺжӨҚзү©жІ№еҗ«дёҚйҘұе’Ңи„ӮиӮӘй…ёй…ҜпјҢиғҪдҪҝBrвӮӮ/CCl4иӨӘиүІ DпјҺжұүд»Јзғ§еҲ¶еҮәвҖңжҳҺеҰӮй•ңгҖҒеЈ°еҰӮзЈ¬вҖқзҡ„з“·еҷЁпјҢе…¶дё»иҰҒеҺҹж–ҷдёәй»ҸеЈ«
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
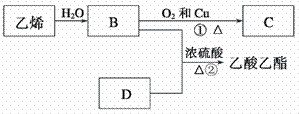
е·ІзҹҘд№ҷзғҜиғҪеҸ‘з”ҹд»ҘдёӢиҪ¬еҢ–пјҡ
пјҲ1пјүд№ҷзғҜзҡ„з»“жһ„з®ҖејҸдёә____________________гҖӮ пјҲ2пјүDдёӯе®ҳиғҪеӣўзҡ„еҗҚз§°пјҡ__________гҖӮ пјҲ3пјүзү©иҙЁBеҸҜд»Ҙиў«зӣҙжҺҘж°§еҢ–дёәDпјҢйңҖиҰҒеҠ е…Ҙзҡ„иҜ•еүӮжҳҜ_____________________гҖӮ пјҲ4пјүв‘Ўзҡ„еҸҚеә”зұ»еһӢ_________________________гҖӮ пјҲ5пјүеҶҷеҮәв‘ зҡ„еҢ–еӯҰж–№зЁӢејҸ___________________________________________гҖӮ
|
|
- 2019-2020е№ҙеәҰй«ҳдёҖеҗҺеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲпјҲе№ҝдёңзңҒзҸ жө·еёӮзҸ жө·дёҖдёӯ пјү
- зҰҸе»әзңҒеҺҰй—ЁеҸҢеҚҒдёӯеӯҰ2020еұҠй«ҳдёүдёҠжңҹ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰеңЁзәҝиҖғиҜ•йўҳе…Қиҙ№з»ғд№
- ж№–еҚ—зңҒйӮөйҳіеёӮйӮөдёңеҲӣж–°е®һйӘҢеӯҰж Ў2020-2021е№ҙй«ҳдәҢдёҠеӯҰжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§Јжһҗ
- 2019-2020е№ҙй«ҳдёҖдёӢеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰпјҲжІіеҢ—зңҒзҹіе®¶еә„еёӮ第дәҢдёӯеӯҰпјү
- 2018-2019е№ҙй«ҳдәҢдёҠеҚҠжңҹ12жңҲжңҲиҖғеҢ–еӯҰиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§ЈжһҗпјҲеҶ…и’ҷеҸӨиҮӘжІ»еҢәд№Ңе…°еҜҹеёғеёӮйӣҶе®ҒдёҖдёӯпјү
- зҰҸе·һеёӮй«ҳдёүеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•иҖғиҜ•е®Ңж•ҙзүҲ
- 2019еұҠй«ҳдёүжЁЎжӢҹиҖғиҜ• еҢ–еӯҰ WordзүҲеҗ«зӯ”жЎҲпјҲиҫҪе®ҒзңҒжҠҡйЎәеёӮжҠҡйЎәй«ҳдёӯпјү
- дёҠжө·еёӮ2018е№ҙй«ҳдёүеҢ–еӯҰдёҠеҶҢй«ҳиҖғжЁЎжӢҹиҜ•еҚ·е®Ңж•ҙзүҲ