第三节 硫和氮的氧化物 知识点题库
因具有放射性而被称为居室“隐形杀手”的是( )
A . 甲醛
B . 苯
C . 氡
D . 一氧化碳
如下图所示为城市自来水的处理示意图。水的净化需经沉淀、过滤、曝气、消毒等操作,有关水的净化说法不正确的是( )

城市自来水处理示意图
A . 沉淀池、砂滤器是污水处理的一级处理,除去污水中的不溶物
B . 曝气池为二级处理装置,是通过微生物的代谢作用,将污水中各种复杂的有机污染物降解为简单的无害的物质
C . 三级处理主要采用化学沉淀法、氧化还原法、离子交换法等对污水进行深度处理和净化
D . 混凝法是化学沉淀法中的一种,但它只有物理变化
Na、Al、Fe、Cu、Cl、Si、N、S是中学化学中重要的元素,请完成下列相关元素及其化合物的问题:
-
(1) 写出工业固氮合成氨的化学方程式
-
(2) 将Na2Fe5Si8O22(OH)2 写出氧化物的形式为
-
(3) 氢硫酸为弱酸,将H2S气体通入到FeCl3溶液中溶液出现淡黄色的沉淀,写出该反应的离子方程式
-
(4) 写出用Al与MnO2高温下反应制Mn的化学方程式
“天宫一号”与“神州八号”的对接成功是我国航天事业发展的又一里程碑.发射时运载火箭的推进剂引燃后,从尾部会喷出大量的高温气体,该气体的主要成分是CO2、H2O、N2、NO等,在发射现场可以看到火箭尾部产生大量红棕色气体,你认为其原因最有可能的是( )
A . 高温下N2遇空气生成了NO2
B . NO遇空气生成了NO2
C . CO2与NO反应生成CO和NO2
D . NO与H2O反应生成H2和NO2
溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末.制备CuBr的实验步骤如下:
步骤1.在如图所示的三颈烧瓶中加入45gCuSO4•5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时.
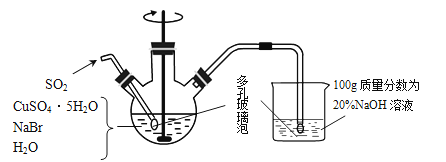
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤.
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤.
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥.
-
(1) 实验所用蒸馏水需经煮沸,煮沸目的是除去其中水中的 (写化学式)
-
(2) 步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为 ②控制反应在60℃进行,实验中可采取的措施是 ;
③说明反应已完成的现象是
-
(3) 步骤2过滤需要避光的原因是
-
(4) 步骤3中洗涤剂需“溶有SO2”的原因是 ;最后溶剂改用乙醚的目的是
-
(5) 欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3•7H2O晶体.
请补充实验步骤,须用到SO2(贮存在钢瓶中)、20%NaOH溶液、乙醇:
①
② .
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶.
④ .
⑤放真空干燥箱中干燥.
某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种金属离子,实验室设计了方案对废液进行以下三步处理,并回收金属.

请回答:
-
(1) 步骤①中得到的沉淀含有的金属单质有.
-
(2) 步骤②是将Fe2+转化为Fe3+ , 还可以选用的试剂是 .A . Fe粉 B . NaOH溶液 C . 新制氯水 D . 稀硫酸
-
(3) 步骤③中加入氨水生成红褐色沉淀的离子方程式为.
下列现象或事实可用同一原理解释的是( )
A . 氯水和活性炭使红墨水褪色
B . 浓硫酸和石灰水长期暴露在空气中浓度降低
C . 漂白粉和水玻璃长期暴露在空气中变质
D . SO2可使品红和酸性高锰酸钾溶液褪色
在喷泉实验的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹子,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( )
a(干燥气体) | b(液体) | |
A | NO2 | 水 |
B | CO2 | 4mol/L NaOH溶液 |
C | Cl2 | 饱和NaCl溶液 |
D | NO | 水 |
A . A
B . B
C . C
D . D
用如图所示的实验装置,比较SO2和Cl2的漂白性.
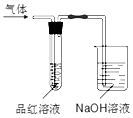
请回答下列问题:
-
(1) 若装置中通入一段时间的SO2 , 观察到试管中的品红溶液,然后再加热试管,溶液又呈现红色;
-
(2) 若装置中通入一段时间的氯气,观察到试管中的品红也褪色,生成的具有漂白性的物质是( 填化学式),然后再加热试管,溶液;
-
(3) 由以上两个实验可以说明SO2和Cl2的漂白原理 (填“相同”或“不相同”);
-
(4) 实验中NaOH溶液的作用是.
下列解释物质用途或现象的反应方程式不准确的是( )
A . 硫酸型酸雨的形成会涉及反应:2H2SO3+O2  2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H
Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H  ═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
 2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H
Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H  ═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
“天更蓝、山更绿、水更清、环境更优美”是我们的共同愿望。下列说法错误的是( )
A . PM2.5是指粒径不大于2.5µm的可吸入悬浮颗粒物
B . 煤经过气化和液化等物理变化可转化为清洁能源
C . 开展植树造林、增加植被面积,可吸收大量CO2
D . 生活污水直接排放,可引起水体富营养化
化学与科技、社会、生产、生活等关系密切,下列有关说法错误的是 ( )
A . 35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果
B . 营养物质淀粉、纤维素和蛋白质都属于高分子化合物
C . 苯酚不小心沾到皮肤上,可用酒精进行洗涤以减轻伤害
D . 提倡人们购物时不用塑料袋,是为了防止白色污染
下列有关实验操作、现象、解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 充分吸收了Na2SiO3 饱和溶液的小木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3 可作防火剂 |
| B | 将H2 在充满Cl2 的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2 化合生成HCl |
| C | 将SO2 通入酸性高锰酸钾溶液中 | 溶液褪色 | SO2 具有漂白性 |
| D | 用分别蘸有浓盐酸和浓氨水的玻璃棒相互靠近 | 冒白烟 | NH3 具有还原性 |
A . A
B . B
C . C
D . D
 、
、  、
、  (超氧化氢)等都属氢氧化合物,其中
(超氧化氢)等都属氢氧化合物,其中  又叫超氧酸,与
又叫超氧酸,与  化学性质相似,又与
化学性质相似,又与 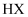 (
( 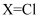 、
、 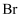 、I等)某些性质相似,下列说法错误的是( )
、I等)某些性质相似,下列说法错误的是( )
A . 向  溶液中滴入品红溶液,品红褪色,加热后红色不恢复
B .
溶液中滴入品红溶液,品红褪色,加热后红色不恢复
B .  在碱中能稳定存在
C .
在碱中能稳定存在
C .  不稳定,分解会生成氧气
D .
不稳定,分解会生成氧气
D .  可与
可与 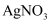 溶液反应:
溶液反应: 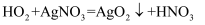
 溶液中滴入品红溶液,品红褪色,加热后红色不恢复
B .
溶液中滴入品红溶液,品红褪色,加热后红色不恢复
B .  在碱中能稳定存在
C .
在碱中能稳定存在
C .  不稳定,分解会生成氧气
D .
不稳定,分解会生成氧气
D .  可与
可与 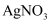 溶液反应:
溶液反应: 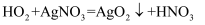
化学与科技、社会、生产、生活等关系密切,下列有关说法错误的是( )
A . 苯酚不小心沾到皮肤上,可用酒精进行洗涤以减轻伤害
B . 营养物质淀粉、纤维素和蛋白质都属于高分子化合物
C . 提倡人们购物时不用塑料袋,是为了防止白色污染
D . 35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果
下列说法错误的是( )
A . 二氧化硅导电能力强,可用于制造光导纤维
B . 石灰石在高温下可用于消除燃煤烟气中的SO2
C . 可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油
D . 利用催化剂可减少汽车尾气中有害气体的排放
下列说法错误的是( )
A .  与
与  互为同系物
B . 有机化合物
互为同系物
B . 有机化合物  与
与  是同分异构体
C .
是同分异构体
C .  与
与  是氮元素的两种核素
D . 金刚石、足球烯、纳米碳管互为同素异形体
是氮元素的两种核素
D . 金刚石、足球烯、纳米碳管互为同素异形体
 与
与  互为同系物
B . 有机化合物
互为同系物
B . 有机化合物  与
与  是同分异构体
C .
是同分异构体
C .  与
与  是氮元素的两种核素
D . 金刚石、足球烯、纳米碳管互为同素异形体
是氮元素的两种核素
D . 金刚石、足球烯、纳米碳管互为同素异形体
在“价—类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。如图中的字母分别代表硫及其常见化合物,相关推断不合理的是( )
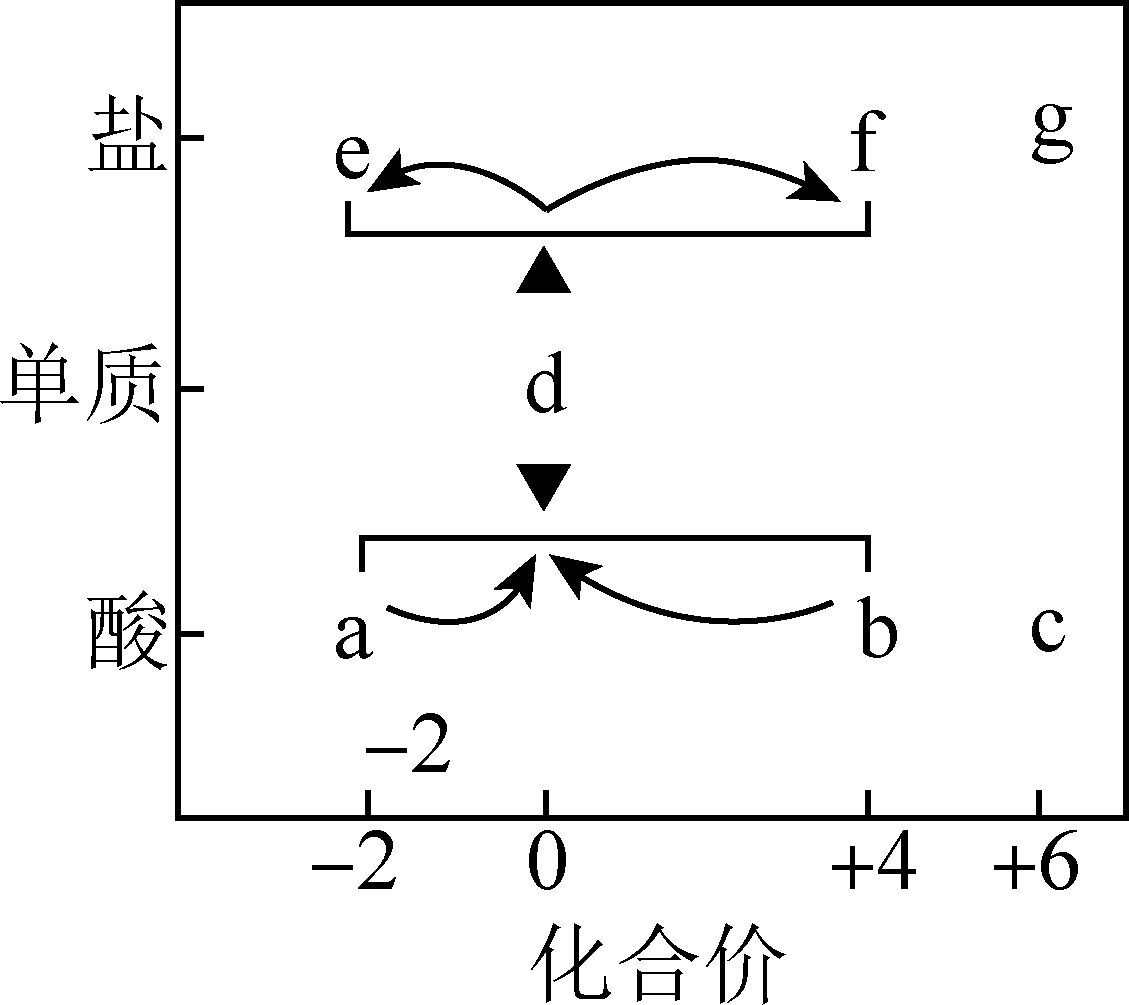
A . b既具有氧化性又具有还原性
B . 硫酸型酸雨的形成过程涉及b到c的转化
C . a溶液与b溶液反应过程中有淡黄色沉淀生成
D . d在加热下与强碱溶液反应生成e和f,且n(e):n(f)=1:2
化学与社会、生活、生产密切相关,下列有关说法错误的是。( )
A . 2022年北京冬奥会开幕式上绚丽多彩的焰火,主要利用了“焰色反应”的知识
B . 航天员所穿航天服的主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C . “闽鹭”是我国制造的第四艘LNG船。船底镶嵌锌块,锌作正极,以防船体被腐蚀
D . 低碳生活需要节能减排,使用太阳能代替化石燃料,可减少温室气体的排放
下列说法错误的是( )
A .  与
与 互为同位素
B . 甘氨酸和硝基乙烷互为同分异构体
C .
互为同位素
B . 甘氨酸和硝基乙烷互为同分异构体
C . 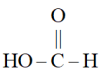 和
和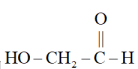 互为同系物
D .
互为同系物
D .  和
和 互为同素异形体
互为同素异形体
 与
与 互为同位素
B . 甘氨酸和硝基乙烷互为同分异构体
C .
互为同位素
B . 甘氨酸和硝基乙烷互为同分异构体
C . 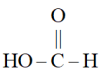 和
和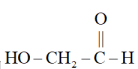 互为同系物
D .
互为同系物
D .  和
和 互为同素异形体
互为同素异形体
最近更新



