第三节 硫和氮的氧化物 知识点题库
①若不考虑SO2与水的反应向BaCl2溶液中通入SO2无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”。 。原因是。
②沉淀A的化学式为,该沉淀能否溶于稀盐酸?。
③写出生成沉淀B的离子方程式:。
④生成2.33 g沉淀B,需消耗标准状况下的Cl2mL。
煤是重要的能源,也是化工生产的重要原料.
(1)煤燃烧产生的废气直接排放到空气中,可能导致的环境污染问题是 .
(2)下图是对煤燃烧产生的废气进行常温脱硫处理的流程示意图.
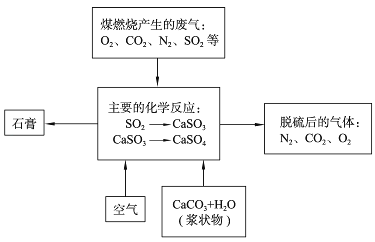
①废气脱硫过程中,主要反应的化学方程式为
②在煤中直接添加一种物质,可有效减少煤燃烧产生的SO2 , 该物质是
③石膏在工业生产中的用途是 (写出一种用途即可).
(3)煤经过 (填加工方法)可以得到炉煤气、煤焦油和焦炭.煤焦油经过 (填加工方法)可得到芳香族化合物.煤也可以用氢化法转化成燃油,氢化法的本质是
资料:氰化钠白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化 氢、水溶液呈碱性.
-
(1) 白磷有毒,能和氯酸溶液发生氧化还原反应:3P4+10HClO3+18H2O⇌10HCl+12H3PO4 , 该反应的氧化产物是,若有1mo1P4参加反应转移电子为 mol.
-
(2) 氰化钠(NaCN)是一种化工原料,用于基本化学合成、电镀、冶金和有机合成医药、农药及金属处理等方面.
①已知:25℃时,HCN的电离平衡常数1=6.2×10﹣10 , H2CO3在25℃时的电离平衡常数是Ka1=4.5×10﹣7、Ka2=4.7×10﹣11 , 则向NaCN溶液通入少量CO2反应方程式是:.
②常温下,氰化钠能与过氧化氢溶液反应,生成碳酸氢钠和能使湿润的红色石蕊试纸变 蓝色的气体,大大降低其毒性.该反应的化学方程式是:.
-
(3)
实验室通过如图所示装置制备Na2SO3 .
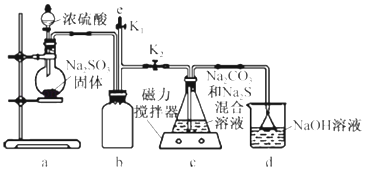
装置a中盛装Na2SO3固体的仪器名称是;装置b的作用是
① 装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2 CO3 , 还可能有.
②实验结束后,在e处最好连接盛(选填“NaOH溶液”、“水”、“CCl4”中任一种.
-
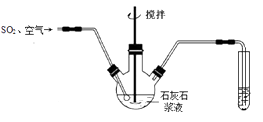
(1) 实验中为提高石灰石浆液脱硫效率采取的措施是,写出通入SO2和空气发生反应生成石膏(CaSO4·2H2O)的化学方程式。
-
(2) 将脱硫后的气体通入KMnO4溶液,可粗略判断烟气脱硫效率的方法是。
-
(3) 研究发现石灰石浆液的脱硫效率受pH和温度的影响。烟气流速一定时,脱硫效率与石灰石浆液pH的关系如图所示,在为5.7时脱硫效果最佳,石灰石浆液5.7<pH<6.0时,烟气脱硫效果降低的可能原因是,烟气通入石灰石浆液时的温度不宜过高,是因为。
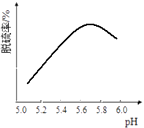
-
(4) 石灰石烟气脱硫得到的物质中的主要成分是CaSO4和CaSO3 , 实验人员欲测定石灰石浆液脱硫后的物质中CaSO3的含量,以决定燃煤烟气脱硫时通入空气的量。请补充完整测定CaSO3含量的实验方案:取一定量石灰石烟气脱硫后的物质,。[浆液中CaSO3能充分与硫酸反应。实验中须使用的药品:75%的硫酸、标准浓度的(NH4)2Fe(SO4)2溶液,标准浓度的酸性KMnO4溶液]
| 选项 | 目的 | 实验 |
| A | 除去溴苯中的溴 | 加蒸馏水后振荡、分液 |
| B | 验证SO2的漂白性 | 将SO2通入高锰酸钾溶液中 |
| C | 区分葡萄糖溶液和淀粉溶液 | 往两溶液中分别滴加KI溶液 |
| D | 比较浓H2SO4与浓HNO3的氧化性的强弱 | 常温下,将铜丝分别插入两溶液中 |
 O与H
O与H 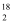 O互为同素异形体
D . Na和Na+属于同种元素,且性质相同
O互为同素异形体
D . Na和Na+属于同种元素,且性质相同
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究 | 取少量浓硝酸加热分解,将产物先通入浓硫酸,后用集气瓶收集气体 | 将带火星的木条放置瓶内,木条复燃,不能说明 |
| B | 鉴别NaCl和 | 分别取少量溶液于试管中,然后滴加酸性的 | 若紫红色退去,则该溶液为NaCl溶液 |
| C | 向盛有 | 溶液变成棕黄色,一段时间后产生气泡,随后生成红褐色沉淀。 | |
| D | 探究淀粉在酸性条件下的水解程度 | 取少量淀粉溶液,加入适量稀硫酸加热5min后,再加NaOH中和硫酸,最后滴加碘水 | 溶液无明显现象,则淀粉完全水解 |
①减少化石燃料使用 ②发展CO2捕集技术 ③燃煤中加入石灰石 ④开发新的能源
 B .
B .  C .
C .  D .
D . 
 均可使溴水褪色,褪色原理相同
均可使溴水褪色,褪色原理相同
 气体的还原性,下列说法错误的是( )
气体的还原性,下列说法错误的是( )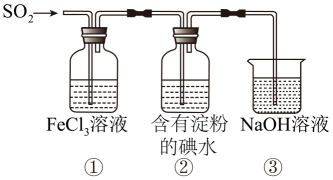
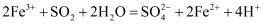 B . ①中加入
B . ①中加入 溶液,紫红色褪去,可说明
溶液,紫红色褪去,可说明 与
与 发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明
发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明 的还原性强于
的还原性强于 D . 装置③的作用是吸收
D . 装置③的作用是吸收 尾气,防止污染空气
尾气,防止污染空气
 能否支持燃烧
能否支持燃烧 溶液
溶液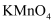
 溶液的试管中滴入几滴硫酸酸化的硫酸亚铁
溶液的试管中滴入几滴硫酸酸化的硫酸亚铁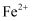 被
被  ;
;  ,且反应放热,促进了
,且反应放热,促进了 


