第二节 金属的腐蚀和防护 知识点题库
下图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是 ( )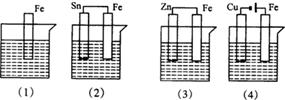
A . (4)>(2)>(1)>(3)
B . (4)>(2)>(3)>(1)
C . (2)>(1)>(3)>(4)
D . (3)>(2)>(4)>(1)
化学与社会、生产、生活密切相关.下列说法错误的是( )
A . 油脂和草木灰的混合物有一定的去污能力,在热水中去污能力更强
B . 胶体粒子吸附电荷是胶体相对稳定的主要原因,中和所带电荷可以使胶体聚沉
C . 在船底镶嵌锌块以保护船体的方法叫阴极电保护法,利用的是原电池原理
D . 过多的汽车尾气排放物容易造成雾霾、酸雨和光化学污染等环境污染问题
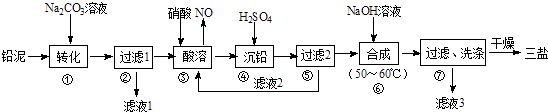
利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbO•PbSO4•H2O (三盐),主要制备流程如下:
-
(1) 步骤①PbSO4转化为难溶PbCO3的离子方程式为.
-
(2) 滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为(写化学式).
-
(3) 步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为;滤液2中溶质主要成分为 (写化学式).
-
(4) 步骤⑥合成三盐的化学方程式为.
-
(5) 步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是.
下列各种方法中,能对金属起到防止或减缓腐蚀作用的是( )
①金属表面涂抹油漆 ②改变金属内部结构 ③保持金属表面清洁干燥 ④金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜.
A . ①②③④
B . ①③④⑤
C . ①②④⑤
D . 全部
下列各装置中都盛有0.1mol•L﹣1的NaCl溶液,放置一定时间后,装置中的四块相同锌片,腐蚀速率由快到慢的顺序是( )
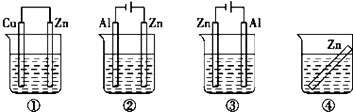
A . ③①④②
B . ①②④③
C . ①②③④
D . ②①④③
有关金属腐蚀的论述,正确的是( )
①金属的腐蚀一定伴有电流产生
②纯银器表面在空气中因化学腐蚀渐渐变暗
③可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
④发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀
⑤发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子
⑥当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
⑦海轮外壳连接锌块以保护外壳不受腐蚀.
A . ②③⑤⑦
B . ①②③⑥⑦
C . ①②④⑦
D . ②③⑤⑥⑦
下列叙述不正确的是( )
A . 铁制品表面镀锌可以增强其抗腐蚀性
B . 在海轮外壳上连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
C . 马口铁(镀锡)外层镀层被破坏后,里面的铁更易被腐蚀
D . 利用外加电流的阴极保护法,可以将水下的钢闸门与电源正极相连
下列事实不能用电化学理论解释的是( )
A . 轮船水线以下的船壳上装上一定数量的锌块
B . 银质奖章久置后表面变暗
C . 黄铜(铜锌合金)制作的铜锣不易产生铜绿
D . 纯锌与稀H2SO4反应滴入少量的CuSO4溶液后反应速率加快
如图各烧杯中都是天然水,纯铁腐蚀由快到慢的顺序是( )
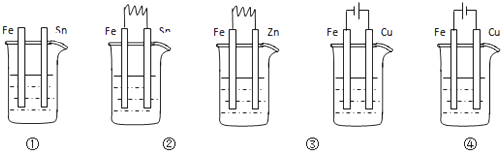
A . ⑤②①④③
B . ③②⑤④①
C . ⑤④②③①
D . ⑤②①③④
下列叙述正确的是( )
A . 金属腐蚀就是金属失去电子被还原的过程
B . 将水库中的水闸(钢板)与外加直流电源的负极相连接,可防止水闸被腐蚀
C . 合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强
D . 铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe﹣3e+=Fe3+ , 继而形成铁锈
下列说法不正确的是( )
A . 碘酒可使蛋白质变性,故能消毒杀菌
B . 天然氨基酸能溶于强酸或强碱溶液,是两性化合物
C . 食盐、糖、醋可作调味剂,不可用作食品防腐剂
D . 船舶外壳装上锌块,是牺牲阳极的阴极保护法进行防腐
化学与生活、环境密切相关,下列说法错误的是( )
A . 补铁剂与维生素C共同服用可提高补铁效果
B . 铁粉和碳粉的混合物可作食品抗氧化剂
C . 生活中钢铁制品生锈主要是析氢腐蚀所致
D . 新能源汽车的推广使用有助于减少光化学烟雾
下列说法或表达正确的是( )
①次氯酸的电子式为 ![]()
②含有离子键的化合物都是离子化合物
③等质量的O2与O3中,氧原子的个数比为3:2
④丁达尔效应可用于区分溶液和胶体,云、雾均能产生丁达尔效应
⑤将金属Zn与电源的负极相连,可防止金属Zn被腐蚀
⑥稀硫酸、氨水均为电解质
A . ②④⑤
B . ②④
C . ①③⑤
D . ①②③
金属材料的开发一直是材料科学的研究热点,一些新的金属材料相继被开发出来并应用于工农业生产和高科技领域。例如,铀(U)用作核电厂反应堆的核燃料,镅(Am)在烟雾探测器中用作烟雾监测材料;特点是被誉为“21世纪的金属”——钛(Ti),应用前景更为广阔。钛(titanium)是一种活泼金属,但因其表面容易形成致密的氧化物保护膜使它不易跟其他物质反应,而具有一定的抗腐蚀能力。除此之外,它还具有熔点高、硬度大、可塑性强、密度小等优点。根据以上背景资料及所学知识,你认为下列说法中错误的是( )
A . 钛不属于稀土金属
B . 钛是很好的航天航空材料
C . 钛在空气中不与其他物质反应
D . 钛有较好的抗腐蚀能力,是很好的防腐材料
对下列过程的化学用语表述正确的是( )
A . 用硫酸铜溶液除去乙炔中的硫化氢气体:H2S+Cu2+=CuS↓+2H+
B . 向氯化铝溶液中滴入过量氨水:Al3++4OH-=AlO2-+2H2O
C . 用电子式表示Na和Cl形成NaCl的过程: 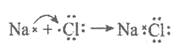 D . 钢铁发生电化学腐蚀的正极反应:Fe-3e-=Fe3+
D . 钢铁发生电化学腐蚀的正极反应:Fe-3e-=Fe3+
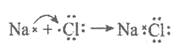 D . 钢铁发生电化学腐蚀的正极反应:Fe-3e-=Fe3+
D . 钢铁发生电化学腐蚀的正极反应:Fe-3e-=Fe3+
下列防止钢铁腐蚀的方法不属于电化学防护的是( )
A . 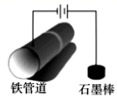 B .
B . 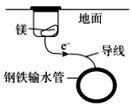 C .
C . 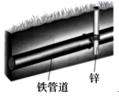 D .
D . 
 B .
B .  C .
C .  D .
D . 
下列实际应用,解释错误的是( )
A . 工业采用高压合成NH3——勒夏特列原理
B . 石膏降低Na2CO3盐碱地的碱性——离子互换反应的规律
C . 在船身上装锌块来避免船体遭受腐蚀——牺牲阳极的阴极保护法
D . 接触室中装有热交换器——防止催化剂中毒
我国自主研发的新一代动车组在京沪高铁上跑出过486.1公里的世界列车最高时速,这得益于全路铺设的优质无缝平滑的超长钢轨。下列有关说法不正确的是( )
A . 制造钢轨的材料是钢,钢是用量最大的合金
B . 在空气中将金属钛、铝混合后熔化可制得铝合金,强度、硬度比铝大
C . 在我国使用最早上合金是铜合金
D . 不锈钢的合金元素主要是铬和镍
下列叙述正确的是( )
A . 需要通电才可进行的有:电离、电解、电泳、电镀、电化学腐蚀
B . 盐卤(含MgCl2)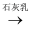 Mg(OH)2
Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
C . 煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化
D . 淀粉、蛋白质、纤维素、油脂都是高分子化合物,氨水、王水、双氧水都是混合物
Mg
C . 煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化
D . 淀粉、蛋白质、纤维素、油脂都是高分子化合物,氨水、王水、双氧水都是混合物
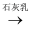 Mg(OH)2
Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
C . 煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化
D . 淀粉、蛋白质、纤维素、油脂都是高分子化合物,氨水、王水、双氧水都是混合物
Mg
C . 煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化
D . 淀粉、蛋白质、纤维素、油脂都是高分子化合物,氨水、王水、双氧水都是混合物
金属腐蚀现象普遍存在。下列事实与电化学腐蚀有关的是( )
A . 金属钠置于空气中变暗
B . 铝片浸入浓硝酸中产生致密的氧化膜
C . 黄铜(铜锌合金)制作的铜锣不易生成铜绿
D . 铁在  和
和  的混合溶液中发蓝、发黑
的混合溶液中发蓝、发黑
 和
和  的混合溶液中发蓝、发黑
的混合溶液中发蓝、发黑
最近更新



