第二节 金属的腐蚀和防护 知识点题库
-
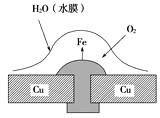
(1) 铁锅的锈蚀是腐蚀(填“析氢”或“吸氧”)。
-
(2) 写出铁锅腐蚀时负极的电极反应式:。
-
(3) 写出铁锅在中性条件下正极的电极反应式:。
-
(4) 写出电化学反应的总方程式:。
某工厂的酸性废水中含有大量的Fe3+、Cu2+、SO42﹣和少量Na+ . 为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾.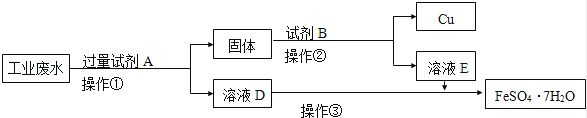
(1)工业废水中加入试剂A后,反应的离子方程式为Fe+Cu2+═Fe2++Cu、Fe+2H+═Fe2++H2↑、 .
(2)试剂B是 .
(3)①~③中均涉及的实验操作是 .
(4)可用绿矾消除工业废水中+6价铬(Cr2O72﹣)的污染,使之转化为Cr3+ , 若处理1t废水(含Cr2O72﹣ 10﹣3 mol/kg),则需加入绿矾的质量至少为 g .
-
(1) 水是一种宝贵的资源,保护水资源就是保护我们的生命.
①下列做法不利于水资源保护的是(填字母代号)
A.科学合理使用农药 B.任意排放化工厂废水 C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃.根据垃圾分类方法,矿泉水瓶属于(填“可回收物”或“可堆肥垃圾”);
③在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向大气的排放,减小环境污染.在催化转化器中,CO和NO发生反应.请完成该反应的化学主程式.
-
(2)
保护环境、爱护地球已成为人们的共同呼声.
①我们常在公共场所见到下列标志,其中属于回收标志的是

②2014年1月,教育部规定在学校公共场所禁止吸烟.下列有关说法中,不正确的是.
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO尼古丁和都属于室内空气污染物
-
(3) 化学与生活关系密切.现有下列四种物质:
A.蛋白质 B.亚硝酸盐 C.维生素C D.油脂
① 是重要的体内能源;
②广泛存在于新鲜水果和绿色蔬菜中,有酸性和还原性,又称为抗坏血酸;
-
(4) 材料是人类赖以生存和发展的重要物质基础
①试管、烧杯和烧瓶等化学仪器的主要材质是;
A.玻璃 B.陶瓷 C.水泥
②“辽宁号”航母的服役举世瞩目.钢铁是制造航母的主要材料.生铁和钢成分上的主要差别是;
A.碳的含量不同 B.磷、硫的含量不同 C.镍、铬等金属含量不同
③钢铁在潮湿空气中易发生吸氧腐蚀,负极反应式为.
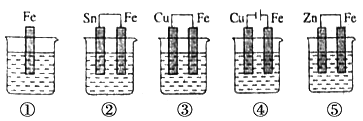
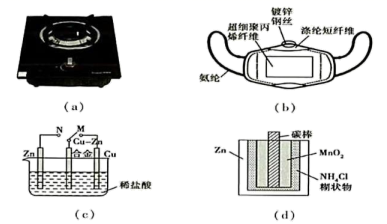
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤电泳

-
(1) 经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为。
-
(2) 为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。

①下列说法错误的是。
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为。
-
(3) 船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。
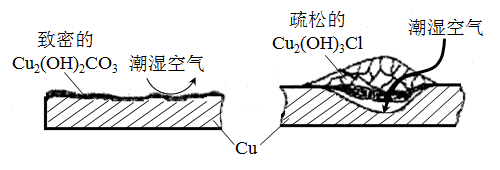
下列说法正确的是
A.疏松的Cu2(OH)3Cl属于有害锈
B.Cu2(OH)2CO3既能溶于盐酸也能溶于氢氧化钠溶液
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO3溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
②文献显示Cu2(OH)3Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,可以使CuCl转化为难溶的Cu2(OH)2CO3反应的离子方程式为。
-
(4) 考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析“脱盐、干燥”的防腐原理:。
选项 | 家务劳动 | 化学知识 |
A | 用温热的纯碱溶液清洗油污 | 油脂在热的纯碱溶液中更易发生水解 |
B | 白醋除去水垢中的CaCO3 | 醋酸酸性强于碳酸 |
C | “84消毒液”稀释后拖地 | 利用NaClO的还原性消毒杀菌 |
D | 餐后将洗净的铁锅擦干 | 减缓铁的锈蚀 |



