实验3-4 酸碱滴定曲线的测绘 知识点题库
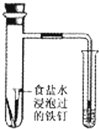 通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸氧腐蚀
C . 均不能采取将溶液直接蒸干的方法制得AlCl3、Al2(SO4)3、FeCl3、Fe2(SO4)3
D . 滴定用的滴定管、锥形瓶和配制一定物质的量浓度溶液用的容量瓶,使用前均要润洗
通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸氧腐蚀
C . 均不能采取将溶液直接蒸干的方法制得AlCl3、Al2(SO4)3、FeCl3、Fe2(SO4)3
D . 滴定用的滴定管、锥形瓶和配制一定物质的量浓度溶液用的容量瓶,使用前均要润洗

A | 乙烯使溴水褪色 苯使溴水褪色 | 均发生了加成反应 |
B | 用pH试纸测定某盐酸的pH 用红色石蕊试纸检验某气体为氨气 | 试纸均需要蒸馏水湿润 |
C | MnO2与浓盐酸反应制备Cl2 CaCO3与稀盐酸反应制备CO2 | 均发生氧化还原反应 |
D | 淀粉在酶的作用下生成葡萄糖 蛋白质在酶的作用下生成氨基酸 | 均发生了水解反应 |
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制浓硫酸和浓硝酸的混合酸时,将浓硝酸沿器壁慢慢加入到浓硫酸中,并不断搅拌;
③用pH试纸测得氯水的pH为2;
④用稀硝酸清洗做过银镜反应实验的试管;
⑤浓硝酸保存在棕色细口瓶中;
⑥将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡
⑦某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+ .

 ,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则
,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则  减小
减小
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;
②测定新制氯水的  时,先用玻璃棒蘸取液体滴在
时,先用玻璃棒蘸取液体滴在  试纸上,再与标准比色卡对照;
试纸上,再与标准比色卡对照;
③用米汤直接检验食用盐中是否含有碘元素;
④  在5.6~7.0之间的降水通常称为酸雨;
在5.6~7.0之间的降水通常称为酸雨;
⑤加入 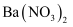 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有
溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有  存在;
存在;
⑥  通入紫色石蕊试液,溶液先变红后褪色;
通入紫色石蕊试液,溶液先变红后褪色;
⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便转移到容量瓶中,导致结果偏高;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤;
⑨蒸干 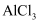 溶液可得纯净的无水氯化铝;
溶液可得纯净的无水氯化铝;

 B . A点溶液的
B . A点溶液的 小于C点溶液的
小于C点溶液的 C . D点溶液中:
C . D点溶液中: D . 随着
D . 随着 溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
 D . 0.01mol/L
D . 0.01mol/L 溶液中存在:
溶液中存在:

 <
< C . 向b点溶液中通入CO2可使b点溶液向c点溶液转化
D . b点对应的溶液中存在:3c(Ca2+)+c(K+)+c(H+)=3c(
C . 向b点溶液中通入CO2可使b点溶液向c点溶液转化
D . b点对应的溶液中存在:3c(Ca2+)+c(K+)+c(H+)=3c(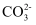 )+c(OH−)+c(Cl−)
)+c(OH−)+c(Cl−)
编号 | 实验操作 | 实验结论 |
A | 室温下,用pH试纸测定浓度均为 | 两溶液中水的电离程度相同 |
B | 向饱和 | 酸性: |
C | 将 |
|
D | 相同温度下,向浓度均为 |
|
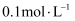 的KCl溶液和
的KCl溶液和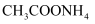 溶液的pH,pH都等于7
溶液的pH,pH都等于7 溶液中通入适量
溶液中通入适量 , 将所得气体一次通入品红溶液和澄清石灰水,品红不褪色,石灰水变浑浊
, 将所得气体一次通入品红溶液和澄清石灰水,品红不褪色,石灰水变浑浊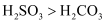
 溶液滴入酸性
溶液滴入酸性 溶液中,溶液紫红色褪去
溶液中,溶液紫红色褪去 具有还原性
具有还原性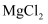 、
、 的混合溶液中逐滴加入氨水,先出现蓝色沉淀
的混合溶液中逐滴加入氨水,先出现蓝色沉淀



