氧气的性质和利用 知识点题库
自来水消毒过程中常会发生甲、乙两个化学反应。其反应的微观过程可用下图表示

下列说法正确的是( )
A . 物质a、d都是氧化物
B . 气体b不能用排水法收集
C . 物质c的溶液pH 大于7
D . 气体e具有可燃性
有CO2、N2、O2三种气体,能让燃着的木条燃烧更旺的是 .小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是 , 所得溶液的pH 7(选填“<”、“=”或“>”).
下列实验中的做法错误的是( )
A . 用红磷燃烧测定空气中氧气的含量时,用足量的红磷
B . 做铁丝在氧气中燃烧实验前,在集气瓶内铺一层细沙
C . 排水法收集气体,当导管口刚有气泡冒出时立即收集
D . 蒸发操作中,当蒸发皿中出现较多量固体时停止加热
做铁丝在氧气中燃烧的实验时,要先点燃铁丝上系着的火柴,再伸入集满氧气的集气瓶中,火柴燃烧所起的作用是( )
A . 升高铁丝的着火点
B . 升高铁丝的温度
C . 增加可燃物
D . 增大与氧气的接触面积
比较、推理是化学学习常用的方法.以下是根据一些反应事实推导出的影响化学反应的因素,其中不合理的是( )
序号 | 化学反应事实 | 影响反应的因素 |
A | 过氧化氢遇二氧化锰后迅速分解,水遇二氧化锰不分解 | 催化剂 |
B | 镁与盐酸反应生成氢气,铜与盐酸不反应 | 反应物的种类 |
C | 碳在常温下不与氧气反应,在点燃时能与氧气反应 | 反应的温度 |
D | 红热的铁丝在空气中很难燃烧,在氧气中能剧烈燃烧 | 反应物的浓度 |
A . A
B . B
C . C
D . D
如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )

A . Ⅰ类反应放出热量,Ⅱ类反应吸收热量
B . Fe在Ⅰ、Ⅱ两类反应中的产物相同
C . Ⅰ、Ⅱ两类反应均体现了氧气的氧化性
D . S,P在氧气中燃烧均会产生大量白烟
对物质的性质进行比较归纳,有利于更好地学习科学。下列对物质性质的归纳中,正确的是( )
A . H2、O2、CH4都具有可燃性
B . 浓硫酸、浓盐酸、酒精都具有挥发性
C . H2、C,CO都能和CuO发生置换反应
D . Fe、Al、Cu都能和AgNO3溶液发生置换反应
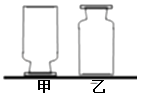
如图,在实验台上放置两瓶气体,集气瓶甲、乙中分别盛有CO2、O2、H2中的一种。
-
(1) 如果其中一瓶是氧气,则你认为是瓶。
-
(2) 将一种溶液(填化学式)倒入乙瓶中,振荡,若出现浑浊,则乙瓶中是CO2气体。
通过一年的化学学习,我们熟悉了许多物质.请从①石墨;②活性炭;③金刚石;④氢气;⑤二氧化碳;⑥氧气中,选取相应物质的序号填空.
-
(1) 其固态可作制冷剂、人工降雨
-
(2) 最清洁的燃料是
-
(3) 可用于冰箱除异味的是
-
(4) 用于切割玻璃是
-
(5) 用于急救病人的气体是
-
(6) 可作干电池电极的是.
将下列有关性质、变化、现象不同的原因填写在横线上:
-
(1) 金刚石和石墨的硬度不同,主要原因是它们的不同;
-
(2) 硫在空气中和在氧气中燃烧的现象不同,主要原因是不同;
-
(3) CaCl2能跟Na2CO3反应而NaCl不能,主要原因是它们含有的不同.
下列说法正确的是( )
A . 红磷在空气中燃烧产生大量白雾
B . 铁丝伸入盛有氧气的集气瓶中剧烈燃烧
C . 液态氧可用作发射火箭的燃料
D . 通过低温加压,可使氧气液化成淡蓝色的液体
下列现象可用氧气的物理性质解释的是( )
A . 白磷在40℃时即可燃烧,烈日下白磷不经点燃就可燃烧
B . 红色的铜经加热表面生成黑色的氧化铜
C . 实验室制取氧气时,最好用排水法而不用排气取气法收集
D . 氧气可使带火星的木条燃烧
下列实验操作的先与后正确的是( )
A . 检查装置气密性时,先用手握住试管,再将导气管的一端浸到水里
B . 先装入药品,再检查装置气密性
C . 收集完氧气后先熄灭酒精灯,再将导气管移出水面
D . 先在集气瓶底部铺一层细沙,再把系有燃着的火柴的铁丝伸入集气瓶中
类推是化学学习中常用的思考方法.以下四个类推结果正确的是( )
A . 氧化反应都会放出热量,所以放出热量的变化都是氧化反应
B . 化学变化生成了新物质,所以初中阶段有新物质生成的变化都是化学变化
C . 氧气是无色无味的气体,所以无色无味的气体就是氧气
D . 分解反应生成了多种物质,因此只要生成了两种或两种以上物质的化学反应就应该是分解反应
对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
实验装置 | 解释 | |
A |
| 集气瓶中的水:吸收放出的热量 |
B |
| 烧杯中的水:加热铜片,隔绝空气 |
C |
| 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 |
D |
| 集气瓶中的水:水先将集气瓶内的空气排尽,后便于观察O2何时收集满 |
A . A
B . B
C . C
D . D
下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是( )
A .  B .
B .  C .
C .  D .
D . 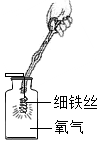
 B .
B .  C .
C .  D .
D . 
如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.

| 内容步骤 | [实验1]研究燃烧条件 | [实验2]研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
-
(1) H2O2稀溶液与MnO2接触时发生反应的化学方程式为
-
(2) 实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是;;推入H2O2溶液后,观察到烧杯中的现象是
-
(3) 实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,该实验中,集气瓶内压强的变化过程是.
小明设计如图所示的实验装置来同时完成燃烧条件的探究和空气中氧气含量的测定。装置中注射器活塞与内壁摩擦非常小,可忽略不计。
查阅资料发现:
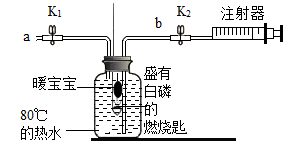
①当容器内的氧气浓度低于一定值时,白磷无法继续与氧气反应。
②“暖宝宝”能耗尽容器中少量的氧气。
实验操作步骤如下:
步骤1:检查装置气密性。
步骤2:将盛有足量白磷的燃烧匙放入空集气瓶中,
塞紧塞子,白磷不燃烧。
步骤3:打开集气瓶塞子,往瓶中倒满80℃的热水,并塞紧塞子,白磷仍然不能燃烧。
步骤4:打开K1和K2 , 通过注射器从b管抽水,当注射器中水量达到V1毫升时,瓶中液面低于燃烧匙底部,此时立即关闭K1、K2 , 发现瓶中白磷燃烧。
步骤5:待整个装置冷却至室温时,打开K2 , 发现注射器中的水剩余V2毫升。
-
(1) 结合步骤3、4,说明白磷燃烧需要的条件是。
-
(2) 该实验测得空气中氧气的含量为。(用V1、V2来表示)
-
(3) 小明多次重复上述实验,测得空气中氧气的体积分数远大于21%,原因是。
将适当物质的名称填写在空格中。
-
(1) 为证明某物质燃烧后有二氧化碳产生,可将产物通入。
-
(2) 为证明生石灰跟水反应生成可溶性碱,可向生成物中滴入无色,如果呈红色,就证明生成了碱。
-
(3) 将氧气和二氧化硫的混合气体通过盛有氢氧化钠固体的玻璃管中,若发生反应的物质能完全反应,最后剩余的气体主要是。
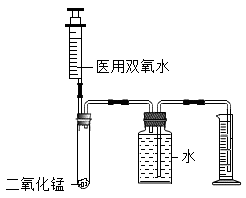
家庭医药箱里有一瓶标签缺损的医用双氧水,为测定其溶质质量分数,小宁设计了如图实验:在试管中放入一定量的二氧化锰,然后用注射器注入10mL该医用双氧水,直到试管中不再有气泡产生,通过测量量筒中水的体积就可以大致计算出双氧水质量分数。
-
(1) 实验中用排水法测量氧气的体积是因为氧气具有的性质。
-
(2) 若俯视读得量筒中水的体积,则测得的双氧水质量分数将。(填“偏大”“偏小”或“不变")。
最近更新






