离子方程式的有关计算 知识点题库

B .
B . 
C .
C . 
D .
D . 
常温下在20mL0.1mol/L碳酸钠溶液中逐滴加入0.1mol/L盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的百分含量也发生变化(二氧化碳因为逸出未画出).据此回答下列问题:

-
(1) 用离子方程式表示碳酸钠溶液呈碱性的原因:
-
(2) 当加入盐酸使溶液pH为10时,混合液中含碳元素的离子的物质的量之比为
-
(3) 用等式表示碳酸钠溶液中所有离子浓度之间的关系:
-
(4) 请写出OAB段的离子方程式:
-
(5) 当混合溶液的pH= 时,开始放出二氧化碳气体

 当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系
B . 当a=b时,所得溶液中存在:c(OH﹣)+c(CO32﹣)=c(H+)+c(H2CO3)
C . 当2a=b时,所得溶液中存在:c(Na+)>c(CO32﹣)>c(OH﹣)>c(HCO3﹣)>c(H+)
D . 当
当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系
B . 当a=b时,所得溶液中存在:c(OH﹣)+c(CO32﹣)=c(H+)+c(H2CO3)
C . 当2a=b时,所得溶液中存在:c(Na+)>c(CO32﹣)>c(OH﹣)>c(HCO3﹣)>c(H+)
D . 当  <a/b<1时,所得溶液中一定存在:c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
<a/b<1时,所得溶液中一定存在:c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)


注:SS表示固体悬浮物
模拟工业处理流程如下:

已知:i.常温时CaSO4微溶于水; ii.溶解度: CaSO4>Fe(OH)2>FeS。
-
(1) ①采用20%的硫酸对废水进行预中和处理,pH变化如下图所示。硫酸的用量和废水中固体悬浮物(SS)含量的关系是。

②废水中SS含量随时间变化如下表所示。
静置时间(h)
1
2
3
4
5
6
24
SS含量(mg/L)
2500
1800
1300
900
820
800
780
为降低成本,减少硫酸投加量的最好办法是。
③滤渣A的主要成分有SS和。
-
(2) 根据表中数据,回答下列问题。

①化学絮凝沉淀过程中,加入FeSO4发生反应的离子方程式是。
②熟石灰能促进沉淀的生成,结合离子方程式,从平衡角度分析其原因是。
-
(3) 用臭氧进一步处理废水中的氰化物和残留硫化物,若将500mL废水中的CN-完全氧化成N2和CO2 , 转移mol e-。
 、
、  、
、  、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中()
、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中()
 、
、  一定存在,Cl-可能不存在
D .
一定存在,Cl-可能不存在
D .  、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在

 mol
D .
mol
D .  mol
mol
|
阳离子 |
Na+ H+ Ba2+ |
|
阴离子 |
OH- CO32- SO42- |
为鉴别它们,分别完成一些实验。请根据实验的结果回答下列问题:
-
(1) A溶液与B溶液反应可生成气体X。根据上述六种离子之间的可能反应判断X的化学式为,A溶液与B溶液反应的离子方程式为。
-
(2) 气体X可以和C溶液反应生成沉淀D,沉淀D可与B溶液反应。则C的化学式为,B溶于水后的电离方程式为 。
-
(3) B溶液与C溶液反应生成不溶于稀硝酸的白色沉淀E。B溶液与C溶液反应至中性的离子方程式为。
-
(4) D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为bL,则求算E在混合物中的质量分数的表达式为。
-
(1) 取该碱式盐 3.40 g,研磨、加水、搅拌使之充分分散,滴加 2.00 mol·L-1 盐酸,先后与 OH-和CO32-反应,当加入盐酸 35.0 mL 时,开始产生 CO ,加入盐酸 45.0 mL 时恰好完全反应,该碱式盐中氢氧根与碳酸根的物质的量之比为。
-
(2) 在上述反应后所得溶液中加入过量氢氧化钠溶液,过滤、洗涤、干燥后沉淀物重 1.74 g,该碱式盐中铝离子与镁离子的物质的量之比为。
-
(3) 若 3.40 g 该碱式盐完全受热分解产生 0.81 g 水,该碱式盐的化学式为。
 的物质的量为( )
的物质的量为( )
-
(1) 一、 H2O2是医药、卫生行业上广泛使用的消毒剂。某课外小组采用滴定法测定某医用消毒剂中H2O2的浓度。实验步骤如下:
①标准液的配制和标定:称取一定量KMnO4固体溶于水,避光放置6至10 天,过滤并取滤液于滴定管中待用,称取mgNa2C2O4固体于锥形瓶中,加水溶解,再加H2SO4酸化,滴定至终点,消耗KMnO4溶液的体积V1ml,滴定过程中发生的一个反应为:5H2C2O4+2MnO
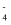 +6H+=2Mn2++10CO2↑+8H2O。(草酸不稳定,易分解)
+6H+=2Mn2++10CO2↑+8H2O。(草酸不稳定,易分解)②H2O2浓度的测定:取待测样品25mL稀释至500mL,再移取10.00mL于锥形瓶中,加H2SO4酸化,用上述KMnO4标准液滴定至终点,消耗溶液的体积V2mL。
回答下列问题:
①中移取酸性高锰酸钾溶液滴定时所用主要仪器名称为
-
(2) 标定KMnO4标准液时需要控制温度为75至85℃,温度过低反应较慢,温度过高可能会因为 导致KMnO4标准液的标定浓度偏高,在恒定温度下进行滴定操作时,开始时反应速率较慢,随后加快,导致速率加快的原因是
-
(3) KMnO4标准液滴定H2O2的离子方程式为 ,当滴定到 可以认为已达到滴定终点。
-
(4) 该医用消毒剂中H2O2的物质的量浓度为mol·L-1。
-
(5) 二、KMnO4是一种典型的强氧化剂。用酸性KMnO4溶液处理残留的Cu2S时,反应如下:KMnO4+Cu2S+H2SO4→ K2SO4+MnSO4+CuSO4+SO2↑+H2O
关于该反应的下列说法中错误的是
A 被氧化的元素是S
B KMnO4是氧化剂,Cu2S既是氧化剂又是还原剂
C 氧化剂与还原剂的物质的量之比为8:5
D 生成2.24L(标准状况)的SO2 , 转移电子的物质的量是0.8mol
E 氧化性的强弱关系是 MnO
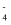 >Mn2+>Cu2+
>Mn2+>Cu2+

-
(1) 步骤Ⅰ、步骤Ⅲ发生反应的离子反应方程式为、。
-
(2) 步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是。
-
(3) 步骤Ⅱ通入热空气或水蒸气吹出Br2 , 利用了溴的。(填性质)
-
(4) 步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:。
 Br2+
Br2+ CO
CO =
= BrO
BrO +
+ Br-+
Br-+ CO2↑
CO2↑ -
(5) 步骤Ⅱ中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。若从1000L海水中提取溴,理论上需要SO2的质量为。



