饱和溶液与不饱和溶液 知识点题库
工业上,通过如下转化可制得KClO3晶体:NaCl溶液 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体

-
(1)
完成Ⅰ中反应的化学方程式:NaCl+3H2O
 NaClO3+3 ↑ .
NaClO3+3 ↑ . -
(2) Ⅱ中析出晶体后的母液是KClO3的 (填“饱和”或“不饱和”)溶液,写出母液中的所有溶质的化学式 .
-
(3) 用如图装置(夹持、加热装置已略)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是 .
选项
①中实验
②中现象
A
加热氯化钾和二氧化锰的混合物
伸入试管内的带火星木条复燃
B
加热碱式碳酸铜固体
澄清石灰水变浑浊
C
加热铜丝
伸入水中导管口有气泡冒出
D
加热氯化铵和熟石灰的混合物
酚酞溶液变红
A、B、C三个烧杯中盛有相同质量的水(其中A、C烧杯中水温为10℃,B烧杯中水温为30℃,不考虑溶解过程中温度的变化),分别加入甲、乙两物质各10g,充分溶解后现象如图所示,试回答: 

-
(1) 你认为烧杯中的溶液可能是不饱和溶液.
-
(2) 如图是甲、乙两种物质的溶解度曲线图,据图分析,10℃时A烧杯和C烧杯中未溶解的溶质质量关系是(填“相等”或“不想等”).其他条件不变,将C烧杯中的温度升到30℃时,C烧杯中的溶液是(填“饱和”或“不饱和”)溶液.
关于溶液下列说法正确的是( )
A . 饱和溶液一定是浓溶液
B . t℃时,100克某物质的饱和溶液中含该溶质18克,则该物质在t℃时溶解度是18克
C . 饱和溶液指一定温度下一定量溶剂中不能继续溶解某种溶质的溶液
D . 不饱和溶液加溶剂可以变为饱和溶液
氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
① | 10 | 2 | 12 |
② | 10 | 3 | 13 |
③ | 10 | 4 | 13.6 |
④ | 10 | 5 | m |
-
(1) 表中m=;
-
(2) 在这4次实验中,得到的是20℃氯化钠溶液属于饱和溶液的是(填实验序号)
-
(3) 计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
-
(4) 20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
如图所示,在室温下的饱和食盐水中放了一个塑料小球。

-
(1) 现加入少量食盐晶体,充分搅拌和静置后,在温度不变的情况下,试分析小球在液面处的沉浮情况有何变化,并简述原因。
-
(2) 若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是:
①;
②;
③。
如图是某同学在厨房里看到的食用纯碱(主要成分是 Na2CO3)包装袋信息,他带了一包食用纯碱到学校实验室。

-
(1) 为测定室温下 Na2CO3 的溶液溶解度,在编号为 A、B、C、D的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的 Na2CO3 固体,搅拌至充分溶解,实验数据记录如下表:
烧杯编号
A
B
C
D
水的质量/克
100
100
100
100
加入 Na2CO3 的质量/克
30
35
40
50
溶液的质量/克
130
135
140
140
分析上述数据,烧杯编号为中的溶液是饱和溶液。室温下,Na2CO3 的溶解度是。
-
(2) 为确定食用纯碱的纯度,称取自带的食用纯碱 5.4g 放入烧杯中,再滴加盐酸至刚好完全反应,共用去稀盐酸 25g,得溶液质量为 28.2g(杂质溶于水且与盐酸不反应)。通过计算判断该食用纯碱中碳酸钠的质量分数是否与包装袋信息相符。(计算结果精确到 0.1%)
某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。

-
(1) 能判断原硫酸铜溶液已饱和的方法是 。A . 观察颜色,溶液蓝色较深 B . 溶液冷却,有蓝色晶体析出 C . 蒸发少量水,有蓝色晶体析出 D . 加入硫酸铜晶体,晶体质量不变
-
(2) 现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。
如表是氯化钠(NaCl)和硝酸钾(KNO3)在不同温度时的溶解度,回答问题。 

-
(1) 两种物质中,溶解度受温度影响变化较大的是。
-
(2) 60℃时,按图示操作:

A中溶液是 (填“饱和”或“不饱和”)溶液,C中溶液的总质量是克。
-
(3) 50℃时,将两种物质的饱和溶液各100克,分别加热蒸发10克水后,再恢复到50℃,剩余溶液的质量:NaCl溶液(填“大于”“等于”或“小于”)KNO3溶液。
放学后,感觉有点饿的小新用开水泡了一杯白糖水,他用筷子充分搅拌杯中的白糖后,将杯子放在一边待糖水变凉。喝糖水时,发现杯底有少量未溶解的白糖(如图所示)。下列操作或现象能说明糖水一定属于饱和溶液的是( )

A . 喝糖水时感觉很甜
B . 泡糖水时进行了充分搅拌
C . 热的糖水中白糖全部溶解
D . 凉的糖水底部有剩余的白糖
无土栽培技术是植物根能直接接触培养液的栽培方法,小明在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图A,一段时间后变成了图C。下列说法不正确的是( )

A . 硝酸钾的溶解度随温度的升高而增大
B . 图C中的培养液一定是不饱和溶液
C . 图A中的培养液一定是饱和溶液
D . 可以通过升温把硝酸钾的饱和溶液转变为不饱和溶液
向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )

|
A的溶解度 |
温度(℃) |
20 |
30 |
40 |
50 |
60 |
|
溶解度(g) |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
A . ②中A的质量分数最大
B . ③⑤中A的质量分数相等
C . ②④⑤的溶液为饱和溶液
D . ①③④⑤中没有固体存在
在一定温度下,向100克水中依次加入一定质量的氯化钾(KCl)固体,充分溶解。加入氯化钾的质量与得到相应溶液质量的关系如图所示,下列说法正确的是( )

A . 该温度下氯化钾的溶解度是60克
B . 实验②所得溶液中溶质的质量分数为40%
C . 实验①、②、③的溶液都是饱和溶液
D . 实验②和实验③所得溶液的质量分数相同
一杯50℃的氯化钠溶液发生如图所示的变化,不计乙溶液变成丙溶液过程中水分的蒸发,则下列有关叙述正确的是( )

A . 甲溶液可能是50℃时的氯化钠饱和溶液
B . 乙溶液一定是50℃时的氯化钠饱和溶液
C . 乙溶液的溶质质量分数最高
D . 丙溶液的溶质质量分数最高
在20℃时,100克5%的食盐溶液温度升高到60℃(忽略水分蒸发),则溶质的质量分数为 ;若将该溶液恒温蒸发水分,则溶液中溶质的质量分数会(选填“增大”或“减小”) ;在20℃时,当溶液成为时,该溶液的质量分数最大,其最大值为。(20℃时,食盐的溶解度为36克)
20℃时,向3个盛有50克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据回答。
|
烧杯编号 |
A |
B |
C |
|
加入氯化钠的质量(克) |
9 |
18 |
27 |
|
溶液质量(克) |
59 |
68 |
68 |
-
(1) 实验所得3杯溶液中,属于不饱和溶液的是(填编号)。
-
(2) 若将A杯中的溶液稀释成溶质质量分数为0.9%的生理盐水,需加水克。
20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分溶解,实验过程如图所示。下列分析正确的是( )

A . 甲烧杯中,硝酸钾溶液是不饱和溶液
B . 丁烧杯中,硝酸钾溶液是不饱和溶液
C . 乙一丙过程中,硝酸钾溶液的溶质质量分数变大
D . 丙丁过程中,硝酸钾溶液的溶质质量分数变大
向甲物质中逐渐加入乙物质至过量。若x轴表示加入乙物质的质量,则下列选项与下图不相符合的是( )

A . 如果甲是二氧化锰,乙是过氧化氢溶液,则y轴表示二氧化锰的质量
B . 如果甲是某一温度下的水,乙是硝酸钟,则y轴表示硝酸钾的溶解度
C . 如果甲是氯化银,乙是稀硝酸则y轴表示氯化银的质量
D . 如果甲是饱和石庆乐,乙是生石灰,则y轴表示溶液的质量
科学中部分概念在逻辑上存在并列、交叉和包含关系,可用如图表示这三种关系。下列说法错误的是( )

A . 合金和金属材料属于包含关系
B . 化合物和有机物属于包含关系
C . 饱和溶液和不饱和溶液属于交叉关系
D . 物理变化和化学变化属于并列关系
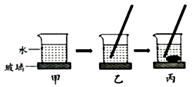
如图所示,把装有适量水的烧杯放在湿玻璃上,向烧杯中两次加入硝酸铵固体充分搅拌,发现玻璃上的水结冰使烧杯和玻璃粘在一起。
-
(1) 烧杯里的硝酸铵溶液一定是饱和溶液的是图。
-
(2) 该过程中玻璃上水发生物态变化的名称是。
下列关于结晶和晶体的说法错误的是( )
A . 饱和溶液降温析出晶体后的溶液还是饱和溶液
B . 降低饱和溶液的温度不一定有晶体析出
C . 从溶液中析出的晶体中不一定含有结晶水
D . 将溶液的溶剂蒸发掉一些一定会析出晶体
最近更新



