饱和溶液与不饱和溶液 知识点题库
下列曲线能正确表达对应的反应或过程的是( )
A . 向一定量的水中加入生石灰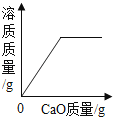 B . 红磷在装有空气的密闭容器中燃烧
B . 红磷在装有空气的密闭容器中燃烧 C . 向一定质量的烧碱溶液中滴入盐酸
C . 向一定质量的烧碱溶液中滴入盐酸 D . 向饱和KNO3溶液中加入KMnO4固体
D . 向饱和KNO3溶液中加入KMnO4固体
 B . 红磷在装有空气的密闭容器中燃烧
B . 红磷在装有空气的密闭容器中燃烧 C . 向一定质量的烧碱溶液中滴入盐酸
C . 向一定质量的烧碱溶液中滴入盐酸 D . 向饱和KNO3溶液中加入KMnO4固体
D . 向饱和KNO3溶液中加入KMnO4固体
20℃时,在三个各盛有100g水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各10g,充分溶解后,情况如下表所示,有关说法不正确的是( )
物 质 | 甲 | 乙 | 丙 |
未溶解固体的质量/g | 7 | 0 | 3 |
A . 升高温度,三溶液中溶质的质量分数一定会改变
B . 三溶液中溶质的质量分数乙>丙>甲
C . 所得溶液可能都是饱和溶液
D . 20℃时,甲的溶解能力最小
20℃时,分别盛有10克水的两支试中,等质量的甲乙两种固体物质,是其充分溶解,可观察到如图1所示现象.

-
(1) 20℃时,(A或B)试管中的溶液一定是饱和溶液.
-
(2) 图2中表示甲物质的溶解度曲线的是,(填a或b),要是A试管中剩余的固体继续溶解,可采用的方法是

-
(3) P点的含义.
在一定温度下,向 100g 水中依次加入一定质量的 KCl 固体,充分溶解。加入 KCl 的质量与得到相应溶液质量的关系如图所示。
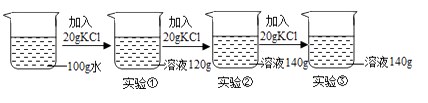
-
(1) 实验③所得溶液的质量分数是。3 次实验所得溶液质量分数由小到大的关系 是。
-
(2) 实验②的溶液是否为饱和溶液?(填“是”“不是”或者“无法判断”)。
在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:
![]()
则下列结论正确的是( )
A . 溶液甲可能是饱和溶液
B . 溶液乙和溶液丙中的溶质质量分数相等
C . 溶液乙一定是不饱和溶液
D . 溶液丙若再蒸发5克水,析出的晶体可能大于2克
图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关系符合图3所示关系是( )

|
X |
Y |
Z |
|
|
A |
结晶 |
蒸馏 |
沉淀 |
|
B |
悬浊液 |
乳浊液 |
溶液 |
|
C |
溶质 |
溶剂 |
溶液 |
|
D |
饱和溶液 |
不饱和溶液 |
浓溶液 |
A . A
B . B
C . C
D . D
下表是氯化钠(NaCl)和硝酸钾(KNO3)在不同温度时的溶解度,回答问题
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |

-
(1) 60℃时,按图示操作A中溶液是(填“饱和”或“不饱和”)溶液,C中溶液的总质量是。
-
(2) 50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃剩余溶液的质量:氯化钠溶液(填“大于”、“等于”或“小于”)硝酸钾溶液.
如图是a、b两种固体物质的溶解度曲线,据图可以得到的正确信息是( )

A . a的溶解度大于b的溶解度
B . b物质宜用冷却热饱和溶液的方法获取晶体
C . t1℃时,a、b两种物质的饱和溶液中,溶质的质量分数相等
D . t2℃时,100克水中最多能溶解的物质,b比a多
我国西北地区有一些天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。

-
(1) “夏天晒盐”中的“盐”其溶解度可用图中来表示(填“a”、或“b”、或“c”)。
-
(2) 在t1℃时,三种物质的溶解度大小关系是。
-
(3) 在t2℃时,将40g的a放入50g水中充分搅拌,所得溶液质量为g。
-
(4) 将t2℃时a,b,c的饱和溶液降温至t1℃时,溶质的质量分数由大到小的顺序为 。
一定温度下,向图I烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )

A . 所得溶液是饱和溶液
B . 溶质的质量增加
C . 溶质的质量分数变大
D . 溶质的溶解度变大
同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.木糖醇和蔗糖的溶解度曲线如图,据图回答:
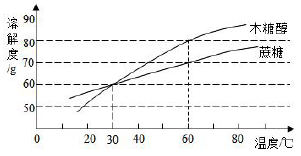
-
(1) 10℃时,木糖醇的溶解度蔗糖的溶解度。(选填“大于”、“小于”或“等于”)
-
(2) 60℃时,向100克水中加入100克木糖醇,充分溶解后,所得的溶液是溶液(选填“饱和”或“不饱和”),该溶液的溶质质量分数为。要得到木糖醇的晶体可用的蒸发溶剂的方法,还可用。
推理判断是科学学习的重要方法。针对下列三种以水为材料的实验,请做出合理的推理:
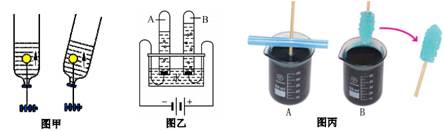
-
(1) 图甲:切除矿泉水瓶的底部,粘着乒乓球的-根线穿过带小孔的瓶盖,系上一颗较轻的螺丝。加水后发现乒乓球慢慢上浮如图所示,此实验说明浮力的方向是的。
-
(2) 图乙:水的电解实验中,发现A试管产生气体体积是B试管的两倍,由此推测A试管中的气体是 气。
-
(3) 图丙:将竹签置于热的糖水溶液(A杯)中过夜,第二天早上发现烧杯(B杯)中出现了神奇的“棒棒糖”,则一定是饱和溶液的是杯。(选填字母 “A”或“B”)
向100克水中不断加入固体A或改变温度,该过程如图所示,得到相应的溶液①~~~⑤
![]()
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/克 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
-
(1) 这五种溶液中,溶质质量分数最大的是(填序号,下同)。
-
(2) 这五种溶液中,属于饱和溶液为。
在一定温度下,在一定量的溶剂里不能继续溶解某种溶质的溶液,称为在该温度下这种溶质的溶液。
如图是对20℃一定质量的甲溶液进行恒温蒸发的结晶实验过程,请回答:
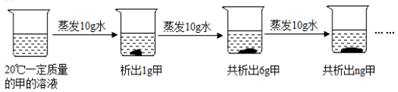
-
(1) 蒸发前原溶液是(填“饱和”或“不饱和”)溶液,n的值是。
-
(2) 依据上述实验,你认为甲的溶解度随温度变化的趋势是(填字母)
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
在室温下,小乐完成了如下实验,若固体 A(不含结晶水)溶于水既不吸热,也不放热,且实验过程中。不考虑水的蒸发。则下列说法正确的是( )

A . 在室温下,溶液①为饱和溶液
B . 在 t℃时,A 的溶解度可能为 50 克
C . 溶液③和溶液④的溶液质量相同
D . 溶液②和溶液④的溶质质量分数不相同
一定温度下,向盛有100g蔗糖溶液的烧杯中再加入10g蔗糖,充分搅拌后,一定保持不变的是( )
A . 溶质的质量
B . 溶液的质量
C . 溶质的质量分数
D . 蔗糖的溶解度
下列关于溶液说法正确的是( )
A . 某温度下两种不同物质的溶液,溶质质量分数相同,则这两种物质的溶解度一定相同
B . 在一定温度下,同一种溶质其饱和溶液的溶质质量分数比不饱和溶液的大
C . 溶液是无色透明的,无色透明的液体不一定都是溶液
D . 浓溶液是饱和溶液,饱和溶液不一定是浓溶液
已知:
⑴20℃时,溶解度在10克以上的物质称为易溶物质;溶解度在1~10克的物质为可溶物质;溶解度在0.01~1克为微溶物质;溶解度小于0.01克的物质为难溶物质。
⑵20℃时几种物质的溶解度如下:
|
物质名称 |
氯化钠 |
氢氧化钙 |
氯酸钾 |
硝酸钾 |
|
溶解度(克) |
36.0 |
0.165 |
7.4 |
31.6 |
下列说法正确的是( )
A . 20℃时氢氧化钙是难溶物质
B . 20℃时可以配制出20%的硝酸钾溶液
C . 20℃时氯酸钾是易溶物质
D . 20℃时硝酸钾的溶解度比氯化钠大
有一瓶敞口放置的氢氧化钠固体,为判断是否变质,进行了以下操作。
-
(1) 向装有少量该固体的试管中加过量稀盐酸,如果现象为,可知氢氧化钠变质;
-
(2) 为进一步确定其变质程度,另取16g样品配成溶液,配制过程如下。烧杯A,B,C中的溶液一定为饱和溶液的是;
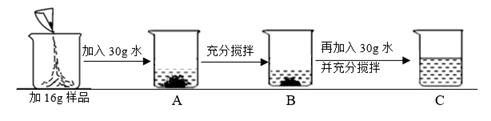
-
(3) 向(2)中的C烧杯逐滴加入10% 氯化钙溶液,产生沉淀的质量与氯化钙溶液的质量关系如图所示,计算16克样品中碳酸钠的质量。


最近更新



