一定溶质质量分数的溶液的配制 知识点题库
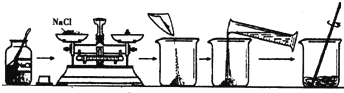
某实验小组探究选稻种的实验,需配制质量分数为10%的氯化钠溶液105g,实验操作步骤如图所示:
-
(1) 计算应称取氯化钠g,需加水mL(把水的密度近似看作lg/cm3).
-
(2) 如果配制的氯化钠溶液溶质质量分数小于10%,则造成误差的原因可能有?(请举两条)
①,②.
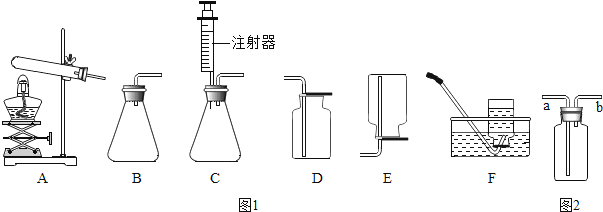
如图是实验室常用气体制备装置,据图回答问题:
-
(1) 实验室用高锰酸钾制氧气的化学方程式是 ,应选择的收集装置是 (填字母代号),如果选用如图2装置收集氧气,气体应从 (填“a”或“b”)端导入.
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为 .某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气.实验中,同学们发现不能得到平稳的氧气流.大家提出从两个方面加以改进:
一是把发生装置由B改为C,其理由是 ;
二是将过氧化氢溶液加水稀释,溶液的稀释须要经过计算,量取,搅匀三个步骤.
如果把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,需加水的质量为 g;在稀释过程中,除了烧杯外,还需要用到的仪器有 (填数字序号).
①量筒 ②药匙 ③试管 ④酒精灯 ⑤滴管 ⑥玻璃棒.
-
(1) 配制溶液需完成计算,称量和三个步骤.
-
(2) 下列几种情况会造成配制溶液溶质质量分数出现偏差:
①硝酸钾中含杂志,则配制溶液中溶质质量分数 10%(选填“>”“=”或“<”,下同)
②称量时使用生锈的砝码,则配制溶液中溶质质量分数 10%.
③称量时KNO3和砝码的位置颠倒,则配制溶液中溶质质量分数 10%
④用量筒量取水时,俯视读数,则配制溶液中溶质质量分数 10%
⑤配制完成后称取液体时有部分溅出,则配制溶液中溶质质量分数 10%
-
(3) 配制该溶液必须用到的玻璃仪器有:、和.
-
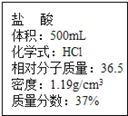
(1) 这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
-
(2) 取100克此瓶内的浓盐酸可以稀释成18.5%的稀盐酸多少克?同时加水多少克?
-
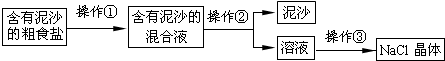
(1) 操作②中玻璃棒的作用是。
-
(2) 用上述实验所得的氯化钠晶体和蒸馏水配制5%NaCl溶液50.0g,配制时需要用到的玻璃仪器有量筒、胶头滴管、
|
实验序号 |
① |
② |
③ |
④ |
|
加入氯化钠的质量/g |
9 |
36 |
81 |
90 |
|
溶液质量/g |
209 |
236 |
272 |
272 |
-
(1) 若将①中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是g。
-
(2) 关于上述实验的叙述正确的是 (填序号)。A . ①②所得溶液是不饱和溶液 B . ③④所得溶液中,溶质的质量分数相等 C . 20℃时,将④继续恒温蒸发100g水,过滤,得到质量为36g的固体 D . 20℃时,200g水中最多溶解氯化钠的质量为72g
|
实验序号 |
水的质量(g) |
加入氯化钠的质量(g) |
溶液的质量(g) |
|
① |
10 |
2 |
12 |
|
② |
10 |
3 |
13 |
|
③ |
10 |
4 |
13.6 |
|
④ |
10 |
5 |
m |
-
(1) 表中m=;
-
(2) 计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
-
(3) 20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
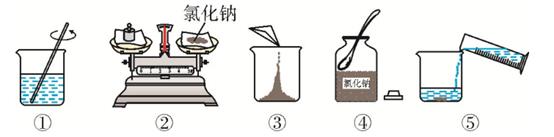
-
(1) 现欲配制一瓶 75 g 溶质质量分数为 10%的氯化钠溶液,需氯化钠的质量为g。
-
(2) 请用图中的序号表示配制溶液的正确操作顺序:。
-
(3) 图中某步骤错误,该步骤的正确操作为。
-
(4) 下列情况中,可能会使氯化钠溶液质量分数低于10%的是。
A.称取的氯化钠不纯,有杂质 B.在量取水时,俯视液面读数
C.配制好的溶液转移时,不小心有少量液体溅出
D.配制好的溶液装入刚用蒸馏水润洗过的试剂瓶保存
E.氯化钠固体潮湿 F.称量时砝码端忘垫质量相同的纸片
G.量取水时,仰视读数 H.装瓶时,有少量溶液洒出 I.左码右物
-
(5) 实验室用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,则需要15%的氯化钠溶液g,向其中加入g水可配得 120 克 5%的氯化钠溶液。
-
(1) 现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金 (填写代号)
-
(2) 取与上述用稀盐酸鉴别出的同种合金 10g,放入烧杯中,再向其中加入 93.7g 某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为 103.5g.
①上述过程中产生氢气的质量是 ;
②10g 该合金中铜的质量,已知反应后溶液中溶质全部溶解,求该溶液中溶质的质量分数为;
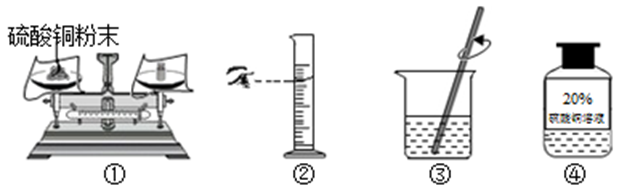
-
(1) ①称量硫酸铜粉末时,若发现天平指针偏左,应,直至指针指向分度盘中央刻度线。
-
(2) ②量取所需水时,选择的量筒的量程是(选填“20”“50”或“100”)ml。
-
(3) 通过③溶解和④装瓶后,得到了一瓶20%的硫酸铜溶液,若测得此硫酸铜溶液的密度为1.16g/cm3。取出50mL此硫酸铜溶液,可稀释得到8%的硫酸铜溶液g。
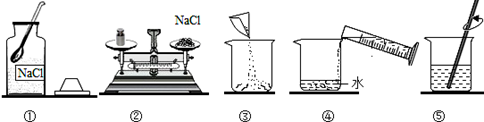
请回答下列问题:
-
(1) 按图中操作,会导致溶液的溶质质量分数 (选填“偏大”、“偏小”或“无影响”)。
-
(2) 20℃时,某同学将配置的 100g10%的氯化钠(NaCl)溶液,第一次恒温蒸发65g水,析出1g,再恒温蒸发5g水,又析出晶体1.8g, 该温度下氯化钠的溶解度是g。
-
(3) 实验室现有5%的氯化钠溶液、20%的氯化钠溶液、水、氯化钠固体,请选择其中两种试剂混合,配制10%的氯化钠溶液,所需试剂质量的最简整数比。
例如:选择水和氯化钠固体,质量比9:1混合。请再写出一种合理方案。
方案:。

| 选项 | 操作 | 目的 |
| A | 用剩的食盐放回原试剂瓶 | 避免浪费 |
| B | 天平调平后在左、右托盘中各垫一张相同的纸 | 保证称取的食盐质量更准确 |
| C | 溶解时用玻璃棒搅拌 | 增加食盐的溶解能力 |
| D | 用50ml量筒替代天平量取所需的水 | 更加简便 |
 B . 配制质量分数为15%的食盐水
B . 配制质量分数为15%的食盐水 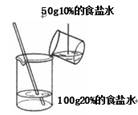 C . 压入空气使烧瓶内刚停止沸腾的水重新沸腾
C . 压入空气使烧瓶内刚停止沸腾的水重新沸腾 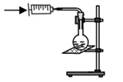 D . 往漏斗里吹气使乒乓球不下落
D . 往漏斗里吹气使乒乓球不下落 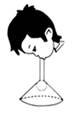
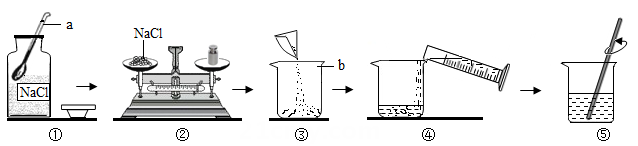
-
(1) 图示实验操作中有一处明显错误的是 。(填序号)
-
(2) 小科应选取规格为的量筒(填10mL、50mL或100mL),若他在量取水的体积时,俯视读数,则所配制溶液中氯化钠的质量分数(选填 “偏大”、“偏小”或“不变”)。

-
(1) 配制50g质量分数为6%的氯化钠溶液,配制溶液的步骤:计算、称量和量取、、装瓶、贴标签。
该同学的操作如下,其中有错误的是。
①计算需称取氯化钠固体3.0g;
②称量前托盘天平应先检查游码是否归零,并调节平衡;
③用托盘天平称量氯化钠固体时,为防止污染托盘,可将氯化钠放在玻璃皿上称量;
④选用250mL量筒量取47mL的水;
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存。
-
(2) 粗盐中难溶性杂质的去除。步骤如下:
①取一定质量的粗盐样品,加水溶解;②过滤;③蒸发结晶;④称量、计算产率。
在上述各步实验中,都用到玻璃棒,它在步骤③中的作用是。



