过滤的原理、方法及其应用 知识点题库
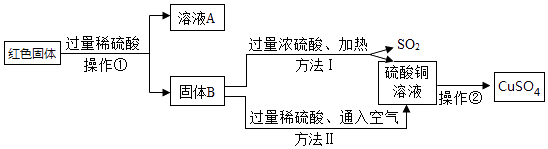
回收利用废金属是解决废金属造成资源浪费和不同程度的环境污染的方法之一.某市一家大型化工厂处理回收含铜废料的生产流程与部分操作如下:
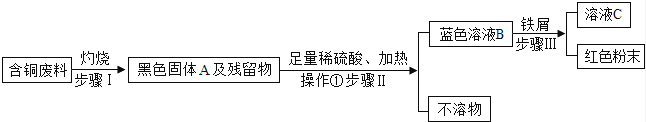
(注:步骤Ⅰ得到的残留物不溶于水和稀硫酸)
请回答下列问题:
(1)黑色固体A的成分是 (用化学式表示).
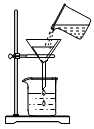
(2)流程图中操作①的名称是 .
(3)写出步骤Ⅲ的一个反应的化学方程式 .
(4)通常在步骤Ⅲ必须加入略过量的“铁屑”,原因是 .
 称量固体
B .
称量固体
B .  取用块状固体
C .
取用块状固体
C .  过滤
D .
过滤
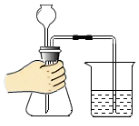
D .  检查装置气密性
检查装置气密性
【查阅资料】Cu+Fe2(SO4)3=2FeSO4+CuSO4 .
-
(1) 操作①所需要用到的玻璃仪器有:烧杯、漏斗、.
-
(2) 溶液A的溶质有.
-
(3) 两种方法比较,符合绿色化学要求的是方法;方法Ⅱ的化学反应方程式为:2Cu+2H2SO4+═2CuSO4+.
-
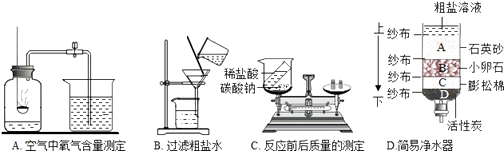
(1) A中所用物质是红磷,写出相关的化学方程式为.
-
(2) B中玻璃棒的作用是.
-
(3) C中发生的反应是:稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,写出相关的化学方程式.反应后天平不平衡,该反应(填“遵循”或“不遵循”)质量守恒定律.
-
(4) 粗盐中含泥沙、氯化钙、氯化镁等杂质,某同学自制的简易净水器D中放置物质的顺序错误,使净水效果不理想.请按由上到下的顺序重新排列(填字母).
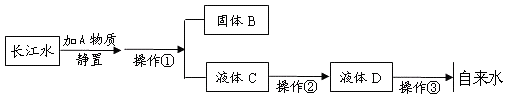
请回答以下问题:
-
(1) 操作①的名称是;该操作中用到的玻璃仪器有玻璃棒、漏斗和,其中玻璃棒的作用是。
-
(2) 操作②主要是用活性炭除去一些异味和色素,其净水原理是利用活性炭的作用,该过程主要是变化(填“物理”或“化学”)。
-
(1) Ⅰ.在农业生产上,常需要用质量分数为16%的氯化钠溶液选种。某同学配制100g质量分数为16%的氯化钠溶液,需要氯化钠的质量为 g;水的体积为 mL(水的密度近似看作1g/cm3)。
-
(2) Ⅱ.海水中提取氯化钠。利用风吹日晒可以从海水中提取粗盐,粗盐中一般含有少量泥沙等杂质。以下是制备纯净氯化钠的实验流程,请据图回答问题。
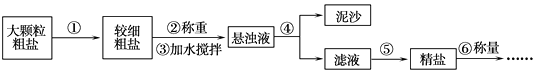
①操作⑤中用到的仪器有铁架台、玻璃棒、酒精灯、坩埚钳、。其中玻璃棒的作用是。
②实验结束后称量获得的精盐,并计算精盐的产率,发现产率偏低,其可能的原因是(填序号)。
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.过滤时滤纸有破损
③如图是甲、乙两种固体物质的溶解度曲线。
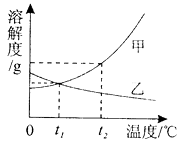
①℃时,甲、乙两种物质的溶解度相等。
②t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲乙(填“>”、“<”或“=”)。
-
(3) Ⅲ. 家庭制备氯化钠: 将洁厕灵(含有盐酸)与炉具清洁剂(含有氢氧化钠)混合,如下图甲所示。
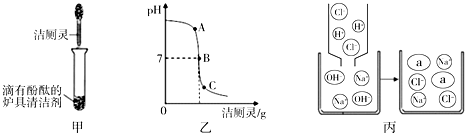
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外),此时溶液可用图乙中(选填A、B、C)点处表示。
②若反应后溶液pH为7,图丙中a微粒的化学式为。
 C .
C .  D .
D . 
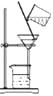 B . 稀释浓硫酸
B . 稀释浓硫酸 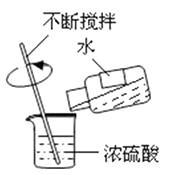 C . 配制溶液
C . 配制溶液 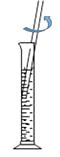 D . 测试某溶液的酸碱度
D . 测试某溶液的酸碱度 
-
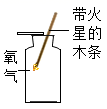
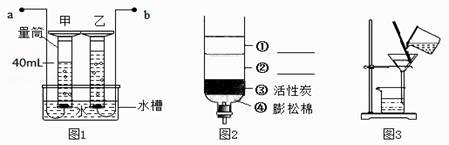
(1) 图1是用100mL的量筒等仪器组装成的电解水的简易装置,从图中可以看出,a连接电源的极,(填“甲”或“乙”)量筒内产生的气体能使带火星木条复燃,乙量筒内气体的体积约为ml,该实验的结论是;水是由组成的。从能量转化角度分析,电解水将能转化为能。
-
(2) 下列各种水中,属于纯净物的是____(填字母)。A . 汽水 B . 矿泉水 C . 蒸馏水 D . 经过净化处理的自来水
-
(3) 净水时,为了使水中悬浮的小颗粒沉降,可以向水中加入(填物质名称)。
-
(4) 硬水会给生产、生活带来很多问题,生活中可用 区分硬水和软水,可采用的方法降低水的硬度。
-
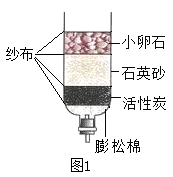
(5) 图2是小刚用身边的物品(饮料瓶、膨松棉、活性炭、细沙、小卵石等)制作的一个简易净水器。图2中的②处是(填上述物质名称)。其中小卵石、石英沙等作用是。其中活性炭的主要作用是。
-
(6) 自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为。
-
(7) 图3是过滤操作,该操作中玻璃棒的作用是。
-
(1) Ⅰ.粗盐的提纯
粗盐中含有不溶性泥沙、可溶性CaCl2 , MgCl2等杂质。学习小组设计了如下方案提纯粗盐:

用化学方程式表示Na2CO3溶液的作用:。
-
(2) “过滤”中玻璃棒的作用为;“操作X”的名称为。
-
(3) Ⅱ.探究氨盐水与二氧化碳的反应
步骤1:取50mL.浓氨水于锥形瓶中,加入NaCl晶体至不再溶解,制得氨盐水。
步骤2:向烧瓶中加入20mL氨盐水和约16g干冰,塞紧瓶塞,振荡、静置。一段时间后溶液中析出细小晶体,过滤、用冷水洗涤晶体并低温干燥。
(提出问题)晶体的成分是什么?
(实验探究1)①经甲同学检验,晶体中不含铵盐。甲同学的实验操作及现象是。
②乙同学取晶体少许,加入稀硝酸,晶体溶解并产生无色气体,再滴加几滴AgNO3溶液,未见明显现象,说明晶体中不含有离子。
(提出猜想)晶体的成分为Na2CO3或NaHCO3或两者的混合物。
(查阅资料)Na2CO3受热不分解;
NaHCO3受热易分解:2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑ (实验探究2)称取m1g晶体,利用下图装置(夹持仪器略)探究晶体的成分。
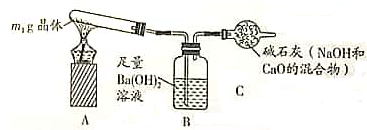
(实验现象)反应一段时间后,试管口凝结了少量小液滴,Ba(OH)2溶液变浑浊。
(实验分析)①晶体中一定含有(填化学式)。
②将晶体加热至残留固体的质量不断改变,测得残留固体的质量为m2g。
若m1g:m2g
 ,说明晶体为NaHCO3。
,说明晶体为NaHCO3。(拓展延伸)①氨盐水与二氧化碳反应所得铵盐的用途为。
②丙同学认为通过测定装置B中沉淀的质量,经计算分析也可确定晶体的组成。请对两同学的观点进行评价:。
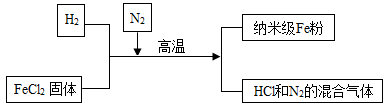
请回答下列问题:
-
(1) 上述流程中可以循环利用的物质是,在制备纳米级Fe粉的工艺流程中,其作用是。
-
(2) 纳米级Fe粉在氧气中能自发燃烧生成黑色固体,该反应的化学方程式为。
-
(3) 上述制备纳米级铁粉的化学方程式是,其反应类型为。
-
(4) 研究人员发现最后在制得的纳米级Fe粉样品中混有少量的
 杂质,为了除去样品中的杂质,在无氧环境下,先加水溶解,然后再洗涤、、烘干。
杂质,为了除去样品中的杂质,在无氧环境下,先加水溶解,然后再洗涤、、烘干。
-
(1) 将浑浊的河水用图1所示的简易净水器进行净化,其中活性炭的主要作用是,净化后得到的水属于(填“纯净物”或“混合物”)。
-
(2) 生活中常用来区分硬水和软水,生活中降低水的硬度的方法是。
-
(3) 下图是电解水的装置。
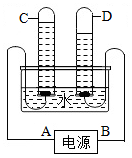
①试管D中收集的气体是,A是电源的极。
②理论上生成气体的体积比V(C)∶V(D)=。
③原子是化学变化中的最小微粒,若a→c→b可表示一种化合反应,那表示分解反应的顺序应该是。
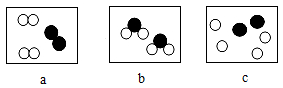
④运用分与合的思想都能证明水是组成的化合物,请写出电解水的化学方程式。
请回答以下问题:
-
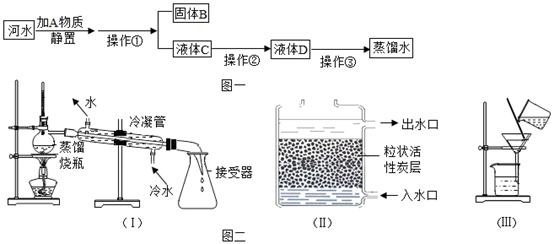
(1) 图一中,加入的A物质是絮凝剂,该物质的名称是;其作用是:。
-
(2) 图一中操作①②③对应图二中的装置分别是(填序号),其中除去水样中的色素和异味,所用试剂的名称为;单一净化水程度最高的是(写名称)。
-
(3) 图二中的装置(Ⅱ)从下端入水的目的是。
-
(4) 若经过操作①后,所得液体C中仍有浑浊,其原因可能是(写一点即可);要将浑浊的液体C变澄清还要进行的操作是。经上述操作后,检验所得液体是硬水,生活中转化硬水的方法是。
| | | | |
| A、过滤 | B、O2验满 | C、检查装置气密性 | D、取用固体粉末 |
 加热液体
B .
加热液体
B .  过滤液体
C .
过滤液体
C . 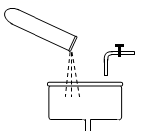 倾倒废液
D .
倾倒废液
D . 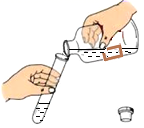 倾倒液体
倾倒液体
-
(1) 向水样中加入明矾搅拌溶解,静置一段时间后,进行(填操作名称),除去固体小颗粒,再向滤液中加入活性炭,利用其性除去水样中的颜色和异味。这样得到的水仍然是硬水,它会给生活带来许多不便,为了判断得到的水是硬水或软水,可加入。日常生活中可采用的方法将硬水软化。
-
(2) 河水中含有许多杂质,可利用吸附、沉降、过滤、蒸馏等方法净化,其中净水程度最高,能获得蒸馏水的是。
-
(3) 从分子及元素的角度看,地球表面的“水循环”主要是由的运动引起的,自然界“碳循环”中的“碳”是指。
-
(4) 水在自然环境中不易分解,但在通电的条件下可以分解,写出该反应的化学方程式。

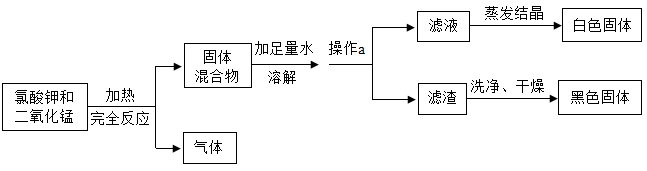
-
(1) 操作a的名称是。
-
(2) 在这个反应中二氧化锰的作用是。
-
(3) 请你计算:若制得1.92g氧气,则参加反应的氯酸钾(KClO3)的质量为g。
-
(4) 请你设计实验方案,证明滤渣已洗净。