氢气的制取和检验 知识点题库
实验室部分仪器或装置如图所示,请回答下列问题.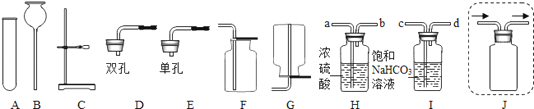
(1)实验室常用石灰石和稀盐酸制取二氧化碳气体,发生装置可选择图中的A、B、C、D 进行组装,反应的化学方程式为
(2)在制取过程中,小雨同学选用F装置收集二氧化碳,并用燃着的小木条放在瓶口验证二氧化碳是否收集满,结果发现小木条始终不灭,说明该瓶气体没有集满.出现上述情况的原因可能是1 , 2 , 3(写出其中3条).
(3)采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气.为获得纯净、干燥的二氧化碳气体,可选用图所示的H装置和I装置进行除杂和干燥,导管口连接的正确顺序是:气体→→F.
(4)在实验室中制取氢气,发生装置与制二氧化碳的相同,收集方法可采用(填“向上”或“向下”)排空气法.若用如图J所示装置采用“排空气法”收集氢气,请在图中将导管补画完整 .
实验室常用二氧化锰与浓盐酸来制备氯气,反应原理为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,实验装置如图1所示.
MnCl2+Cl2↑+2H2O,实验装置如图1所示. 
【查阅资料】
①氯气是黄绿色且有毒的气体,难溶于饱和食盐水;
②氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水;
③常温常压下,氢气的密度为0.09g/L.
-
(1) 【回答问题】
装置B的作用为;
根据装置C判断,氯气的密度比空气(填“大”或“小”);
装置D的作用为(用化学方程式表示)
-
(2)
【发现问题】
制备过程中,因盐酸浓度下降导致反应停止,某化学兴趣小组同学为测定装置A中反应后残余液中HCl的质量分数,提出两套测定方案如图3所示

方案Ⅰ中操作m的名称为,通过称量生成沉淀的质量,计算出残余液中HCl的质量分数,此测定方案是(填“可行”或“不可行”)的,原因是;
-
(3) 方案Ⅱ利用图2装置(固定仪器的装置已略)进行测定.
①实验过程中观察到锌粒表面有气泡产生,反应的化学方程式为?
②当装置恢复至常温时,测得反应生成气体的体积为183.5mL,根据化学方程式计算,残余液中HCl的质量分数为多少?
-
(4) 【反思讨论】
①为了保证方案Ⅱ测定结果的准确性,正确操作是:倾斜Y形管,(填标号)
a.将残余溶液转移到锌粒中 b.将锌粒转移到残余溶液中
②Y形管内空气对气体体积的测量(填“有”或“没有”)影响.

-
(1) H2O中氧、氢元素的质量比为.
-
(2) 分离器中分离出的副产品是,生产流程中能被循环利用的物质为.
-
(3) 写出膜反应器中HI气体发生分解反应的化学方程式(请注明反应条件).
-
(4) 尝试书写反应器中发生反应的化学方程式:(反应条件不做要求)
-
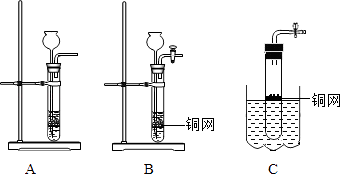
(1) 用装置A制取O2的化学方程式是.
-
(2) 小东同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,则B与A相比优点是.
-
(3) 在实验室用装置C制取CO2的化学反应方程式为,若隔离铜网改用铁丝做成,则产生的后果是.

-
(1) 用高锰酸钾制取氧气时,所选用的发生装置是(均填字母序号,下同);若用C装置收集氧气,当观察至导管口有气泡地放出时,即可进行收集.
-
(2) 用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是,该装置还可以用于实验室制氢气,其反应的化学方程式为;
-
(3) 乙炔又称电石气,是一种无色、无味、密度跟空气接近、不溶于水的气体;工业常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔.制取乙炔应选择的发生装置和收集装置是.

-
(1) A装置中发生反应的化学方程式为.
-
(2) 选择A装置制备气体最大的优点是.
该装置对反应物的状态和反应条件的要求是:.
-
(3) 运用A发生装置还可以制备初中化学常见的气体(填写化学式).写出实验室制备该气体的化学方程式.欲用B装置收集一瓶干燥的该气体,气体应由导管通入.(填a或b)
-
(4) 化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,然后选用上图装置(填写装置序号)可测量产生的CO2的体积,再利用此时CO2的密度,可计算CO2的质量,再根据CO2的质量求出样品中碳酸钙的质量.图中瓶内水面上油层的作用是.

实验步骤:①连接好装置;② ;③装入药品;④打开分液漏斗活塞,向锥形瓶中滴加稀盐酸;⑤一段时间后点燃酒精灯;⑥D中黑色固体完全变成红色,停止加热,待D中玻璃管冷却至室温,关闭分液漏斗活塞;⑦数据处理.
请回答下列问题:
-
(1) 补全实验步骤②.
-
(2) 若使制取氢气的装置随开随用,随关随停,如图2所示装置可选用的是.
-
(3) 长玻璃管的作用.
-
(4) 已知:CuO样品质量为m1克,E中增重为m2克,D中反应后固体质量为m3克,实际参加反应的氢气质量为m4克,试用m1、m2列出铜的相对原子质量的表达式.若无F装置,则对测定结果的影响(填“偏大”、“偏小”或“无影响”),以下数据还能确定铜的相对原子质量的是.
A、m1、m3 B、m1、m4 C、m2、m4 D、m3、m4
-
(5) 请你评价实验有什么不妥之处,并说明原因.

【查阅资料】无水硫酸铜遇水变蓝色
-
(1) 装置 A 中仪器①的名称是; 写出发生反应的化学方程式.
-
(2) 实验中看到 B 中无水硫酸铜变蓝色,说明产生的气体中含有杂质水.为了检验气体中还可能存在的杂质,可将 E 装置连接到上述装置( 填序号) 之间,气体从(填 a 或 b)进入装置 E.
-
(3) D 装置中的试剂是( 写出名称).
-
(4) 下列收集氢气的方法中符合题意的是 .A . 排水法 B . 向下排空气法 C . 干瘪的塑料袋 D . 塑料瓶.
 稀释浓硫酸
B .
稀释浓硫酸
B . 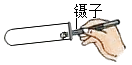 加入锌粒
C .
加入锌粒
C . 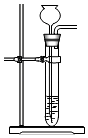 产生氢气
D .
产生氢气
D . 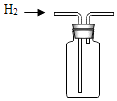 收集氢气
收集氢气
-
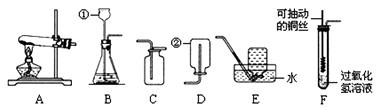
(1) 写出装置图中标号仪器的名称:①,②。
-
(2) 实验室制取二氧化碳的化学方程式为,选用的收集装置为(填字母),检验二氧化碳是否收集满的方法是。
-
(3) 实验室常用锌粒和稀硫酸反应制取氢气,选用的发生装置为(填字母)。
点燃氢气前,一定要。
-
(4) 查阅资料发现,氧化铜也可用作过氧化氢分解制氧气的催化剂,该反应的化学方程式为。若选用F作为氧气的发生装置,铜丝的螺旋处预先要在酒精灯上加热一段时间,目的是。
-
(1) 煤燃烧时产生NO2、等气体,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
-
(2) 在一定条件下,甲烷(CH4)和水反应(未配平)的微观示意图如图所示。

①W表示的物质的化学式是。
②该反应中两种生成物Z和W的分子个数比为。
-
(3) 实验室可用锌和稀硫酸反应制取氢气。写出该反应的化学方程式:。目前,氢气作为新能源在生活和生产中还未能广泛应用,其原因是。
-
(4) 在高温下,工业上以赤铁矿(主要成分是Fe2O3)和一氧化碳反应来炼铁的化学方程式为。
-
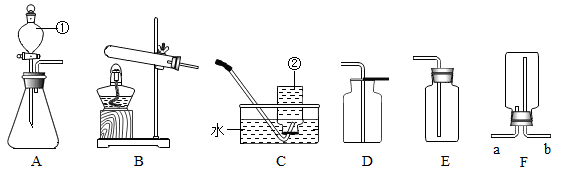
(1) 仪器①的名称是。
-
(2) 制取二氧化碳气体的发生装置可选择,实验室收集二氧化碳气体的装置可选择。(答一种即可)
-
(3) 若用F装置收集氢气,则氢气应从(填“a”或“b”)通入。
-
(4) 实验室利用A装置制取H2的反应方程式为

图1
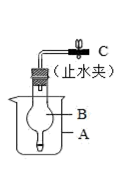
图2
-
(1) 装置图中仪器a的名称为。
-
(2) 写出以纯净物为原料用装置A制O2的化学方程式:。
-
(3) 若用G装置采用排空气法收集NH3 , 氨气应从口进(选“b”或“c”)。
-
(4) 医用H2O2在常温下难分解,但在双氧水溶液中加入铁锈,就会迅速分解,且反应结束后过滤出的铁锈可重复使用。试写出该反应的化学方程式:。若需要控制该反应的速率,应选择的发生装置为(填装置序号)。
-
(5) 某学生利用烧杯、球形干燥管和单孔橡皮塞等组成制取氢气的装置(如图2)。
①实验室制取氢气的化学方程式为。
②该装置B处应放的药品是。
③该装置的优点是(只需回答一点)。
④若使正在发生的反应停止,可以通过操作来实现。

-
(1) 写出图中仪器名称a b
-
(2) 对装置①中的固体加热时应先;若用装置⑥净化气体,则气体应从端通入(填“a”或“b”)。
-
(3) 实验用锌粒和稀硫酸制取氢气,欲得干燥的氢气,则应选择的装置有(选填编号),其反应方程式为。
-
(4) 实验室常用无水醋酸钠固体和碱石灰在加热条件下得到甲烷,已知甲烷难溶于水,密度比空气小,则制取甲烷发生装置应选,收集装置选(填序号)。

请回答下列问题:
-
(1) 标号为a的仪器名称是。
-
(2) 实验室高锰酸钾制取较纯净的氧气,选择的发生装置和收集装置是。
-
(3) 实验室用A、C装置组合制取某气体,写出其反应的化学方程式。
-
(4) 用F装置除去二氧化碳气体中少量水蒸气,F中应放入试剂名称是。

-
(1) 写出有标号仪器的名称:①;
-
(2) 实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为;若用充满水的D装置来收集氧气,气体应从(填“a”或“b”)端进入;
-
(3) 实验室制取氢气的化学方程式是;用装置C来制备氢气,使用注射器的优点是、。
-
(4) 用质量分数为37%的浓盐酸配制100g10%的盐酸,除了用到胶头滴管、玻璃棒和两种规格的量筒外,还需补充的一种仪器是。需要用量筒取用的水是mL(常温下水的密度为1g/mL)。

-
(1) 实验1中:一段时间后,能观察到的现象为。
-
(2) 实验2中:
①一段时间后,缓慢倾斜Y型管,将右侧的稀硫酸部分倒入左侧,依据现象,可得出结论:Zn的金属活动性比Cu强。
②写出Zn与稀硫酸反应的化学方程式。
-
(1) 生活中常用 的方法除去硬水中过多的(填离子符号)以得到软水。
-
(2) 图甲是水电解实验示意图。实验中,试管a与试管b中产生的气体的质量比为。

-
(3) 图乙是氢气的验纯实验,若氢气不纯,混有一定量的空气或氧气,点燃气体时,会发出。
-
(4) 有的同学利用所学的知识将浑浊的水用简易净水器(如图丙所示)进行净化,其中小卵石、石英砂的作用是。
-
(5) 下图是电解水的微观示意图。
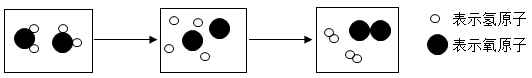
电解水生成氢气和氧气,由此说明水是由氢、氧两种元素组成的。电解水过程中保持不变的微粒是(用化学符号表示)。

-
(1) 图中标号为a的仪器名称是。
-
(2) 实验室常用锌和稀硫酸反应制取氢气,反应的化学方程式为;装置A、B都可作为实验室制取氢气的发生装置,与装置A相比,选用装置B的优点是,该装置还可用于实验室制取气体。
-
(3) 若用装置C排空气法收集氢气,则气体应从(选填“b”或“c”)端通入。



