钠的重要化合物 知识点题库
一块表面被氧化的钠质量是8.5g,投入到水中,完全反应得到标准状况下的H2 0.1g,则原钠块中被氧化的钠的质量是
A . 2.3g
B . 4.6g
C . 6.2g
D . 7.8g
某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
-
(1) NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为 。
-
(2) Fe2O3是主氧化剂,与Na反应生成的还原产物为 (已知该反应为置换反应).
-
(3) KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为 ,K的原子结构示意图为 。
-
(4) NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为 。
-
(5) 100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况).
①用碱石灰除去的物质为
②该产气药剂中NaN3的质量分数为
下列有关NaHCO3与Na2CO3的说法中,正确的是( )
A . 分别加热两种样品,没有残留物质是NaHCO3
B . 分别配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3
C . 分别配成溶液,向其中逐滴加入同浓度的盐酸反应,先产生CO2的是NaHCO3
D . 二者在一定条件下不能相互转化
为了验证NaHCO3固体中是否含有Na2CO3 , 下列实验事实及判断中,正确的是( )
A . 溶于水后加石灰水,看有无沉淀
B . 加稀盐酸观察是否有气体产生
C . 溶于水后加CaCl2溶液,看有无沉淀
D . 在无色火焰上灼烧,观察火焰是否呈黄色
将下列固体溶于水,再将其溶液加热蒸发,结晶后再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
A . ③④
B . ①③④
C . ①②③④⑤
D . 全部
氢化钠(NaH)是一种白色晶体,NaH与水反应放出H2 , 下列叙述不正确的是( )
A . NaH在水中显碱性
B . NaH中氢离子电子层排布与氦原子相同
C . NaH中氢离子半径比锂离子半径大
D . NaH中氢离子被还原为H2
下列说法不正确的是( )
A . 做CO还原CuO的实验时,尾气用点燃的方法除去
B . FeCl2、Na2O2、Fe(OH)3均可通过化合反应生成
C . 金属钠、钾起火,可用泡沫灭火器灭火
D . “水滴石穿”是因为溶解了CO2的雨水与CaCO3作用生成Ca(HCO3)2
下列物质与其用途完全符合的是( )
①Na2O2﹣供氧剂 ②晶体Si﹣太阳能电池 ③AgI﹣人工降雨 ④NaCl﹣制纯碱 ⑤Al2O3﹣焊接钢轨 ⑥NaClO﹣消毒剂⑦Fe2O3﹣红色油漆或涂料 ⑧SO2﹣食品漂白剂 ⑨NH3﹣制冷剂.
A . ①④⑤⑧⑨
B . ①②③⑥⑦⑨
C . ①②③④⑥⑦⑨
D . ①②③④⑤⑥⑦⑧⑨
下列关于氧化钠和过氧化钠的叙述中,正确的是( )
A . 都属于碱性氧化物
B . 都能与水发生化合反应
C . 水溶液的成分相同
D . 与二氧化碳反应生成不同的盐
下列物质的溶液在蒸发皿中加热蒸干并灼烧,最后得到该物质固体的是( )
A . 氯化铝
B . 碳酸氢钠
C . 硫酸镁
D . 高锰酸钾
下列有关物质用途的说法正确的是( )
A . 稀硫酸用于除铁锈
B . 碳酸钠用于治疗胃酸过多
C . 晶体硅用于制造光导纤维
D . 硫酸钡用于制作石膏绷带
取一定物质的量浓度的
NaOH 溶液 100 mL,向其中通入一定量的
CO2 气体,得到溶液 A,向A 中逐滴缓慢加入 2.00mol/L 的
HCl 溶液,产生的 CO2 气体体积
(标准状况)与所加
HCl 溶液的体积之间关系如图所示,请回答(结果留三位有效数字):

-
(1) A 溶液中的溶质。(用化学式表示)
-
(2) 通入的 CO2 的体积(标准状况)为L。
-
(3) 原 NaOH 溶液的物质的量浓度mol/L。
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | KAlO2 | 稀硫酸 |
| ② | KOH溶液 | NaHCO3 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
A . ①③
B . ①④
C . ②④
D . ②③
某NaOH样品中含有少量Na2CO3、NaHCO3和H2O,经分析测定,其中含NaOH83.4%(质量分数,下同), NaHCO3 8.8%,Na2CO3 6.4%,H2O 1.4%。将此样品若干克投入到49克21%的稀硫酸中,待反应完全后,需加入20克9.0%的NaOH溶液方能恰好中和。则蒸发中和后的溶液可得固体质量接近于( )
A . 25
B . 20
C . 15
D . 10
加热7.78g碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g。
-
(1) 原混合物中碳酸氢钠的质量为,反应的化学方程式为 。
-
(2) 将剩余固体溶于水,配成500mL溶液,所得溶液的物质的量浓度为。取出该溶液50mL,向其中逐滴滴入0.2mol/L盐酸35mL,完全反应后在标准状况下生成二氧化碳的体积为mL。
下表各选项中,不能通过置换反应实现由Y到W转化的一组化合物是( )
| A | B | C | D | |
| Y | CO2 | SiO2 | Na2O2 | Fe2O3 |
| W | MgO | CO | NaOH | Al2O3 |
A . A
B . B
C . C
D . D
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法错误的是( )
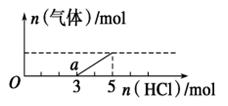
A . O点溶液中所含溶质的化学式为NaOH、Na2CO3
B . a点溶液中c (HCO3-) >c (CO32-)
C . 标准状况下,通入CO2的体积为44.8L
D . 原NaOH溶液的物质的量浓度为5mol/L
下列关于Na2CO3、NaHCO3的说法正确的是( )
A . 受热时Na2CO3较NaHCO3更不稳定,更易分解产生CO2
B . 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多
C . CaCl2溶液无法鉴别Na2CO3溶液和NaHCO3溶液
D . 等物质的量的两种盐与足量盐酸完全反应,Na2CO3所消耗HCl的物质的量是NaHCO3的两倍
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A . 在密闭容器中加入l.5mol H2和0.5molN2 , 充分反应后得到NH3分子数为NA
B . 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA
C . 1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA
D . 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA
下列钠及其化合物的叙述中正确的是( )
A . Na2O与Na2O2都能和水反应生成碱,他们都是化合反应
B . Na2CO3和NaHCO3都不稳定,受热容易分解
C . Na2O2可以作为呼吸面具或潜水艇里的氧气来源
D . 将Na2O加到酚酞溶液中,溶液先变色后褪色
最近更新



