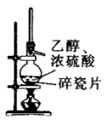
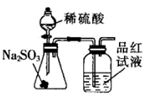
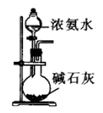
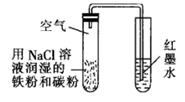
二氧化硫的漂白作用 知识点题库
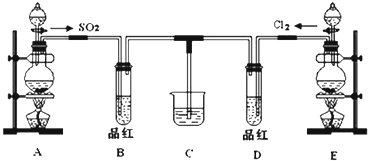
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置.

(1)实验室用装置A制备SO2 . 某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是: .
(2)实验室用装置E制备Cl2 , 其反应的化学化学方程式为:MnO2+4HCl(浓)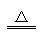 MnCl2+Cl2↑+2H2O.若有6mol的HCl参加反应,则转移的电子总数为 .
MnCl2+Cl2↑+2H2O.若有6mol的HCl参加反应,则转移的电子总数为 .
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B: ,D: .
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:B: ,D: .
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用化学方程式表示)提示SO2有较强的还原性. .
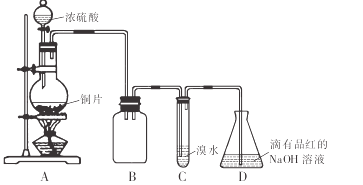
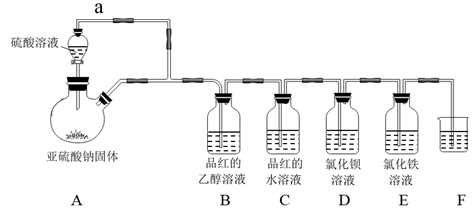
某化学兴趣小组设计如下实验方案.将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
-
(1) 装置B的作用是
-
(2) 设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式是 .装置D中NaOH全部转化为NaHSO3的标志是
-
(3) 向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3﹣与ClO﹣恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
序号
实 验操作
现 象
结 论
①
加几小块CaCO3固体
有气泡产生
I或Ⅱ
②
滴加少量淀粉KI溶液,振荡
Ⅲ
③
滴加少量溴水,振荡
Ⅱ
④
滴加少量酸性KMnO4溶液、振荡
溶液为紫色
-
(4) 请设计简单实验证明:室温下HSO3﹣的电离平衡常数Ka与水解平衡常数Kb , 的相对大小:
-
(1) 将相关的含硫物质分为如表所示3组,则第2组中物质X的化学式是.
第1组
第2组
第3组
S(单质)
SO2、X、Na2SO3、NaHSO3
SO3、H2SO4、Na2SO4、NaHSO4
-
(2) 实验室制取SO2的化学方程式为.
-
(3) 利用下图所示的装置研究SO2的性质:(熔点:SO2﹣76.1℃,SO3 16.8℃,沸点:SO2﹣10℃,SO3 45℃).
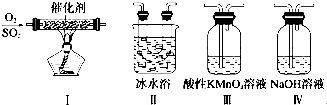
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是.
②甲同学按Ⅰ、Ⅱ、III、Ⅳ的顺序连接装置,装置Ⅱ的作用是; 装置Ⅲ中溶液逐渐褪色,生成Mn2+ , 则该反应的离子方程式是.
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40mL 2.5mol•L﹣1 NaOH溶液,反应后增重4.8g,则产物(水除外)的物质的量之比是.
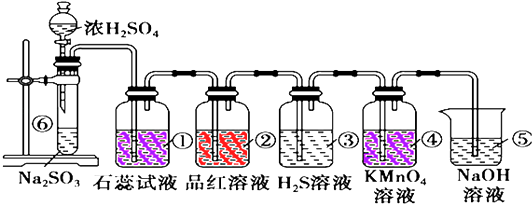
已知Na2SO3+H2SO4=Na2SO4+SO2+H2O
-
(1) ①中为紫色石蕊试液,实验现象为实验证明SO2是气体
-
(2) ②中为红色品红溶液,现象为证明SO2有性
-
(3) ④为紫红色高锰酸钾,实验现象为证明SO2有性.
-
(4) ⑤的作用反应方程式.
-
(1) 用装置A制备SO2 . 某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是.
-
(2) 实验室用装置E制备Cl2 , 该反应的化学方程式为,若反应中有1mol的HCl被氧化,则反应中转移的电子总数为.
-
(3) ①反应开始一段时间后,观察到B试管中的品红溶液出现的现象是:.
②停止通气后,再给D试管加热,试管中的现象为:.
-
(4) 另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中现象为.请你分析该现象的原因(用化学方程式表示):.
-
(5) SO2和Cl2均属于大气污染物,需要进行尾气处理(用装置C),则在装置C中的试剂是(填名称),请写出SO2和Cl2分别与该试剂反应的离子方程式;.
 CuSO4+SO2↑+2X
CuSO4+SO2↑+2X 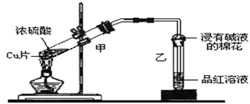
请回答下列问题:
-
(1) 通过试管乙中发生的现象,说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有性。
-
(2) 若要收集试管甲中生成的气体,可以采用方法收集(填序号)。
①排水取气法 ②向上排空气取气法 ③向下排空气取气法
-
(3) 补充试管甲中所发生反应的化学反应方程式中X物质(填分子式)。
-
(4) 试管乙口部浸有碱液的棉花的作用是,此防范措施也说明产生的气体是气体(填“酸性”、“中性”或“碱性”),(填“有”或“无”)毒性。
 的性质。下列离子方程式书写错误的是( )
的性质。下列离子方程式书写错误的是( ) 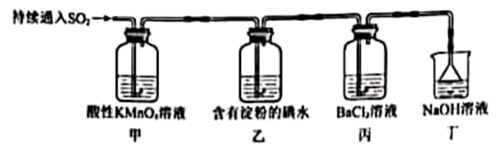
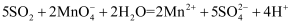 B . 乙中蓝色逐渐变浅:
B . 乙中蓝色逐渐变浅: 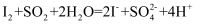 C . 丙中产生少量白色沉淀:
C . 丙中产生少量白色沉淀: 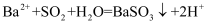 D . 丁中可能的反应:
D . 丁中可能的反应: 
-
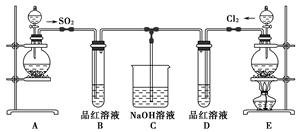
(1) 实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:;
-
(2) 实验室用装置E制备Cl2 , 其反应的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为;
MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为;
-
(3) ①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:,D:;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:。
D:。
 +2H2O
+2H2O
| A | B | C | D |
| | | | |
| 制取 | 验证 | 制取少量 | 检验该条件下铁发生了吸氧腐蚀 |
| A | B | C | D |
| | | | |
| 蒸发NaCl溶液获得NaCl晶体 | 分离CCl4和I2混合物 | 验证SO2的漂白性 | 制备少量的SO2 |
 可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料
可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料