工业合成氨 知识点题库
关于氨的合成工业的下列说法正确的是( )
A . 从合成塔出来的气体,其中氨气一般占15%,所以生产氨的工业的效率都很低
B . 由于NH3易液化,N2、H2可循环使用,则总的说来氨的产率很高
C . 合成氨工业的反应温度控制在400~500 ℃左右,目的是使平衡向正反应方向进行
D . 合成氨工业采用10 MPa~30 MPa,是因该条件下催化剂的活性最好
合成氨工业上采用循环操作,主要是为了( )
A . 加快反应速率
B . 提高NH3的平衡浓度
C . 降低NH3的沸点
D . 提高N2和H2的利用率
下列关于工业生产的说法正确的是( )
A . 在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气
B . 在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C . 在氯碱工业,电解槽一般用铁网作电极
D . 合成氨工业用天然气造气的方法中,与水蒸汽高温反应优于热分解法
化学无处不在,下列与化学有关的说法不正确的是( )
A . 侯氏制碱法的工艺过程中应用了物质溶解度的差异
B . 工业上以氯气和石灰乳为原料制备漂白粉
C . 单质硅常用做光导纤维的材料,这与硅的半导体性能有一定关系
D . 高压钠灯发出的黄光射程远、透雾能力强,常用做路灯
下列有关工业生产的叙述正确的是( )
A . 合成氨工业中,将NH3及时液化分离有利于加快反应速率
B . 氯碱工业中,使用离子交换膜可防止Cl2和NaOH溶液反应
C . 硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量
D . 硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响
实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
(1)从图中选择制取氮气的合适装置: (填编号)
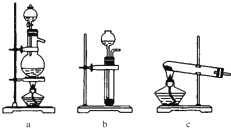
(2)氮气和氢气通过甲装置,甲装置的作用:① ② ③
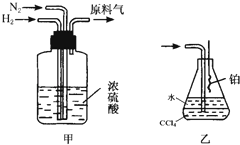
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能说明反应发生的现象是 ,乙装置中的CCl4的作用是 .
(4)反应结束后锥形瓶内的溶液中含有的离子有:H+、OH﹣、 、 .
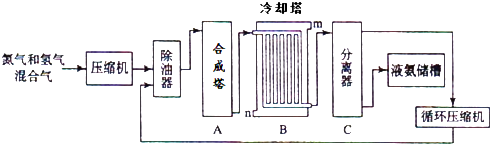
氨气是一种重要的化工产品,工业上可以按照下图所示流程生产氨气:
-
(1) 原料气之一氮气的工业制取方法是,写出氨气的工业用途(任答一点).
-
(2) 写出合成塔中发生的反应的化学反应方程式.
在冷却塔中对混合气体进行冷却,冷水的入口(答m或n).
-
(3) 设备C的作用.
其分离器中的过程对整个工业合成氨的意义.(试结合平衡移动原理回答)
-
(4) 在原料气制备过程中混有 CO对催化剂有毒害作用,欲除去原料气中的 CO,可通过如下反应来实现:CO(g)+H2O(g)⇌CO2(g)+H2(g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过80%,则起始物中c(H2O):c(CO)不低于(精确到小数点后一位).
向空气中“挖矿”,为人类粮食增产做出巨大贡献的化学工业是( )
A . 硫酸工业
B . 合成氨工业
C . 纯碱工业
D . 石油化工
合成氨工业是贵州省开磷集团的重要支柱产业之一。氨是一种重要的化工原料,在工农业生产中有广泛的应用。
-
(1) 在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)
 2NH3(g)。该可逆反应达到平衡的标志是。
2NH3(g)。该可逆反应达到平衡的标志是。 a.3v正(H2)=2v逆(NH3)
b.单位时间生成mmolN2的同时生成3mmolH2
c.容器内的总压强不再随时间而变化
d.混合气体的密度不再随时间变化
-
(2) 工业上可用天然气原料来制取合成氨的原料气氢气。某研究性学习小组的同学模拟工业制取氢气的
原理,在一定温度下,体积为2L的恒容密闭容器中测得如下表所示数据。请回答下列问题:
时间/min
CH4(mol)
H2O(mol)
CO(mol)
H2(mol)
0
0.40
1.00
0
0
5
a
0.80
c
0.60
7
0.20
b
0.20
d
10
0.21
0.81
0.19
0.64
①写出工业用天然气原料制取氢气的化学方程式:。
②分析表中数据,判断5min时反应是否处于平衡状态?(填“是”或“否”),前5min反应的平均反应速率v(CH4)=。
③反应在7~10min内,CO的物质的量减少的原因可能是 (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
将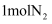 和
和 充入某密闭容器中,控制适当条件使其充分反应生成
充入某密闭容器中,控制适当条件使其充分反应生成 。下列关于合成氨反应的说法正确的是( )
。下列关于合成氨反应的说法正确的是( )
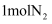 和
和 充入某密闭容器中,控制适当条件使其充分反应生成
充入某密闭容器中,控制适当条件使其充分反应生成 。下列关于合成氨反应的说法正确的是( )
。下列关于合成氨反应的说法正确的是( )
A . 该反应是吸热反应
B . 温度越高,压强越大,氨的平衡产率越高
C . 达到限度时正逆反应速率相等
D . 该容器中最终得到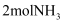
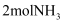
最近更新



