硫酸根离子的检验 知识点题库
用可溶性钡盐检验SO42﹣离子的存在时,先在待测溶液中加入盐酸,其作用是( )
A . 形成较多的白色沉淀
B . 形成的沉淀纯度更高
C . 排除SO42﹣以外其它阴离子及Ag+的干扰
D . 排除Ba2+以外的其它阳离子干扰
下列检验某溶液中是否含有SO42﹣的方法中正确的是( )
A . 向该溶液中加入酸化的Ba(NO3)2溶液出现白色沉淀,说明溶液中一定有SO42﹣
B . 向该溶液中加入BaCl2溶液出现白色沉淀,说明该溶液中一定有SO42﹣
C . 向该溶液中加入足量HCl,无现象,再加入BaCl2溶液出现白色沉淀,说明该溶液中一定有SO42﹣
D . 向该溶液中加入BaCl2溶液,产生白色沉淀,再加入HCl沉淀不溶解,说明该溶液中一定有SO42﹣
SO42﹣离子的检验试剂一般是 溶液,实验现象是 ,化学方程式为
检验未知溶液中是否含有SO 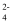 ,下列操作中最合理的是( )
,下列操作中最合理的是( )
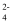 ,下列操作中最合理的是( )
,下列操作中最合理的是( )
A . 加入硝酸酸化的硝酸钡溶液
B . 先加硝酸酸化,再加入硝酸钡溶液
C . 加盐酸酸化了的BaCl2溶液
D . 先加盐酸酸化,再加入BaCl2溶液
下列实验,能证明溶液中一定含有SO42﹣的是( )
A . 某溶液加入BaCl2溶液,产生白色沉淀
B . 某溶液加入BaCl2溶液,产生白色沉淀,再加盐酸沉淀不溶解
C . 某溶液加入硝酸酸化,再加入Ba(NO3)2溶液有白色沉淀产生
D . 某溶液加入盐酸酸化,再加入BaCl2溶液有白色沉淀产生
下列由相关实验现象所推出的结论正确的是( )
A . NH4Cl和NH4HCO3受热都能分解,说明可以用加热NH4Cl和NH4HCO3固体的方法制氨气
B . 向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42-
C . NH3遇到浓盐酸产生白烟,说明二者发生反应生成白色固体
D . Fe与稀HNO3、稀H2SO4反应均有气泡产生。说明Fe与两种酸均发生置换反应
为了将混有Na2SO4、NH4HCO3的NaCl提纯。某学习小组设计了如图所示的方案:

-
(1) 操作①盛放药品的仪器名称是,发生反应的化学反应方程式为。
-
(2) 进行操作②后,如何判断杂质是否除尽?。
-
(3) 操作③的目的是。
-
(4) 请你评价该设计方案设计是否严密?若不严密,请说明理由,并提出改进方案。
下列实验方案中,能达到实验目的的是( )
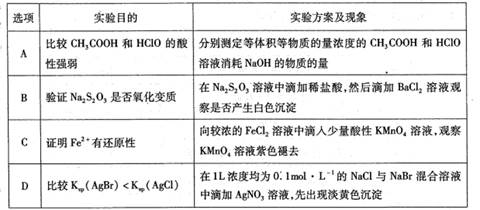
A . A
B . B
C . C
D . D
下列由相关实验现象所推出的结论正确的是( )
A . 分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
B . 向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42-
C . Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
D . Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性
将BaCl2溶液加入某无色溶液后,生成白色沉淀,再加入稀HNO3 , 则沉淀不溶解,下列说法正确的是( )
A . 一定存在Ag+
B . 一定存在CO32—
C . 一定存在SO42—
D . 以上说法都不对
由下列实验及现象,推出的相应结论正确的是( )
| 实验 | 现象 | 结论 |
| A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+ , 不含 K+ |
| B.漂白粉在空气中久置 | 变成块状固体 | 漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
| C.①某溶液中加入 Ba(NO3)2 溶液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 SO42﹣ |
| D.向碘水中加入等体积 CCl4 , 振荡后静置 | 上层接近无色,下层显紫红色 | I2 在CCl4中的溶解度大于在水中的溶解度 |
A . A
B . B
C . C
D . D
粗盐中含Ca2+、Mg2+、SO42-以及泥沙等杂质,为了除去可溶性杂质,首先将粗盐溶解,再通过以下实验步骤进行提纯:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。
-
(1) 以下操作顺序不合理的是_____________。A . ②⑤④③① B . ④⑤②①③ C . ⑤②④①③ D . ⑤④②①③
-
(2) 通过步骤①中过滤后的滤液,检验SO42-是否除尽的操作方法是。
-
(3) 实验室将上述得到的精制食盐水制成精盐的过程中,还需要进行某一操作,该操作中需要加热的仪器为:。
-
(4) 实验室需要450 mL 4.00 mol·L-1NaCl溶液,现利用提纯的NaCl进行配制,所用仪器除天平、药匙、烧杯、玻璃棒外还有(填仪器名称)。定容时,俯视刻度线,对所配溶液浓度的影响:(填:偏大、偏小、或无影响)。
某无色溶液中可能含有Na+、K+、NH 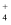 、Mg2+、Cu2+、SO
、Mg2+、Cu2+、SO 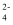 、SO
、SO 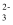 、Cl-、Br–、CO
、Cl-、Br–、CO 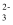 中的若干种,各离子浓度均为 0.1mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
中的若干种,各离子浓度均为 0.1mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
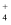 、Mg2+、Cu2+、SO
、Mg2+、Cu2+、SO 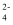 、SO
、SO 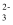 、Cl-、Br–、CO
、Cl-、Br–、CO 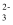 中的若干种,各离子浓度均为 0.1mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
中的若干种,各离子浓度均为 0.1mol•L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
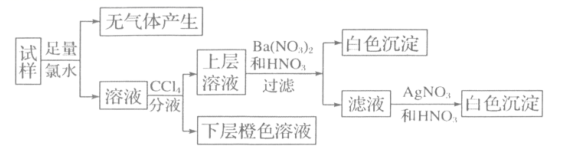 则关于原溶液的判断中正确的是( )
则关于原溶液的判断中正确的是( )
A . 无法确定原溶液中是否存在Cl-
B . 若步骤中 Ba(NO3)2 和 HNO3的混合溶液改用 BaCl2和盐酸, 则对溶液中离子的判断无影响
C . 肯定存在的离子是NH 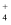 、Mg2+、SO
、Mg2+、SO 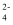 、Br–
D . 是否存在 Na+ 、K+需要通过焰色反应来确定
、Br–
D . 是否存在 Na+ 、K+需要通过焰色反应来确定
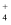 、Mg2+、SO
、Mg2+、SO 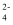 、Br–
D . 是否存在 Na+ 、K+需要通过焰色反应来确定
、Br–
D . 是否存在 Na+ 、K+需要通过焰色反应来确定
根据要求,回答下列问题:
-
(1) 写出离子反应方程式“Ba2++SO
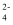 =BaSO4↓”对应的化学反应方程式。
=BaSO4↓”对应的化学反应方程式。
-
(2) 反应“2Na+O2
 Na2O2”,氧化产物是;产物中O的化合价为。
Na2O2”,氧化产物是;产物中O的化合价为。
-
(3) 维生素C 又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+ , 这说明维生素C具有。(填氧化性或还原性)
-
(4) 某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入溶液,再加入溶液发现有白色沉淀生成,并由此得出该混合物中含有硫酸盐的结论。
对下列事实的解释中,错误的是( )
A . 附着在试管内壁上的硫可用CS2洗涤,说明硫易溶于CS2
B . 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C . 向某溶液中加足量稀盐酸无现象,再加BaCl2溶液产生白色沉淀,说明该溶液中一定有 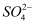 D . 常温下浓硫酸可以用铁质容器贮存,说明铁与浓硫酸不反应
D . 常温下浓硫酸可以用铁质容器贮存,说明铁与浓硫酸不反应
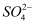 D . 常温下浓硫酸可以用铁质容器贮存,说明铁与浓硫酸不反应
D . 常温下浓硫酸可以用铁质容器贮存,说明铁与浓硫酸不反应
物质检验是化学研究常用的方法之一。下列有关溶液成分的检验,结论错误的是( )
A . 滴加 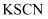 溶液,溶液变为红色,该溶液中一定存在
溶液,溶液变为红色,该溶液中一定存在  B . 加入稀盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中一定存在
B . 加入稀盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中一定存在  C . 滴加
C . 滴加 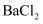 溶液产生白色沉淀,再加稀硝酸沉淀不溶解,该溶液中一定存在
溶液产生白色沉淀,再加稀硝酸沉淀不溶解,该溶液中一定存在  或
或  D . 加入足量浓
D . 加入足量浓  溶液、加热,产生有刺激性气味且能使湿润红色石蕊试纸变蓝的气体,该溶液中一定存在
溶液、加热,产生有刺激性气味且能使湿润红色石蕊试纸变蓝的气体,该溶液中一定存在 
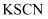 溶液,溶液变为红色,该溶液中一定存在
溶液,溶液变为红色,该溶液中一定存在  B . 加入稀盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中一定存在
B . 加入稀盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中一定存在  C . 滴加
C . 滴加 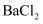 溶液产生白色沉淀,再加稀硝酸沉淀不溶解,该溶液中一定存在
溶液产生白色沉淀,再加稀硝酸沉淀不溶解,该溶液中一定存在  或
或  D . 加入足量浓
D . 加入足量浓  溶液、加热,产生有刺激性气味且能使湿润红色石蕊试纸变蓝的气体,该溶液中一定存在
溶液、加热,产生有刺激性气味且能使湿润红色石蕊试纸变蓝的气体,该溶液中一定存在 
某溶液中加入稀硫酸,能产生使澄清石灰水变浑浊的无色无味的气体;再加入氯化钡溶液,能产生白色沉淀。关于该溶液的下列结论中正确的是( )
A . 一定含有碳酸根离子
B . 一定含有碳酸氢根离子
C . 一定含有硫酸根离子
D . 可能含有硫酸根离子
根据下列实验操作和现象所得到的结论正确的是( )
| 实验操作和现象 | 实验结论 | |
| A | 向某溶液先滴加 | 原溶液中一定有 |
| B | 向 | |
| C | 向某溶液加入氢氧化钠溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝。 | 原溶液中一定无 |
| D | 将相同大小的铜片和锌片插入苹果中,用导线在铜片和锌片之间串联一个电流表,发现电流表的指针发生偏转。 | 水果电池产生的电流从锌片沿导线流向铜片 |
A . A
B . B
C . C
D . D
化学与生活息息相关,前不久央视曝光的毒胶囊事件,就是使用含铬的鞣制剂加工皮革的边角料制成明胶,再制成药用胶囊。由于重金属铬超标,这种胶囊严重危害消费者健康。
-
(1) Fe(CrO2)2是铬铁矿的主要成分,已知其中的Fe显+2价,则Cr的化合价为。CrO
 是一种酸根离子,则Fe(CrO2)2属于(填“酸”“碱”“盐”或“氧化物”)。
是一种酸根离子,则Fe(CrO2)2属于(填“酸”“碱”“盐”或“氧化物”)。
-
(2) 明胶的主要成分为蛋白质,溶于水形成胶体。明胶的水溶液和K2SO4溶液共同具备的性质是(填字母,下同)。
a.都不稳定,密封放置产生沉淀
b.两者均有丁达尔效应
c.分散质微粒可透过滤纸
-
(3) 已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置应选用下列中的___________。A .
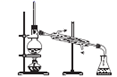 B .
B . 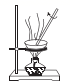 C .
C .  D .
D . 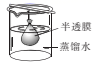
-
(4) 将10mL明胶的水溶液与5mLNa2SO4溶液混合装入半透膜内,再将此半透膜浸入盛蒸馏水的烧杯中,设计实验证明SO
 能够透过半透膜:。
能够透过半透膜:。
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
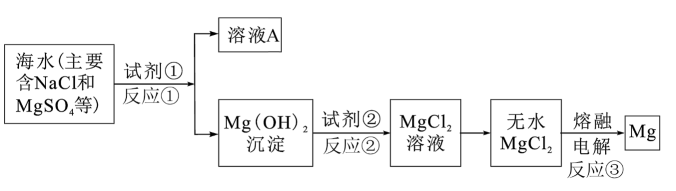
-
(1) 镁在元素周期表中的位置是。反应①②③中属于氧化还原反应的有。
-
(2) 为了使
 转化为
转化为 ;试剂①可以选用,确定海水中的
;试剂①可以选用,确定海水中的 已全部转化为
已全部转化为 的方法是。
的方法是。
-
(3) 若要检验溶液A中含有的
 , 使用的试剂是。
, 使用的试剂是。
-
(4) 无水
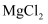 在熔融状态下,通电后会产生Mg和
在熔融状态下,通电后会产生Mg和 , 该反应的化学方程式为。
, 该反应的化学方程式为。
-
(5) 海水中本来就有氯化镁,从海水中制取
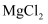 时,却要经历“
时,却要经历“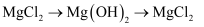 ”的转化。该转化过程的目的是。
”的转化。该转化过程的目的是。
最近更新
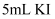 溶液中滴加5-6滴相同浓度
溶液中滴加5-6滴相同浓度  溶液,充分反应后滴入
溶液,充分反应后滴入 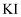 与
与 


